Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
AminoglycosiderArikayce
Resume af lægemiddeloversigt
Hvad er Arikayce?
Arikayce (Amikacin liposomindåndingssuspension) er et aminoglycosid Antibakteriel Indikeret hos voksne, der har begrænset eller ingen alternative behandlingsmuligheder til behandling af Mycobacterium avium -kompleks (MAC) lungesygdom som en del af en kombination af antibakterielt lægemiddelregime hos patienter, der ikke opnår negative sputumkulturer efter mindst 6 på hinanden følgende måneder af et multidrug -baggrundsregime -terapi. Dette lægemiddel er indikeret til brug i en begrænset og specifik population af patienter.
Hvad er bivirkninger af Arikayce?
Arikayce
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- Hoste (især i den første måned med brug af medicinen)
- problemer med at tale
- Ringer i dine ører
- Ændringer i høringen
- svimmelhed
- Spinning sensation
- Lightheadedness
- brysttæthed
- hvæsende
- åndenød
- Hoste blod
- lidt eller ingen vandladning
- hævelse i dine fødder eller ankler og
- træthed
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Almindelige bivirkninger af Arikayce inkluderer:
- vanskeligheder med at tale
- hoste
- Bronchospasme
- Hoste blod
- Skader på det indre øre
- Øvre luftvejsirritation
- Muskuloskeletalsmerter
- træthed
- svaghed
- Forværring af underliggende lungesygdom
- diarré og
- kvalme
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; og pludselig svimmelhed letthed eller udlevering;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til Arikayce
Den anbefalede dosering af Arikayce hos voksne er en gang daglig oral indånding af indholdet af en 590 mg/8,4 ml Arikayce -hætteglas. Brug kun Arikayce -hætteglas med Lamira Nebulizer -systemet.
Hvilke stoffer stoffer eller kosttilskud interagerer med Arikayce?
Arikayce kan interagere med ethacrynic acid furosemid Urea Intravenøs mannitol eller medicin forbundet med neurotoksicitet nefrotoksicitet og ototoksicitet. Fortæl din læge alle medicin og kosttilskud, du bruger.
Arikayce under graviditet eller amning
Fortæl din læge, hvis du er gravid eller planlægger at blive gravid, før du bruger Arikayce; Det kan skade et foster. Det er ukendt, om Arikayce passerer ind i modermælk. Kontakt din læge inden amning.
Yderligere oplysninger
Vores Arikayce (Amikacin liposomindåndingssuspension) til oral inhalationsanvendelse af bivirkninger lægemiddelcenter giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når man tager denne medicin.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Dosering
- Bivirkninger
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
ADVARSEL
Risiko for øgede respiratoriske bivirkninger
Arikayce har været forbundet med en øget risiko for respiratoriske bivirkninger, herunder overfølsomhed pneumonitis hemoptysis bronchospasme forværring af underliggende lungesygdom, der i nogle tilfælde har ført til indlæggelser ADVARSELS AND FORHOLDSREGLER ].
Beskrivelse af Arikayce
Den aktive ingrediens i Arikayce (amikacin liposomindåndingsophæng) er amikacinsulfat USP og aminoglycosid antibakteriel. Dens kemiske navn er d-streptamin O -3-amino-3-deoxy-a-dlucopyranosyl- (1 → 6)- O -[6-amino-6-deoxy-a-d-glucopyranosyl- (1 → 4)]- N 1 -(4-amino-2-hydroxy-1oxobutyl) -2-deoxy- ( S )- sulfat (1: 2) salt med en kemisk formel af C 22 H 43 N 5 O 13 • 2H 2 SÅ 4 med en molekylvægt på 781,76. Dens strukturelle formel er:
 |
Arikayce er en hvid mælkeagtig suspension bestående af amikacinsulfat indkapslet i liposomer og tilføres i en enhedsdosis 10 ml klart glashætteglas indeholdende amikacin 590 mg/8,4 ml (ækvivalent til amikakinsulfat 623 mg/8,4 ml) som en steril vandig liposomal suspension til oral-inhalation. Arikayce består af amikacinsulfat indkapslet i liposomer ved en målrettet koncentration på 70 mg amikacin/ml med pH -området 6,1 til 7,1 og lipid til amikacinvægtforhold i området 0,60 til 0,79. De inaktive ingredienser er kolesteroldipalmitoylphosphatidylcholin (DPPC) natriumchlorid -natriumhydroxid (til pH -justering) og vand til injektion.
Arikayce administreres kun ved hjælp af et Lamira Nebulizer -system [se Dosering og administration ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factellers. Under stogardized In vitro test pr. USP <1601> Voksen vejrtrækningsmønster (500 ml tidevandsvolumen 15 åndedræt pr. Minut og inhalation: udåndingsforhold på 1: 1) Den gennemsnitlige leverede dosis fra mundstykket var ca. 312 mg amikacinsulfat (53% af etiketskravet). Den massemedian aerodynamiske diameter (MMAD) af de nebuliserede aerosoldråber er ca. 4,7 μm (NULL,1 - 5,3 μm) som bestemt ved anvendelse af den næste generations Impactor (NGI) -metode. En procentdel af amikacinet i liposomet frigøres af forstøvningsprocessen, således at de næviseres Arikayce, der leverer en kombination af fri og liposomal amikacin.
Anvendelser til Arikayce
Begrænset befolkning: Arikayce ® er angivet hos voksne, der har begrænset eller ingen alternative behandlingsmuligheder til behandling af Mycobacterium avium Kompleks (MAC) lungesygdom som en del af en kombination af antibakterielt lægemiddelregime hos patienter, der ikke opnår negative sputumkulturer efter mindst 6 på hinanden følgende måneder af et multidrug baggrundsregime -terapi. Som kun begrænsede kliniske sikkerheds- og effektivitetsdata for Arikayce er i øjeblikket tilgængelige Reserve Arikayce til brug hos voksne, der har begrænset eller ingen alternative behandlingsmuligheder. Dette lægemiddel er indikeret til brug i en begrænset og specifik population af patienter.
Denne indikation er godkendt under accelereret godkendelse baseret på opnåelse af sputumkulturomdannelse (defineret som 3 på hinanden følgende negative månedlige sputumkulturer) efter måned 6. Klinisk fordel er endnu ikke etableret [se Kliniske studier ]. Continued approval feller this indication may be contingent upon verification og description of clinical benefit in confirmatellery trials.
Begrænsning af brug
Arikayce er kun blevet undersøgt hos patienter med ildfast MAC -lungesygdom defineret som patienter, der ikke opnåede negative sputumkulturer efter mindst 6 på hinanden følgende måneder af en multidrug baggrundsregimeterapi. Anvendelsen af Arikayce anbefales ikke til patienter med ikke-ærbødig MAC-lungesygdom.
Dosering til Arikayce
Vigtige administrationsinstruktioner
Arikayce er kun til oral inhalationsanvendelse. Administrer kun ved forstøvning med Lamira ® Nebulizer -system. Se instruktionerne til brug til fuld administrationsoplysninger om brug af Arikayce med Lamira Nebulizer -systemet.
Instruer patienter, der bruger en bronchodilator ('reliever') til først at bruge bronchodilatoren efter bronchodilator -folderen til brugsinformation, før du bruger Arikayce.
Forbehandling med kortvirkende selektive beta-2-agonister skal overvejes for patienter med kendt hyperreaktiv luftvejssygdom kronisk obstruktiv lungesygdom astma eller bronchospasme [se ADVARSELS AND FORHOLDSREGLER ].
Anbefalet dosering
Den anbefalede dosering af Arikayce hos voksne er en gang daglig inhalation af indholdet af en 590 mg/8,4 ml Arikayce Vial (590 mg amikacin) ved hjælp af Lamira Nebulizer -systemet [se Kliniske studier ].
Administrer kun Arikayce med Lamira Nebulizer -systemet. Arikayce skal være ved stuetemperatur inden brug. Før du åbner ryster Arikayce Vial godt i mindst 10 til 15 sekunder, indtil indholdet forekommer ensartet og godt blandet. Arikayce -hætteglasset åbnes ved at vende den plastiske top i hætteglasset og trækker nedad for at løsne metalringen. Metalringen og gummiproppen skal fjernes omhyggeligt. Indholdet af Arikayce -hætteglasset kan derefter hældes i medicinreservoiret fra forstøverhåndsættet.
Hvis en daglig dosis af Arikayce går glip af at administrere den næste dosis næste dag. Dobbelt dobbelt dosis for at kompensere for den ubesvarede dosis.
Hvor leveret
Dosering Fellerms And Strengths
Arikayce Leveres som en steril hvid mælkeagtig vandig liposomophæng til oral inhalation i et enhedsdosis glashætteglas indeholdende amikacin 590 mg/8,4 ml (svarende til amikacinsulfat 623 mg/8,4 ml).
Arikayce (Amikacin liposomindåndingssuspension) 590 mg/8,4 ml leveres i en steril enhedsdosis 10 ml glashætteglas. Produktet udleveres som et 28-dialkit.
Hver karton indeholder en 28-dages forsyning af medicin (28 hætteglas). Foruden Arikayce -hætteglassene i Carton One Lamira Nebulizer -håndsæt og fire Lamira Aerosol -hoveder leveres.
NDC 71558-590-28
Lamira Nebulizer -systemet indeholder en controller A Resare Aerosol Head et reserve håndsæt netledning og tilbehør.
Opbevaring og håndtering
Opbevar Arikayce hætteglas kølet ved 2 ° C til 8 ° C (36 ° F til 46 ° F) indtil udløbsdatoen på hætteglasset. Frys ikke . Når det er udløbet, skal du kaste ethvert ubrugt lægemiddel.
Arikayce can be stellered at room temperature up to 25°C (77°F) feller up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Fremstillet til: Insmed Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Revideret: Feb 2023
Bivirkninger for Arikayce
Følgende klinisk signifikante bivirkninger er beskrevet mere detaljeret i andre sektioner af mærkning:
- Hypersensitivitet pneumonitis [se Boksadvarsel og ADVARSELS AND FORHOLDSREGLER ]
- Hemoptysis [se Boksadvarsel og ADVARSELS AND FORHOLDSREGLER ]
- Bronchospasme [se Boksadvarsel og ADVARSELS AND FORHOLDSREGLER ]
- Forværring af underliggende lungesygdom [se Boksadvarsel og ADVARSELS AND FORHOLDSREGLER ]
- Anafylakse og overfølsomhedsreaktioner [se ADVARSELS AND FORHOLDSREGLER ]
- Ototoksicitet [se ADVARSELS AND FORHOLDSREGLER ]
- Nefrotoksicitet [se ADVARSELS AND FORHOLDSREGLER ]
- Neuromuskulær blokade [se ADVARSELS AND FORHOLDSREGLER ]
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, kan der ikke sammenlignes bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte med hastigheder i de kliniske forsøg med et andet lægemiddel og muligvis ikke afspejler de satser, der er observeret i praksis.
Oversigt over kliniske forsøg til sikkerhedsevaluering
Inden for det ildfaste NTM -kliniske program blev 404 patienter, der deltog i tre kliniske forsøg, behandlet med Arikayce i en dosis på 590 mg/dag (median varighed af eksponering for Arikayce var 236,5 dage).
Forsøg 1 (NCT Mycobacterium avium Kompleks (MAC) lungesygdom. Patienter blev randomiseret til enten 8 måneders Arikayce plus et baggrundsregime (n = 223) eller baggrundsregime alene (n = 112).
Forsøg 2 (NCT
Forsøg 3 (NCT Mycobacterium . Patienter blev randomiseret til enten Arikayce plus baggrundsregime (n = 44) eller en inhaleret fortyndet tom liposomplacebo plus baggrundsregime (n = 45) i 84 dage.
På tværs af alle kliniske forsøg med patienter med og uden ildfast NTM -lungeinfektion blev 818 patienter udsat for flere doser af Arikayce.
Bivirkninger, der fører til seponering af behandlingen
I de tre NTM -undersøgelser var der en højere forekomst af for tidlig seponering af Arikayce. I forsøget 14,5% ophørte Arikayce for tidligt; De fleste skyldtes bivirkninger (NULL,8%) og tilbagetrækning efter emne (NULL,9%). I komparatorarmen ophørte 10,7% af personerne deres baggrundsregime med 0,9% på grund af bivirkninger og 5,4% på grund af abstinens efter emne. I forsøg 2 (enkeltarmsudvidelsen af forsøg 1) blev 37,8% af patienterne, der starter på Arikayce, ophørt for tidligt med 24,4%, der ophørte på grund af bivirkninger. I forsøg 3 forekom alle 9 (NULL,5%) for tidlige ophør i Arikayce plus baggrundsregime-behandlede patienter, og der var ingen for tidlige ophør i placebo plus baggrundsregime.
Alvorlige bivirkninger i forsøg 1 og 3
I forsøg 1 19,7% af patienterne behandlet med Arikayce plus baggrundsregime rapporterede SAR sammenlignet med 16,1% af patienterne, der blev behandlet med baggrundsregime alene. Derudover i forsøg 1 [2 til 1 randomisering Arikayce plus baggrundsregime versus baggrundsregime alene] var der 80 hospitaliseringer hos 41 patienter (NULL,4%) behandlet med Arikayce plus baggrundsregime sammenlignet med 29 hospitaliseringer hos 15 patienter (NULL,4%) behandlet med baggrundsregime alene. De mest almindelige SAR'er og grunde til indlæggelse i Arikayce plus baggrundsregime var relateret til forværring af underliggende lungesygdom og nedre luftvejsinfektioner såsom lungebetændelse. I forsøg 3 18,2% af patienterne behandlet med Arikayce plus baggrundsregime rapporterede SARS sammenlignet med 8,9% af patienterne, der blev behandlet med baggrundsregime plus inhaleret placebo.
Fælles bivirkninger
Forekomsten af bivirkninger i forsøg 1 vises i tabel 1. Kun de bivirkninger med en hastighed på mindst 5% i Arikayce Plus -baggrundsregimetgruppen og større end baggrundsregimet alene vises.
Tabel 1: Bivirkninger i ≥ 5% af Arikayce-behandlede Mac-patienter og hyppigere end baggrundsregime alene i forsøg 1
| Bivirkning | Arikayce plus Background Regimen (N = 223) n (%) | Baggrundsregime alene (N = 112) n (%) |
| Dysfonia a | 106 (48) | 2 (2) |
| Hoste b | 88 (40) | 19 (17) |
| Bronchospasme c | 64 (29) | 12 (11) |
| Hemoptysis | 41 (18) | 15 (13) |
| Muskuloskeletalsmerter d | 40 (18) | 10 (9) |
| Øvre luftvejsirritation e | 39 (18) | 2 (2) |
| Elitudeicitet f | 38 (17) | 11 (10) |
| Træthed og astheni | 36 (16) | 11 (10) |
| Forværring af underliggende lungesygdom g | 34 (15) | 11 (10) |
| Diarre | 28 (13) | 5 (5) |
| Kvalme | 26 (12) | 4 (4) |
| Hovedpine | 22 (10) | 5 (5) |
| Lungebetændelse h | 20 (9) | 10 (9) |
| Pyrexia | 17 (8) | 5 (5) |
| Vægten faldt | 16 (7) | 1 (1) |
| Opkast i | 15 (7) | 4 (4) |
| Udslæt j | 14 (6) | 1 (1) |
| Ændring i sputum k | 13 (6) | 1 (1) |
| Bryst ubehag | 12 (5) | 3 (3) |
| a Inkluderer afonia og dysfoni b Inkluderer hoste produktiv hoste og øvre luftvejshostsyndrom c Inkluderer astma bronchial hyperreaktivitet bronchospasme dyspnø dyspnø anstrengende langvarig udløb hals stramhed og vejrtrækning d Inkluderer rygsmerter Arthralgia Myalgia Pain/Body Aches Muskel Spasmer og muskuloskeletalsmerter e Inkluderer oropharyngeal smerte oropharyngeal ubehag i halsen irritation faryngeal erythema øvre luftvejsinflammation pharyngeal ødemer stemmesnor betændelse laryngeal smerte laryngeal erythema laryngitis f Inkluderer døvhed døvhed neurosensorisk døvhed ensidig svimmelhed hypoacusis presyncope tinnitus vertigo balance lidelser g Inkluderer KOLS -infektionsforværring af KOLS -infektionsforværring af bronchiectasis h Inkluderer atypisk lungebetændelse Empyema -infektion Pleural effusion Nedre luftvejsinfektion Lunginfektion Lungeinfektion Pseudomonas Lungebetændelse Pneumonia Aspiration Pneumonia Pseudomonas Pseudomonas Infektion og luftvejsinfektion i Inkluderer opkast og post-tussiv opkast j Inkluderer udslæt udslæt makulo-papulært lægemiddeludbrud og urticaria k Inkluderer øget sputum sputum purulent og sputum misfarvet |
Valgte bivirkninger, der opstod i <5% of patients og at higher frequency in Arikayce-treated patients in Trial 1 are presented in Table 2.
Tabel 2: Valgte bivirkninger i <5% of Arikayce-treated MAC Patients og Mellere Frequent than Baggrundsregime alene in Trial 1
| Bivirkning | Arikayce plus Background Regimen N = 223 n (%) | Baggrundsregime alene N = 112 n (%) |
| Angst a | 10 (5) | 0 (0) |
| Oral svampeinfektion b | 9 (4) | 2 (2) |
| Bronchitis | 8 (4) | 3 (3) |
| Dysgeusia | 7 (3) | 0 (0) |
| Hypersensitivitet pneumonitis c | 7 (3) | 0 (0) |
| Tør mund | 6 (3) | 0 (0) |
| Epistaxis | 6 (3) | 1 (1) |
| Åndedrætssvigt d | 6 (3) | 2 (2) |
| Pneumothorax e | 5 (2) | 1 (1) |
| Træningstolerance faldt | 3 (1) | 0 (0) |
| Balanceforstyrrelse | 3 (1) | 0 (0) |
| Neuromuskulær lidelse f | 2 (1) | 0 (0) |
| a Inkluderer angst og angstlidelse b Inkluderer oral candidiasis og oral svampeinfektion c Inkluderer allergisk alveolitis interstitiel lungesygdom og pneumonitis d Inkluderer akut luftvejssvigt og åndedrætssvigt e Inkluderer pneumothorax pneumothorax spontan og pneumomediastinum f Inkluderer muskelsvaghed og neuropati perifer |
Se tabel 1 og tabel 2 for forekomsten af overfølsomhed pneumonitis bronkospasme hoste dysfoni forværring af underliggende sygdom hæmoptysis ototoksicitet øvre luftvejsirritation og neuromuskulære lidelser [se ADVARSELS AND FORHOLDSREGLER ].
Oplevelse af postmarketing
Følgende bivirkninger er blevet identificeret ud fra overvågning af postmarketing. Fordi disse bivirkninger rapporteres frivilligt fra en population af ukendte størrelse præcise estimater af frekvens ikke kan foretages, og et årsagsforhold til lægemiddeleksponering kan ikke fastlægges.
Immunsystemforstyrrelser: Hypersensitivitet Anaphylaxis [se ADVARSELS AND FORHOLDSREGLER ]
Lægemiddelinteraktioner for Arikayce
Lægemidler med neurotoksisk nefrotoksisk eller ototoksisk potentiale
Undgå samtidig brug af arikayce med medicin forbundet med neurotoksicitet nefrotoksicitet og ototoksicitet.
Ethacrynic acid furosemid urinstof eller mannitol
Nogle diuretika kan forbedre aminoglycosid -toksicitet ved at ændre aminoglycosidkoncentrationer i serum og væv. Undgå samtidig brug af Arikayce med ethacrynic acid furosemid Urea eller intravenøs mannitol.
Advarsler for Arikayce
Inkluderet som en del af 'FORHOLDSREGLER' Afsnit
Forholdsregler for Arikayce
Hypersensitivitet pneumonitis
Hypersensitivitet pneumonitis has been repellerted with the use of Arikayce in the clinical trials. Hypersensitivitet pneumonitis (repellerted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Arikayce) was repellerted at a higher frequency in patients treated with Arikayce plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Arikayce og received treatment with cellerticosteroids [see Bivirkninger ]. If hypersensitivity pneumonitis occurs discontinue Arikayce og manage the patient as medically appropriate.
Hemoptysis
Hemoptysis has been repellerted with the use of Arikayce in the clinical trials. Hemoptysis was repellerted at a higher frequency in patients treated with Arikayce plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Bivirkninger ]. If hemoptysis occurs manage the patients as medically appropriate.
Bronchospasme
Bronchospasme has been repellerted with the use of Arikayce in the clinical trials. Bronchospasme (repellerted as asthma bronchial hyperreactivity Bronchospasme dyspnea dyspnea exertional prolonged expiration throat tightness hvæsende) was repellerted at a higher frequency in patients treated with Arikayce plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Bivirkninger ]. If Bronchospasme occurs during the use of Arikayce treat the patients as medically appropriate.
Forværring af underliggende lungesygdom
Forværringer af underliggende lungesygdom er rapporteret ved anvendelse af Arikayce i de kliniske forsøg. Forværringer af underliggende lungesygdom (rapporteret som kronisk obstruktiv lungesygdom Infektionsforværring af kronisk obstruktiv lungesygdom Infektionsforværring af bronchiectasis) er rapporteret med en højere frekvens hos patienter behandlet med Arikayce Plus en baggrundsregime (NULL,2%) sammenlignet med patienter behandlet med baggrundsregimen alene (NULL,8%) [See plus et baggrundsregime (NULL,2%) sammenlignet med patienter, der er behandlet med baggrundsregimen alene (NULL,8%) [Se se Bivirkninger ]. If exacerbations of underlying pulmonary disease occur during the use of Arikayce treat the patients as medically appropriate.
Anafylakse og overfølsomhedsreaktioner
Der er rapporteret om alvorlige og potentielt livstruende overfølsomhedsreaktioner inklusive anafylaksi hos patienter, der tager Arikayce. Tegn og symptomer inkluderer akut indtræden af hud og slimhindevævets overfølsomhedsreaktioner (elveblommer kløende skylle hævede læber/tunge/uvula) Respiratorisk vanskelighed (åndenød i åndenød i stridor hoste) Gastrointestinale symptomer (kvalme (Tachycarding Diyrrhea Crampy Abdominal Pain) og Cardiovaskulære signer og symptomer om enapylayls (TACHYCYDIA Lavt blodtryk Synkope inkontinens svimmelhed). Før terapi med Arikayce indføres evaluering for tidligere overfølsomhedsreaktioner på aminoglycosider. Hvis anafylaksi eller en overfølsomhedsreaktion forekommer, afbryder Arikayce og institutioner passende understøttende foranstaltninger.
Elitudeicitet
Elitudeicitet With Use Of Arikayce
Elitudeicitet has been repellerted with the use of Arikayce in the clinical trials. Elitudeicitet (including deafness svimmelhed presyncope tinnitus og vertigo) were repellerted with a higher frequency in patients treated with Arikayce plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Arikayce plus background regimen vs. 0.9% in the background regimen alone arm) og svimmelhed (6.3% in Arikayce plus background regimen vs. 2.7% in the background regimen alone arm) [see Bivirkninger ].
Overvåg nøje patienter med kendt eller mistænkt auditiv eller vestibulær dysfunktion under behandling med Arikayce. Hvis ototoksicitet forekommer, skal du styre patienten som medicinsk passende, inklusive potentielt at afbryde Arikayce.
Risiko for ototoksicitet på grund af mitokondrielle DNA -varianter
Tilfælde af ototoksicitet med aminoglycosider er blevet observeret hos patienter med visse varianter i den mitokondrialt kodede 12S rRNA-gen (MT-RNR1), især M.1555A> G-varianten. Ototoksicitet forekom hos nogle patienter, selv når deres aminoglycosid -serumniveauer var inden for det anbefalede interval. Mitokondrielle DNA -varianter er til stede i mindre end 1% af den generelle amerikanske befolkning, og andelen af de variantbærere, der kan udvikle ototoksicitet såvel som sværhedsgraden af ototoksicitet, er ukendt. I tilfælde af kendt modershistorie om ototoksicitet på grund af aminoglycosidbrug eller en kendt mitokondrisk DNA -variant i patienten overvejer andre alternative behandlinger end aminoglycosider, medmindre den øgede risiko for permanent høretab opvejes af sværhedsgraden af infektion og mangel på sikre og effektive alternative terapier.
Nefrotoksicitet
Nefrotoksicitet was observed during the clinical trials of Arikayce in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Bivirkninger ]. Nefrotoksicitet has been associated with the aminoglycosides. Close monitellering of patients with known eller suspected renal dysfunction may be needed when prescribing Arikayce.
Neuromuskulær blokade
Patienter med neuromuskulære lidelser blev ikke tilmeldt Arikayce kliniske forsøg. Aminoglycosider kan forværre muskelsvaghed ved at blokere frigivelsen af acetylcholin ved neuromuskulære forbindelser. Overvåg nøje patienter med kendte eller mistænkte neuromuskulære lidelser, såsom myasthenia gravis. Hvis neuromuskulær blokade forekommer, kan det vendes ved indgivelse af calciumsalte, men mekanisk respiratorisk hjælp kan være nødvendig.
Embryo-føtal toksicitet
Aminoglycosides kan forårsage føtal skade, når de administreres til en gravid kvinde. Aminoglycosider inklusive Arikayce kan være forbundet med total irreversibel bilateral medfødt døvhed hos pædiatriske patienter udsat i utero . Patienter, der bruger Arikayce under graviditet eller bliver gravide, mens de tager Arikayce, skal vurderes om den potentielle fare for fosteret [se Brug i specifikke populationer ].
Oplysninger om patientrådgivning
Rådgiv patienten om at læse den FDA-godkendte patientmærkning ( Medicin vejledning og Patient Instructions feller Use ).
Vigtige instruktioner til administration af Arikayce
Instruer patienter om at læse instruktionerne til brug, før de starter Arikayce. Instruer patienter om kun at bruge Lamira ® Nebulizer -system til administration af Arikayce. Rådgiv patienten eller plejeren om ikke at bruge Lamira Nebulizer -systemet med nogen anden medicin.
Hypersensitivitet pneumonitis And Bronchospasme (Difficulty Breathing)
Rådgive patienter om at informere deres sundhedsudbyder, hvis de oplever åndenød eller vejrtrækning efter administration af Arikayce. Rådgiv patienter med en historie med reaktiv luftvejsygdom astma eller bronchospasme til at administrere Arikayce efter at have brugt en kortvirkende bronchodilator [se ADVARSELS AND FORHOLDSREGLER ].
Hemoptysis Or Hoste
Rådgive patienter om at informere deres sundhedsudbyder, hvis de hoster blod eller oplevelse af episodisk hoste enten under eller efter Arikayce -administrationen, især i den første måned efter start af Arikayce [se ADVARSELS AND FORHOLDSREGLER og Bivirkninger ].
Forværringer af underliggende lungesygdom
Rådgive patienter om at informere deres sundhedsudbyder, hvis de oplever forværring af deres lungesygdom efter at have startet Arikayce [se ADVARSELS AND FORHOLDSREGLER ].
Dysfonia Or Difficulty Speaking
Rådgiv patienter om at informere deres sundhedsudbyder, hvis de har svært ved at tale. Der er rapporteret om vanskeligheder med at tale eller tab af evne til at tale med Arikayce [se Bivirkninger ].
Anafylakse og overfølsomhedsreaktioner
Rådgive patienter og plejere om, at alvorlige og potentielt livstruende overfølsomhedsreaktioner, der kræver øjeblikkelig behandling, kan forekomme. Rådgive patienten om at afbryde Arikayce og søge øjeblikkelig lægehjælp, hvis der opstår tegn eller symptomer på en overfølsomhedsreaktion [se ADVARSELS AND FORHOLDSREGLER ].
Elitudeicitet (Ringing In The Ears)
Rådgive patienter om at informere deres sundhedsudbyder, hvis de oplever at ringe i ørerne svimmelhed eller eventuelle ændringer i høringen, fordi Arikayce har været forbundet med høretab [se ADVARSELS AND FORHOLDSREGLER ].
Rådgiv patienten om ikke at betjene tunge maskiner eller udføre farlige aktiviteter, mens Arikayce indåndes gennem Lamira Nebulizer -systemet, fordi Arikayce kan forårsage symptomer som svimmelhed eller respirationssymptomer.
Nefrotoksicitet Or Kidney Damage
Rådgive patienter om at informere deres sundhedsudbyder, hvis de har nyreproblemer, fordi nyreskader er rapporteret med aminoglycosider [se ADVARSELS AND FORHOLDSREGLER ]. Neuromuskulær blokade Advise patients to infellerm their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see ADVARSELS AND FORHOLDSREGLER ].
Embryo-føtal toksicitet
Rådgive gravide kvinder om, at aminoglycosider inklusive Arikayce kan forårsage irreversibel medfødt døvhed, når de administreres under graviditet [se ADVARSELS AND FORHOLDSREGLER og Brug i specifikke populationer ].
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
I en 2-årig inhalationscarcinogenicitetsundersøgelsesrotter blev rotter udsat for Arikayce for 15-25 50-70 eller 155170 minutter om dagen i 96-104 uger. Disse gav omtrentlige inhalerede doser på 5 15 og 45 mg/kg/dag. Pladecellecarcinom blev observeret i lungerne på 2 af 120 rotter, der blev administreret den højeste dosis, der blev testet. Maksimale serum AUC -niveauer af amikacin hos rotterne ved stabil tilstand var ca. 1,3 2,8 og 7,6 mcg · time/ml ved henholdsvis de lave midt- og høje doser sammenlignet med 23,5 mcg · HR/ml (NULL,0 til 46,5 mcg · HR/ml) målt hos mennesker. De pladecellecarcinomer kan være resultatet af en høj lungebyrde af partikler fra Arikayce i rotte -lungen. Relevansen af lungetumorresultaterne med hensyn til mennesker, der modtager Arikayce, er ukendt.
Der blev ikke observeret noget bevis for mutagenicitet eller genotoksicitet i et batteri på In vitro og forgæves Genotoksicitetsundersøgelser med en liposom-indkapslet amikacin-formulering svarende til Arikayce ( In vitro Mikrobiel mutagenesetest In vitro Muslymfommutationsassay In vitro kromosomal afvigelsesundersøgelse og en forgæves Micronucleus -undersøgelse hos rotter).
Ingen fertilitetsundersøgelser blev udført med Arikayce. Intraperitoneal administration af amikacin til han- og hunrotter ved doser op til 200 mg/kg/dag før parring gennem drægtighedsdag 7 var ikke forbundet med svækkelse af fertilitet eller bivirkninger på den tidlige embryonale udvikling.
Brug i specifikke populationer
Graviditet
Risikooversigt
Der er ingen data om Arikayce-brug hos gravide kvinder til at evaluere for nogen medikamentassocieret risiko for større fødselsdefekter spontanabort eller ugunstige moder- eller føtalesultater. Selvom systemisk absorption af amikacin efter oral inhalation forventes at være lav [se Klinisk farmakologi ] Systemisk eksponering for aminoglycosid -antibakterielle lægemidler inklusive Arikayce kan være forbundet med total irreversibel bilateral medfødt døvhed, når de administreres til gravide kvinder [Se ADVARSELS AND FORHOLDSREGLER ]. Advise pregnant women of the potential risk to a fetus.
Dyreforlængelse af toksikologiske undersøgelser er ikke blevet udført med inhaleret amikacin. Subkutan administration af amikacin til gravide rotter (op til 100 mg/kg/dag) og mus (op til 400 mg/kg/dag) under organogenese var ikke forbundet med føtal misdannelser. Ototoksicitet blev ikke evalueret tilstrækkeligt hos afkom i dyreforsøg.
Den estimerede baggrundsrisiko for store fødselsdefekter og spontanabort for de angivne populationer er ukendt. Alle graviditeter har en baggrundsrisiko for tab af fødselsdefekt eller andre bivirkninger. I den amerikanske generelle befolkning er den estimerede baggrundsrisiko for større fødselsdefekter og spontanabort i klinisk anerkendte graviditeter henholdsvis 2-4% og 15-20%.
Data
Dyredata
Der er ikke udført nogen dyreproduktionstoksikologundersøgelser med Arikayce eller ikke-liposomal amikacin administreret ved inhalation.
Amikacin blev underkutant administreret til gravide rotter (drægtighedsdage 8-14) og mus (drægtighedsdage 7-13) i doser på 25 100 eller 400 mg/kg for at vurdere udviklingstoksicitet. Disse doser forårsagede ikke føtal visceral eller skeletmalformationer hos mus. Den høje dosis var overdreven maternalt giftig hos rotter (nefrotoksicitet og dødelighed blev observeret), der udelukkede evalueringen af afkom i denne dosis. Føtale misdannelser blev ikke observeret ved den lave eller midterste dosis hos rotter. Postnatal udvikling af rotter og mus udsat for disse doser af amikacin i utero adskiller sig ikke signifikant fra kontrol.
Elitudeicitet was not adequately evaluated in offspring in animal developmental toxicology studies.
Amning
Risikooversigt
Der er ingen oplysninger om tilstedeværelsen af Arikayce i human mælk Virkningerne på det ammede spædbarn eller virkningerne på mælkeproduktionen efter administration af Arikayce ved indånding. Selvom begrænsede offentliggjorte data om andre administrationsruter af amikacin indikerer, at amikacin er til stede i human mælke -systemisk absorption af Arikayce efter inhaleret administration forventes at være lav [se Klinisk farmakologi ]. The developmental og health benefits of breastfeeding should be considered along with the mother’s clinical need feller Arikayce og any potential adverse effects on the breastfed child from Arikayce eller from the underlying maternal condition.
Pædiatrisk brug
Sikkerhed og effektivitet af Arikayce hos pædiatriske patienter under 18 år er ikke blevet fastlagt.
Geriatrisk brug
I NTM -kliniske forsøg med det samlede antal patienter, der fik Arikayce 208 (NULL,5%), var ≥ 65 år og 59 (NULL,6%) ≥ 75 år. Der blev ikke observeret nogen samlede forskelle i sikkerhed og effektivitet mellem ældre forsøgspersoner og yngre forsøgspersoner. Fordi ældre patienter er mere tilbøjelige til at have reduceret nyrefunktionen, kan det være nyttigt at overvåge nyrefunktionen [se ADVARSELS AND FORHOLDSREGLER ].
Leverskrivning i leveren
Arikayce has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Klinisk farmakologi ].
v 2355 rund hvid pille kodein
Nedskærmning af nyren
Arikayce has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Arikayce clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitellered in patients with known eller suspected renal impairment including elderly patients with potential age-related decreases in renal function [see ADVARSELS AND FORHOLDSREGLER Geriatrisk brug ].
Overdoseringsoplysninger til Arikayce
Bivirkninger, der er specifikt forbundet med overdosis af Arikayce, er ikke identificeret. Akut toksicitet bør behandles med øjeblikkelig tilbagetrækning af Arikayce og baseline -test af nyrefunktion bør udføres.
Hæmodialyse kan være nyttigt til at fjerne amikacin fra kroppen.
I alle tilfælde af mistanke om overdosering skal læger kontakte Regional Poison Control Center for information om effektiv behandling. I tilfælde af overdosering bør muligheden for lægemiddelinteraktioner med ændringer i lægemiddeldisposition overvejes.
Kontraindikationer for Arikayce
Arikayce is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Klinisk farmakologi feller Arikayce
Handlingsmekanisme
Arikayce is an Antibakteriel drug [see Mikrobiologi ].
Farmakodynamik
Arikayce exposure-response relationships og the time course of pharmacodynamic response are unknown.
Farmakokinetik
Sputumkoncentrationer
Efter en gang daglig inhalation af 590 mg Arikayce i Mycobacterium avium Komplekse (MAC) patienter sputumkoncentrationer ved 1 til 4 timer efter inhalation var 1720 884 og 1300 mcg/g henholdsvis 1 3 og 6 måneder. Høj variation i amikacin -koncentrationer blev observeret (CV%> 100%). Efter 48 til 72 timer efter inhalation faldt amikacin-sputumkoncentrationer til ca. 5% af dem 1 til 4 timer efter inhalation.
Serumkoncentrationer
Efter 3 måneder med en gang daglig inhalation af 590 mg arikayce hos Mac-patienter var det gennemsnitlige serum AUC0-24 23,5 mcg*HR/ml (interval: 8,0 til 46,5 mcg*HR/ml; n = 12) og den gennemsnitlige serum Cmax var 2,8 mcg/ml (interval: 1,0 til 4,4 μg/ml; n = 12). Den maksimale Cmax og AUC0-24 var under den gennemsnitlige Cmax på ca. 76 mcg/ml og AUC0-24 af 154 mcg*HR/ml observeret for intravenøs administration af amikacinsulfat til injektion ved den godkendte dosering af 15 mg/kg en gang dagligt hos raske voksne.
Absorption
Arikayce's biotilgængelighed forventes at variere primært fra individuelle forskelle i forstøvereffektivitet og luftvejspatologi.
Fordeling
Proteinbindingen af amikacin i serum er ≤ 10%.
Eliminering
Efter inhalation af Arikayce hos Mac-patienter varierede det tilsyneladende serumhalviteve af amikacin fra ca. 5,9 til 19,5 timer.
Metabolisme
Amikacin gennemgår ikke mærkbar stofskifte.
Udskillelse
Systemisk absorberet amikacin efter Arikayce -administration elimineres hovedsageligt via glomerulær filtrering. I gennemsnit 7,42% (i området fra 0,72 til 22,60%; n = 14) af den samlede arikayce -dosis blev udskilt i urin som uændret lægemiddel sammenlignet med 94% efter intravenøs indgivelse af amikacinsulfat til injektion. Uabsorberet amikacin efter indånding af arikayce elimineres sandsynligvis primært ved cellulær omsætning og forventning.
Lægemiddelinteraktionsundersøgelser
Der er ikke udført nogen kliniske lægemiddelinteraktionsundersøgelser med Arikayce [se Lægemiddelinteraktioner ].
Mikrobiologi
Handlingsmekanisme
Amikacin er et polykationisk semisyntetisk bakteriedræbende aminoglycosid. Amikacin kommer ind i bakteriecellen ved at binde til negativt ladede komponenter i bakteriecellevæggen, der forstyrrer den samlede arkitektur af cellevæggen. Den primære virkningsmekanisme er forstyrrelse og inhibering af proteinsyntese i målbakterierne ved binding til 30S ribosomal underenhed.
Modstand
Mekanismen for resistens over for amikacin i mycobacteria er blevet knyttet til mutationer i RRS -genet fra 16S rRNA. I kliniske forsøg blev MAC -isolater, der udvikler en amikacin -mikrofon på> 64 mcg/ml, efter at baseline blev observeret i en højere andel af forsøgspersoner behandlet med Arikayce [se Kliniske studier ].
Interaktion med andre antimikrobielle stoffer
Der har været ingen In vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Dyretoksikologi Andor farmakologi
For at give information om kronisk dosering af Arikayce til en anden dyreart blev der udført en 9-måneders inhalationstoksikologiundersøgelse hos hunde. Skumiske alveolære makrofager forbundet med clearance af det inhalerede produkt var til stede ved dosisrelateret forekomst og sværhedsgrad, men de var ikke forbundet med inflammationsvævshyperplasi eller tilstedeværelsen af preneoplastiske eller neoplastiske ændringer. Hunde blev udsat for Arikayce i op til 90 minutter pr. Dag med inhalerede amikacin -doser på ca. 5 10 og 30 mg/kg/dag.
Kliniske studier
Forsøg 1 (NCT Mycobacterium avium Kompleks (MAC) lungesygdom som bekræftet af mindst 2 sputumkulturresultater. Patienter blev betragtet som ildfast MAC -lungesygdom, hvis de ikke opnåede negative sputumkulturer efter en minimumsvarighed på 6 på hinanden følgende måneder med baggrundsregime -terapi, der enten var vedvarende eller stoppede ikke mere end 12 måneder før screeningsbesøget. Patienter blev randomiseret til enten Arikayce plus et baggrundsregime eller baggrundsregime alene. Surrogatendepunktet til vurdering af effektiviteten var baseret på opnåelse af kulturkonvertering (3 på hinanden følgende månedlige negative sputumkulturer) inden måned 6. Datoen for konvertering blev defineret som datoen for den første af de 3 negative månedlige kulturer, der måtte opnås i måned 4 for at imødekomme slutpunktet med måned 6. Patienter, der opnåede kulturkonvertering i måned 6 blev fortsat på undersøgelse af undersøgelse (arikayc Randomisering) i alt 12 måneder efter den første negative sputumkultur.
I alt 336 patienter blev randomiseret (Arikayce plus baggrundsregime N = 224; baggrundsregime alene n = 112) (ITT -population) med en gennemsnitlig alder på 64,7 år, og der var en højere procentdel af kvinder (NULL,3%) end mænd (NULL,7%) i undersøgelsen. På tidspunktet for tilmelding af de 336 forsøgspersoner i ITT-befolkningen var 302 (NULL,9%) enten i retningslinjebaseret regime for MAC eller OFF-retningslinjebaseret terapi for MAC i mindre end 3 måneder, mens 34 (NULL,1%) var ude af behandling i 3 til 12 måneder før tilmeldingen. Hos screening blev patienter stratificeret af rygestatus (nuværende ryger eller ej) og af om patienter var på behandling eller slukket behandling i mindst 3 måneder. De fleste patienter ved screening var ikke nuværende rygere (NULL,3%) og havde underliggende bronchiectasis (NULL,5%). Hos baseline var 329 patienter på et multidrug baggrundsregime, der omfattede et makrolid (NULL,3%) en rifamycin (NULL,3%) eller ethambutol (NULL,4%). Samlet set modtog 55,6% af forsøgspersonerne et tredobbelt medikamentregime bestående af et makrolid A rifamycin og ethambutol.
Andelen af patienter, der opnår kulturomdannelse (3 på hinanden følgende månedlige negative sputumkulturer) i måned 6 var signifikant (P <0.0001) greater feller Arikayce plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Arikayce plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 og sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media eller no mellere than 2 consecutive positive cultures on liquid media following culture conversion) feller up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Arikayce plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Kumulativ andel af emner, der opnår kulturkonvertering vist i den første måned med konverteringsintention til behandling (ITT) befolkning
 |
I forsøg 1 23/224 (NULL,3%) af patienterne havde MAC -isolater, der udviklede MIC på> 64 mcg/ml, mens de fik behandling med Arikayce. I baggrundsregimen alene havde ARM 4/112 (NULL,6%) af patienterne MAC -isolater, der udviklede amikacin -mikrofon på> 64 mcg/ml.
Yderligere slutpunkter til vurdering af den kliniske fordel ved Arikayce for eksempel ændrer sig fra baseline i seks minutters gangtestafstand, og Saint George's luftvejsspørgeskema demonstrerede ikke klinisk fordel i måned 6.
Patientinformation til Arikayce
Arikayce
(Ar 'i kase)
Begrænset befolkning
(Amikacin liposomindåndingssuspension) til oral inhalationsanvendelse
Vigtigt: Kun til oral inhalation.
Hvad er de vigtigste oplysninger, jeg skal vide om Arikayce?
Arikayce can cause serious side effects including:
- Allergisk betændelse i lungerne: Disse luftvejsproblemer kan være symptomer på allergisk betændelse i lungerne og kommer ofte med:
- feber
- hvæsende
- hosteing
- åndenød
- Hurtig vejrtrækning
- hosteing up of blood (hemoptysis): Hosteing up blood is a serious og common side effect of Arikayce.
- Alvorlige åndedrætsproblemer: Alvorlige åndedrætsproblemer kan være symptomer på bronchospasme. Bronchospasme er en alvorlig og almindelig bivirkning af Arikayce. Bronchospasmesymptomer inkluderer:
- åndenød
- vanskelig eller arbejdet vejrtrækning
- hvæsende
- hosteing eller brysttæthed
- Forværring af kronisk obstruktiv lungesygdom (KOL): Dette er en alvorlig og almindelig bivirkning af Arikayce.
- Alvorlige allergiske reaktioner: Alvorlige allergiske reaktioner, der kan føre til døden, er sket med mennesker, der tager Arikayce. Stop med at tage Arikayce med det samme og få nødmedicinsk hjælp, hvis du har nogen af følgende symptomer på en alvorlig allergisk reaktion:
- elveblest
- Støjende højhøjde
- Hurtig pasende vejrtrækning (Stridor)
- kløe
- hoste
- Føler dig lys
- rødme eller rødme af
- kvalme
- Føles svag huden (skylning)
- hævede læber tunge eller
- opkast
- Tab af kontrol med tarmene i halsen eller blæren (inkontinens)
- problemer med at trække vejret eller
- diarre
- svimmelhed hvæsende
- åndenød
- Føl kramper i dit maveområde
Mens brug af Arikayce kan disse bivirkninger blive alvorlige nok til, at der er behov for behandling på et hospital.
Ring til din sundhedsudbyder eller få medicinsk hjælp med det samme, hvis Du har nogen af disse alvorlige bivirkninger, mens du tager Arikayce. Din sundhedsudbyder kan bede dig om at stoppe med at bruge Arikayce i en kort periode eller helt stoppe med at bruge Arikayce.
Hvad er Arikayce?
Arikayce is a prescription medicine used to treat adults with refractellery (difficult to treat) Mycobacterium avium Kompleks (MAC) lungesygdom som en del af en kombination af antibakteriel lægemiddelbehandlingsplan (regime).
Det vides ikke, om Arikayce er sikker og effektiv hos børn yngre end 18 år. Dette produkt blev godkendt af FDA ved hjælp af den begrænsede befolkningsvej.
Dette betyder, at FDA har godkendt dette lægemiddel til en begrænset og specifik patientpopulation, og undersøgelser af lægemidlet har muligvis kun besvaret fokuserede spørgsmål om dets sikkerhed og effektivitet.
Brug ikke Arikayce, hvis du:
- er allergiske over for ethvert aminoglycosid eller nogen af ingredienserne i Arikayce. Se Hvad er ingredienserne i Arikayce? I slutningen af denne indlægsseddel til en komplet liste over ingredienser i Arikayce.
Før du bruger Arikayce, fortæl din sundhedsudbyder om alle dine medicinske tilstande, herunder hvis du:
- har astma kronisk obstruktiv lungesygdom (KOLS) åndenød eller vejrtrækning (bronchospasme).
- har fået at vide, at du har dårlig lungefunktion.
- Har eller har haft høringsproblemer (inklusive lyde i dine ører, såsom ringning eller susende) høretab, eller din mor har haft høringsproblemer efter at have taget et aminoglycosid.
- har fået at vide, at du har visse genvarianter (en ændring i genet) relateret til hørende abnormiteter, der er arvet fra din mor.
- Har svimmelhed eller fornemmelse af rummet, der drejer.
- har nyreproblemer.
- har neuromuskulær sygdom, såsom myasthenia gravis.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- er amning eller planlægger at amme. Det vides ikke, om medicinen i Arikayce passerer ind i din modermælk, og om det kan skade din baby. Tal med din sundhedsudbyder om den bedste måde at fodre din baby under behandling med Arikayce.
Fortæl din sundhedsudbyder om alle de medicin, du tager, inklusive Receptpligtig medicin og medicinske medicin og urtetilskud.
Hvordan skal jeg bruge Arikayce?
- Læs de trin-for-trin-instruktioner til brug af Arikayce i slutningen af medicinvejledningen og de fulde instruktioner til brug, der er angivet i dit kit. Producentens brugsinstruktioner giver komplette oplysninger om, hvordan man sammensætter (samler) Forbered brug rent og desinficerer din Lamira ® Nebulizer -system.
- Gør ikke Brug Arikayce, medmindre du forstår de angivne anvisninger. Hvis du har spørgsmål, skal du tale med din sundhedsudbyder eller ringe til Arikares support på 1-833-Arikare (1-833-274-5273).
- Brug Arikayce nøjagtigt, som din sundhedsudbyder fortæller dig at bruge den. Brug ikke Arikayce oftere end foreskrevet til dig.
- Brug kun Arikayce med Lamira Nebulizer -systemet.
- Inhaler hver daglig dosis af Arikayce 1 gang hver dag gennem Lamira Nebulizer -håndsæt. Brug ikke mere end 1 hætteglas af Arikayce på en dag.
- Gør ikke use Arikayce after the expiration date on the vial. If you fellerget to take your daily dose of Arikayce take your next dose at your usual time the next day.
- Gør ikke Dobbelt dosis for at kompensere for den ubesvarede dosis.
- Gør ikke Stop med at bruge Arikayce eller andre medicin til at behandle din Mac Lung Disease, medmindre du får besked om at gøre det af din sundhedsudbyder.
- Hvis du bruger for meget Arikayce, skal du ringe til din sundhedsudbyder eller gå til den nærmeste alarmrum med det samme.
Hvad er de mulige bivirkninger af Arikayce?
Arikayce may cause serious side effects including:
- Se hvad er de vigtigste oplysninger, jeg skal vide om Arikayce?
- høretab eller ringning i ørerne (ototoksicitet) . Ototoksicitet er en alvorlig og almindelig bivirkning af Arikayce. Fortæl din sundhedsudbyder med det samme, hvis du har høretab, eller du hører lyde i dine ører, såsom at ringe eller susende. Fortæl din sundhedsudbyder, hvis du begynder at have problemer med balance eller svimmelhed (Vertigo).
- Forværring af nyreproblemer (nefrotoksicitet). Arikayce is in a class of medicines which may cause wellersening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are wellerking during your treatment with Arikayce.
- Forværring af muskelsvaghed (neuromuskulær blokade). Arikayce is in a class of medicines which can cause muscle svaghed to get wellerse in people who already have problems with muscle svaghed (myasthenia gravis).
De mest almindelige bivirkninger af Arikayce inkluderer:
- Ændringer i din stemme og
- ondt i halsen
- Muskelsmerter heshed (dysfonia)
- diarre
- kvalme
- træthed (træthed)
- feber
- opkast
- hovedpine
- nedsat vægt
- øget sputum
- udslæt
- Bryst ubehag
- hoste during eller after a dose of Arikayce especially in the first month after starting treatment.
Dette er ikke alle de mulige bivirkninger af Arikayce.
bedste hoteller i paris
Ring til din læge eller apotek for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088
Hvordan skal jeg opbevare Arikayce?
- Opbevar Arikayce Vials kølet mellem 36 ° F til 46 ° C (2 ° C (2 ° C) indtil udløbsdatoen på hætteglasset. Frys ikke.
- Efter at Arikayce er blevet opbevaret i køleskabet, skal enhver ubrugt medicin kastes væk (bortskaffes) efter udløbsdatoen på hætteglasset.
- Opbevar Arikayce hætteglas ved stuetemperatur mellem 68 ° F til 77 ° C (20 ° C til 25 ° C) i op til 4 uger
- Efter at Arikayce er blevet opbevaret ved stuetemperatur, skal enhver ubrugt medicin kastes væk (bortskaffes) i slutningen af 4 uger.
- Brug et åbnet Arikayce -hætteglas med det samme.
- Kast Arikayce Vial med det samme efter brug.
Hold Arikayce og alle medicin uden for børns rækkevidde.
Generel information om sikker og effektiv brug af Arikayce
Medicin er undertiden ordineret til andre formål end dem, der er anført i en medicinguide. Brug ikke Arikayce til en betingelse, som den ikke blev ordineret til. Giv ikke Arikayce til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem. Du kan bede din farmaceut eller sundhedsudbyder om information om Arikayce, der er skrevet til sundhedsfagfolk.
Hvad er ingredienserne i Arikayce?
Aktiv ingrediens: amikacin sulfat
Inaktive ingredienser: Dipalmitoylphosphatidylcholin (DPPC) kolesterolnatriumchloridnatriumhydroxid (til pH -justering) og vand til injektion
Denne medicinguide er godkendt af U.S. Food and Drug Administration.
Brug til brug
Arikayce ®
Begrænset befolkning
(Amikacin liposomindåndingssuspension) til oral inhalationsanvendelse
Lamira ®
Nebulizer -system
Før du bruger dit Lamira Nebulizer -system, skal du være sikker på, at du læser og forstår de detaljerede oplysninger i de fulde instruktioner til brug, der følger med Lamira Nebulizer -systemet. Dette vil give mere komplette oplysninger om, hvordan man sammensætter (samler) Forbered brug Rent og desinficerer dit Lamira Nebulizer -system. Hvis du ikke forstår nogen del af instruktionerne Kontakt Arikares support på 1-833-Arikare (1-833-274-5273) Før du bruger Lamira Nebulizer -systemet.
Saml din Arikayce Medicine. Arikayce 28-dages sæt indeholder:
- 1 Arikayce Quick Start Guide
- 1 Instruktioner til brugsindsats
- 1 Fuld ordinerende informationsindsats
- 1 Lamira Nebulizer -håndsæt
- 4 Lamira aerosolhoveder (1 i hver ugentlig boks)
- 28 hætteglas (1 hætteglas hver dag) af Arikayce (7 i hver ugentlig boks)
Kontroller, at du har alle de nødvendige dele til dit Lamira Nebulizer -system:
- Bære sag
- Forbindelsestra
- Controller
- A/C strømforsyning
- AA -batterier
 |
Reserve Lamira Nebulizer -håndsæt:
- Medicinhætte og forsegling
- Medicinreservoir
- Blå ventil
- Aerosolkammer
- Mundstykket
- Spar Aerosol Head
 |
Du har også brug for følgende forsyninger, der ikke kommer i dit Arikayce 28-dages kit, der hjælper dig med at pleje dit Lamira Nebulizer-system:
- Klar flydende sæbe til rengøring af håndsættet og aerosolhovedet
- Destilleret vand til desinfektion af håndsættet og aerosolhoved
Vælg din strømforsyning og gør det klar.
en. 4 AA -batterier
 |
b. A/C strømforsyning
- Sæt AC -strømforsyningen i controlleren.
- Sæt AC -strømforsyningen i stikkontakten.
Gør ikke insert the A/C Power into thefront of the Controller.
 |
Rengøring og desinfektion
Før først skal du skylle rent og desinficere dit håndsæt og aerosolhoved. Gå fremad skyl rent og desinficerer håndsættet inklusive aerosolhovedet efter hver brug.
Når du modtager dit håndsæt og aerosolhoved, vil de ikke være sterile. Rengøring og desinficering af dit håndsæt og aerosolhoved er vigtigt for at reducere risikoen for infektionssygdom og forurening.
- Rengøring af håndsættet og aerosolhovedet påmindelse: Før første brug skyl og rengør håndsættet og aerosolhovedet. Gå fremad skyl og rengør håndsættet inklusive aerosolhovedet lige efter hver brug.
Brug kun almindelige tørre papertowels eller wipes. Gør ikke use towels eller wipes that have any chemicals added to them such as alcohol lotion eller baby wipes.
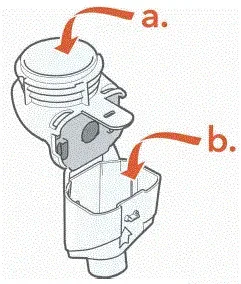
Vær forsigtig med ikke at skade delene. Tør ikke aerosolhoved.
Kast papirhåndklæder væk ved at bortskaffe papirkurven med fast affald.

- Tag fra hinanden (adskill) håndsættet til rengøring
- Tør forsigtigt eventuelle dråber væk af medicin fra medicinreservoiret (a) aerosolkammer (b) og mundstykket (c) før skylning for at reducere antibiotika tilsat vandsystemer.
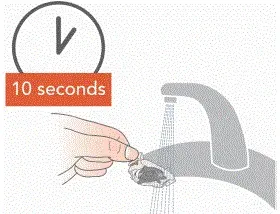
- Skyl hver af de dele, der er under varmt løbende ledningsvand til 10 sekunder. Skyl aerosolhovedet til 10 sekunder på hver side.
- Rengør alle håndsæt dele ved at tilføje et par dråber klar flydende opvaskesæbe og varmt ledningsvand til et rent karbad eller skål. Dæk håndsættets dele i det varme sæbevand og blød i 5 minutter ryster dem med jævne mellemrum. Skyl dem derefter grundigt under varmt løbende ledningsvand.
- Desinficering af håndsættet og aerosolhovedet før første brug påmindelse: Desinficerer håndsættet og aerosolhovedet inden første brug.

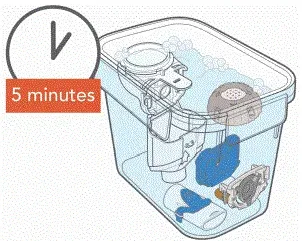
- Sørg for, at dit håndsæt og aerosolhoved er rent, før du desinficerer.
- Sørg for, at gryden har destilleret vand nok til at dække alle håndsætdele, inklusive aerosolhovedet.
- Opvarm vandet i kog i en ren gryde.
- Placer håndsættets dele inklusive aerosolhovedet i det kogende vand.
- Kog for en fuld 5 minutter . Bemærk: Det kan være nyttigt at bruge en timer.
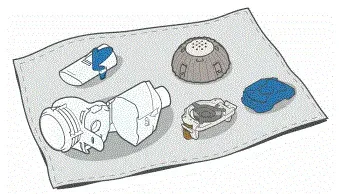
- Lufttør på en fnugfri håndklæde. Når det er fuldt tørt indpak delene i et fnugfrit håndklæde til opbevaring. Du kan sammensætte dem igen lige før du tager din næste behandling.
Samling af dit håndsæt
Trin 1: Vask hænderne med sæbe og vand og dry them well.
 |
Trin 2: Indsæt den blå ventil.
Åbn håndsættet ved forsigtigt at trække op på fanen af medicinreservoiret.
Indsæt den blå ventil, så den hviler på toppen af aerosolkammeret med de 2 ventilsklapper, der vender ned (ventilklapper, der ikke er bøjet).
 |
Aer Osol C HAMBER VAL VE FLAPS VALVE FLAP BLUE VALVE
Trin 3: Indsæt aerosolhovedet.
Tag fat i aerosolhovedet ved de 2 fleksible plastfaner på hver side. Sørg for, at teksten Lamira ® vender mod dig og er øverst på aerosolhovedet.
Klem de 2 fleksible plastfaner sammen, mens du indsætter aerosolhovedet i medicinreservoiret.
Luk håndsættet, når du er færdig (ingen huller langs den blå ventilkant).
 |
Gør ikke touch the silver part of theAerosol Head at any time.
Efter at aerosolhovedet er blevet brugt 7 gange kastet væk (bortskaffes) og udskiftes med en ny oneduring rengøringsprocessen. Lamira -håndsæt skal bruges i 28 dage.
 |
Trin 4: Fastgør mundstykket Toyour -håndsæt med den blå flapfacing op.
 |
Trin 5: Til sidst fastgør håndsættet til controlleren.
en. Fastgør forbindelsesledningen til håndsættet. A1. Line op i bunden af stikket med bunden af håndsættet.
A2. Skub opad mod håndsættet, indtil du hører brikkerne snap sammen. b. Tilslut forbindelsesledningen til controlleren.
 |
At tage Arikayce
Din Arikayce skal være ved stuetemperatur inden brug for at sikre dig, at dit Lamira Nebulizer -system fungerer korrekt. Gør ikke use other medicines in your Hogset.
Bring Arikayce til stuetemperatur ved at fjerne den fra køleskabet mindst 45 minutter Før brug. Gør ikke use if your Arikayce has been frozen.
Trin 1: Gør din Arikayce klar.
- Placer håndsættet på en ren flad stabil overflade.
- Ryst Arikayce -hætteglasset i mindst 10 til 15 sekunder Og indtil medicinen ser den samme igennem og godt blandet.
 |
Hvordan man åbner Arikayce hætteglas
 |
 |
 |
 |
- Løft den orange hætte fra hætteglasset.
- Grib metalringen Oven på hætteglasset og træk det forsigtigt ned, indtil 1 side går væk fra hætteglasset, men trækker ikke fanen helt væk.
- Træk metalbåndet Fra omkring hætteglaset i en cirkulær bevægelse, indtil den kommer helt ud.
- Fjern forsigtigt gummiproppen.
en. Åbn hætteglasset, og hæld Arikayce i medicinreservoiret.
b. Fastgør medicinhætten.
 |
Trin 2: Sid i en afslappet lodret position.
- Tryk og hold nede på tænd/sluk -knappen i et par sekunder for at tænde Lamira.
- Mist begynder at flyde.
 |
Trin 3: Indsæt mundstykket (men dæk ikke den blå klap) og tag langsomt dybe indåndinger.
- Træk derefter normalt ind og ud gennem mundstykket, indtil din behandling er afsluttet.
- Behandlingen skal tage ca. 14 minutter, men kan tage op til 20 minutter.
Sørg for at holde håndsætniveauet under hele behandlingen.
 |
Trin 4: Kontroller, at din behandling er afsluttet.
- Lamira vil bippe 2 gange.
- Et checkmark vises kort på skærmen.
- Controlleren lukkes automatisk.
- Fjern medicinhætten og Kontroller medicinreservoiret for at sikre sig, at ikke mere end et par dråber Arikayce er tilbage. Hvis Arikayce forbliver, skal du udskifte medicinhætten Tryk på knappen ON/OFF og komplet din dosis.
 |
For eventuelle problemer, du måtte have med dit Lamira Nebulizer -system, se afsnit J -frekvens stillede spørgsmål og afsnit K -nedbrydning af de fulde instruktioner til brug, der følger med din medicin.
Rengøring af dit Lamira -håndsæt og aerosolhoved efter brug
- Skyl rent og desinficeret håndsæt med det samme efter hver brug for at reducere infektionssygdom og forurening.
- Desinficerer håndsættet og aerosolhoved efter hver brug.
- Se rengøring og desinfektion i begyndelsen af instruktionerne til brug til, hvordan man korrekt rengør og desinficerer dit håndsæt og aerosolhoved.
Denne brugsanvisning er godkendt af U.S. Food and Drug Administration.






