Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
Antibiotika, LincosamidCleocin IV
Resume af lægemiddeloversigt
Hvad er cleocin?
Cleocin (clindamycin) er et antibiotikum, der anvendes til behandling af alvorlige infektioner forårsaget af modtagelige anaerobe bakterier. Cleocin fås i generisk form.
Hvad er bivirkninger af cleocin?
Cleocin IV
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- Vedvarende diarré
- mavesmerter
- Kramper
- blod eller slim i din afføring
- Smerter eller hævelse på injektionsstedet
- Mørk urin
- Gulning af huden eller øjnene (gulsot)
- vedvarende kvalme eller opkast
- Ændring i mængden af urin
- let blå mærker eller blå mærker
- ledssmerter
- feber
- vedvarende ondt i halsen
- Hurtig langsom eller uregelmæssig hjerteslag
- besvime og
- Alvorlig svimmelhed
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Bivirkninger af cleocin inkluderer:
Har Ultram Aprin i det
- mavesmerter
- Pseudomembranøs colitis
- esophagitis
- kvalme
- opkast
- diarre
- Ubehagelig eller metallisk smag i munden (hvis cleocin injiceres i en vene)
- Smerter og hævelse på injektionsstedet (hvis cleocin injiceres i en muskel)
- Overfølsomhedsreaktioner (udslæt og nældefeber)
- kløe
- vaginal infektion og
- Gulning af hud og øjne (gulsot).
Fortæl din læge, hvis du har alvorlige bivirkninger af cleocin inklusive:
- Smerter eller hævelse på injektionsstedet (hvis dette stof injiceres i en vene)
- Mørk urin
- gulterende øjne eller hud
- vedvarende kvalme eller opkast
- en ændring i mængden af urin
- let blå mærker eller blødning
- Smerter i flere led
- Nye tegn på infektion (f.eks. Feber vedvarende ondt i halsen)
- Hurtig/langsom/uregelmæssig hjerteslag eller
- besvimende.
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; og pludselig svimmelhed letthed eller udlevering;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til cleocin
Den anbefalede dosis cleocin for voksne er 150-450 mg oralt hver 6. time eller intravenøse doser på 600-2700 mg dagligt i 2-4 opdelte doser.
Hvilke stoffer stoffer eller kosttilskud interagerer med cleocin?
Cleocin kan interagere med andre neuromuskulære blokerende midler erythromycin og hormonel fødselskontrol. Fortæl din læge alle medicin og kosttilskud, du bruger.
Cleocin under graviditet og amning
Cleocin er ikke blevet evalueret tilstrækkeligt hos gravide kvinder. Cleocin skal kun bruges under graviditet, hvis det helt klart er nødvendigt. Cleocin passerer ind i modermælk og kunne have uønskede effekter på et ammende spædbarn. Kontakt din læge inden amning.
Yderligere oplysninger
Vores cleocin bivirkninger Drug Center giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Dosering
- Bivirkninger
- Lægemiddelinteraktioner
- Advarsler
- Forholdsregler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
ADVARSEL
C Lostridium hårdt -Associeret diarré (CDAD) er rapporteret ved anvendelse af næsten alle antibakterielle midler, herunder cleocinphosphat og kan variere i sværhedsgrad fra mild diarré til dødelig colitis. Behandling med antibakterielle midler ændrer den normale flora i tyktarmen, der fører til overvækst af C. vanskelig .
Fordi cleocin -phosphatterapi har været forbundet med svær colitis, som kan ende dødeligt, skal det reserveres til alvorlige infektioner, hvor mindre giftige antimikrobielle stoffer er upassende som beskrevet i afsnittet Indikationer og anvendelse. Det bør ikke bruges til patienter med ikke -bakterielle infektioner, såsom de fleste øvre luftvejsinfektioner. C. vanskelig Producerer toksiner A og B, der bidrager til udviklingen af CDAD. Hypertoxinproducerende stammer af C. vanskelig Årsag øget sygelighed og dødelighed, da disse infektioner kan være ildfaste over for antimikrobiel terapi og kan kræve kolektomi. CDAD skal overvejes hos alle patienter, der præsenterer med diarré efter antibiotisk brug. Omhyggelig medicinsk historie er nødvendig, da CDAD er rapporteret at forekomme over to måneder efter administration af antibakterielle midler.
Hvis CDAD er mistænkt eller bekræftes ved løbende antibiotikamisbrug, der ikke er rettet mod C. vanskelig kan være nødvendigt at afbryde. Passende væske- og elektrolytstyringsproteintilskud Antibiotikabehandling af C. vanskelig og kirurgisk evaluering bør indføres som klinisk indikeret.
Beskrivelse for cleocin i.v.
Cleocin -phosphat -steril opløsning i hætteglas indeholder clindamycin -phosphat Et vandopløseligt ester af clindamycin og fosforsyre. Hver ML indeholder ækvivalenten af 150 mg clindamycin 0,5 mg disodiumdetat og 9,45 mg benzylalkohol tilsat som konserveringsmiddel i hver ML. Clindamycin er et semisyntetisk antibiotikum produceret af en 7 (S) -chlor-substitution af 7 (R) -hydroxylgruppen af moderforbindelsen Lincomycin.
Det kemiske navn på clindamycin-fosfat er l- retning -en-d- Galacto -Octopyranosidmethyl-7-chlor-678-trideoxy-6-[[(1-methyl-4-propyl-2-pyrrolidinyl) carbonyl] amino] -1-thio- 2- (dihydrogenphosphat) (2S- Trans )-.
Den molekylære formel er C 18 H 34 Spise 2 0 8 PS og molekylvægten er 504,96.
Den strukturelle formel er repræsenteret nedenfor:
 |
Cleocin-phosphat i tilføjelseshætteglasset er beregnet til intravenøs brug først efter yderligere fortynding med passende volumen af tilføjelsesbasisforsyningsbasisopløsning (se Rutevejledning til brug ).
Cleocin -phosphat IV -opløsning i galakseplastbeholderen til intravenøs anvendelse er sammensat af clindamycin -phosphat svarende til 300 600 og 900 mg clindamycin forblandet med 5% dextrose som en steril opløsning. Disodiumdetat er tilsat i en koncentration på 0,04 mg/ml. PH er blevet justeret med natriumhydroxid og/eller saltsyre.
Plastbeholderen er fremstillet af et specielt designet flerlags plast PL 2501. Løsninger i kontakt med plastbeholderen kan udvask visse af dens kemiske komponenter i meget små mængder inden for udløbsperioden. Plastens egnethed er bekræftet i test i dyr i henhold til USP -biologiske tests for plastbeholdere såvel som af vævskulturstoksicitetsundersøgelser.
Anvendelser til cleocin i.v.
Cleocin -phosphatprodukter er indikeret i behandlingen af alvorlige infektioner forårsaget af modtagelige anaerobe bakterier.
Cleocin -phosphatprodukter er også indikeret i behandlingen af alvorlige infektioner på grund af modtagelige stammer af streptococci pneumococci og staphylococci. Dets anvendelse bør reserveres til penicillin-allergiske patienter eller andre patienter, for hvilke en penicillin dom er upassende. På grund af risikoen for antibiotikasassocieret pseudomembranøs colitis som beskrevet i Bokset advarsel Før valg af clindamycin skal lægen overveje infektionens art og egnetheden af mindre giftige alternativer (f.eks. Erythromycin).
Bakteriologiske undersøgelser skal udføres for at bestemme de årsagsorganismer og deres modtagelighed for clindamycin.
Indikerede kirurgiske procedurer skal udføres i forbindelse med antibiotikabehandling.
Cleocin -phosphat er indikeret i behandlingen af alvorlige infektioner forårsaget af modtagelige stammer af de udpegede organismer under nedenstående forhold:
Infektioner med lavere luftvejsinfektioner inklusive lungebetændelse empyema og lungeabscess forårsaget af anaerober Streptococcus pneumoniae Andre streptokokker (undtagen E. faecalis ) og Staphylococcus aureus.
Infektioner i hud og hudstruktur forårsaget af Streptococcus pyogenes Staphylococcus aureus og anaerobes.
Gynækologiske infektioner inklusive endometritis nongonococcal tubo-ovarian abscess bækkencellulitis og postkirurgisk vaginal manchet infektion forårsaget af modtagelige anaerober.
Intra-abdominale infektioner inklusive peritonitis og intra-abdominal abscess forårsaget af modtagelige anaerobe organismer.
Septicæmi forårsaget af Staphylococcus aureus streptococci (undtagen Enterococcus faecalis ) og susceptible anaerobes.
Knogler og ledinfektioner inklusive akut hæmatogen osteomyelitis forårsaget af Staphylococcus aureus og som supplerende terapi i den kirurgiske behandling af kroniske knogler og ledinfektioner på grund af modtagelige organismer.
For at reducere udviklingen af lægemiddelresistente bakterier og opretholde effektiviteten af cleocinphosphat og andre antibakterielle lægemidler skal cleocinphosphat kun anvendes til behandling eller forhindring af infektioner, der er bevist eller stærkt mistænkt for at være forårsaget af modtagelige bakterier. Når information om kultur og følsomhed er tilgængelige, skal de overvejes ved valg eller ændring af antibakteriel terapi. I mangel af sådanne data kan lokal epidemiologi og følsomhedsmønstre bidrage til det empiriske udvalg af terapi.
Dosering til cleocin I.V.
Hvis diarré opstår under terapi, skal dette antibiotikum afbrydes (se Boksadvarsel ).
Clindamycin -phosphat IM -administration bør bruges ufortyndet.
5 dage i paris rejseplan
Clindamycin -fosfat IV -administration bør fortyndes (se Fortynding til IV -brug og IV -infusionshastigheder under).
Voksne
Parenteral (IM- eller IV-administration): Alvorlige infektioner på grund af aerob gram-positiv cocci og de mere modtagelige anaerober (ikke generelt inklusive Bacteroides fragilis peptococcus arter og Clostridium andre arter end Clostridium perfringens ):
600.1200 mg/dag i 2 3 eller 4 lige doser.
Mere alvorlige infektioner, især dem på grund af bevist eller mistænkt Bacteroides fragilis peptococcus arter eller Clostridium species bortset fra Clostridium perfringens:
1200.2700 mg/dag i 2 3 eller 4 lige doser.
For mere alvorlige infektioner kan disse doser muligvis øges. I livstruende situationer på grund af enten aerober eller anaerober kan disse doser øges. Doser på op til 4800 mg dagligt er blevet givet intravenøst til voksne. Se Fortynding til IV -brug og IV -infusionshastigheder Afsnit nedenfor.
Enkelt intramuskulære injektioner på mere end 600 mg anbefales ikke.
Alternativt kan lægemiddel administreres i form af en enkelt hurtig infusion af den første dosis efterfulgt af kontinuerlig IV -infusion som følger:
| At opretholde serum clindamycin -niveauer | Hurtig infusionshastighed | Vedligeholdelsesinfusionshastighed |
| Over 4 mcg/ml | 10 mg/min for 30 min | 0,75 mg/min |
| Over 5 mcg/ml | 15 mg/min for 30 min | 1,00 mg/min |
| Over 6 mcg/ml | 20 mg/min for 30 min | 1,25 mg/min |
Nyfødte (mindre end 1 måned)
15 til 20 mg/kg/dag i 3 til 4 lige doser. Den nedre dosering kan være tilstrækkelig til små prematurer.
Pædiatriske patienter 1 måned til 16 år
Parenteral (IM eller IV) Administration: 20 til 40 mg/kg/dag i 3 eller 4 lige doser. De højere doser ville blive brugt til mere alvorlige infektioner. Som et alternativ til dosering på kropsvægtbasis kan pædiatriske patienter doseres på grundlag af den firkantede meter kropsoverflade: 350 mg/m 2 /dag for alvorlige infektioner og 450 mg/m 2 /dag for mere alvorlige infektioner.
Parenteral terapi kan ændres til oral cleocin pediatricr ® Aromatiserede granuler (clindamycin palmitathydrochlorid) eller cleocin HCLR ® Kapsler (clindamycinhydrochlorid), når tilstanden garanterer og efter lægens skøn.
I tilfælde af ß-hemolytisk streptokokkinfektion bør behandling fortsættes i mindst 10 dage.
Fortynding til IV -brug og IV -infusionshastigheder: The concentration of clindamycin in diluent for infusion should not exceed 18 mg per mL. Infusion rates should not exceed 30 mg per minute. De sædvanlige infusionsfortyndinger og satser er som følger:
| Dosis | Fortyndingsmiddel | Tid |
| 300 mg | 50 ml | 10 min |
| 600 mg | 50 ml | 20 min |
| 900 mg | 50-100 ml | 30 min |
| 1200 mg | 100 ml | 40 min |
Administration af mere end 1200 mg i en enkelt 1-timers infusion anbefales ikke.
Parenterale lægemiddelprodukter skal inspiceres visuelt for partikler og misfarvning inden administration hver gang løsning og containertilladelse.
Fortynding og kompatibilitet
Fysiske og biologiske kompatibilitetsundersøgelser, der overvåges i 24 timer ved stuetemperatur, har ikke vist nogen inaktivering eller inkompatibilitet med brugen af cleocinphosphat -steril opløsning (clindamycinphosphat) i IV -opløsninger indeholdende natriumchloridglukose calcium eller kalium- og opløsninger indeholdende vitamin B -kompleks i koncentrationer, der normalt anvendes klinisk. Der er ikke påvist nogen inkompatibilitet med antibiotika cephalothin kanamycin gentamicin penicillin eller carbenicillin.
Følgende lægemidler er fysisk uforenelige med clindamycin -phosphat: ampicillin natrium phenytoin natrium barbiturater aminophyllin calciumgluconat og magnesiumsulfat.
Kompatibiliteten og varigheden af stabiliteten af lægemiddelblandinger vil variere afhængigt af koncentration og andre tilstande. For aktuelle oplysninger om kompatibiliteter af clindamycin -phosphat under specifikke forhold bedes du kontakte den medicinske og lægemiddelinformationsenhed Pharmacia
Fysisk-kemisk stabilitet af fortyndede opløsninger af cleocin-phosphat-stuetemperatur
6 9 og 12 mg/ml (svarende til clindamycinbase) i dextrose -injektion 5% natriumchloridinjektion 0,9% eller lactated ringersinjektion i glasflasker eller minibags demonstreret fysisk og kemisk stabilitet i mindst 16 dage ved 25 ° C. Også 18 mg/ml (svarende til clindamycinbase) i dextrose -injektion 5% i minibags demonstrerede fysisk og kemisk stabilitet i mindst 16 dage ved 25 ° C.
Køling
6 9 og 12 mg/ml (svarende til clindamycinbase) i dextrose -injektion 5% natriumchloridinjektion 0,9% eller lakterede ringereinjektion i glasflasker eller minibags demonstreret fysisk og kemisk stabilitet i mindst 32 dage ved 4 ° C.
VIGTIGT: Denne kemiske stabilitetsoplysning på ingen måde indikerer, at det ville være acceptabel praksis at bruge dette produkt godt efter forberedelsestiden. God professionel praksis antyder, at sammensatte blandinger skal administreres så hurtigt efter forberedelse som det er muligt.
Frossen
6 9 og 12 mg/ml (svarende til clindamycinbase) i dextrose -injektion 5% natriumchloridinjektion 0,9% eller lactated ringersinjektion i minibags demonstreret fysisk og kemisk stabilitet i mindst otte uger ved -10 ° C.
Frossen solutions should be Thawed at room temperature and not refrozen.
Kørselsvejledning til dispensering
Apotekbulkpakke
Ikke til direkte infusion
Apotekbulk -pakken er kun til brug i en apotek blandingstjeneste under en laminær flowhætte. Indtræden i hætteglasset skal foretages med en sterilt overførselssæt med lille diameter eller anden steril dispenseringsenhed med lille diameter og indhold, der er dispenseret i portioner ved hjælp af aseptisk teknik. Flere poster med en nål og sprøjte anbefales ikke. Efter indgang skal du bruge hele indholdet af hætteglasset straks. Enhver ubrugt del skal kasseres inden for 24 timer efter den første post.
Rutevejledning til brug
Cleocin Phosphate IV -opløsning i galakseplastbeholder
Forblandet cleocin -phosphat IV -opløsning er til intravenøs administration ved hjælp af sterilt udstyr. Kontroller for minutlækager inden brug ved at presse taske fast. Hvis der findes lækager, kasseres opløsning som sterilitet kan være nedsat. Tilsæt ikke supplerende medicin. Parenterale lægemiddelprodukter skal inspiceres visuelt for partikler og misfarvning inden administration hver gang løsning og containertilladelse. Brug ikke, medmindre opløsningen er klar, og tætningen er intakt.
Forsigtighed
Brug ikke plastbeholdere i serieforbindelser. En sådan anvendelse kan resultere i, at luftemboli på grund af resterende luft, der trækkes fra den primære beholder, før den administration af væsken fra den sekundære beholder er afsluttet.
Forberedelse til administration
- Suspend container fra eyelet support.
- Fjern beskytter fra udløbsporten i bunden af beholderen.
- Vedhæft administrationssæt. Se komplette retninger, der ledsages.
Fremstilling af cleocin-phosphat i tilføjelsessystemet- . For IV Brug kun. Cleocin -phosphat 300 mg 600 mg og 900 mg kan rekonstitueres i 50 ml (for 300 mg og 600 mg) eller 100 ml (for 900 mg) dextrose -injektion 5% eller natriumchloridinjektion 0,9% i tilsætnings -diluentbeholderen. Se separate instruktioner for Add-Vantage System.
Hvor leveret
Hver ml af Cleocin -phosphat Steril opløsning indeholder clindamycin -phosphat svarende til 150 mg clindamycin 0,5 mg disodiumdetat 9,45 mg benzylalkohol tilsat som konserveringsmiddel. Når det er nødvendigt, justeres pH med natriumhydroxid og/eller saltsyre. Cleocin -phosphat fås i de følgende pakker:
25-2 ml hætteglas NDC 0009-0870-26
25-4 ml hætteglas NDC 0009-0775-26
25-6 ml hætteglas NDC 0009-0902-18
5-60 ml apotek bulkpakke NDC 0009-0728-09
Cleocin -phosphat leveres i tilføjelseshætteglas som følger:
| NDC | Hætteglasstørrelse | Total clindamycin -phosphat/hætteglas |
| 0009-6582-01 | 25-2 ml hætteglas | 300 mg |
| 0009-3124-03 | 25-4 ml hætteglas | 600 mg |
| 0009-3447-03 | 25-6 ml hætteglas | 900 mg |
Opbevares ved kontrolleret stuetemperatur 20 ° til 25 ° C (68 ° til 77 ° F) [se USP].
Cleocin -phosphat IV Solution I galakseplastbeholdere er en steril opløsning af clindamycin -phosphat med 5% dextrose. Den enkelte dosis galakseplastbeholdere fås som følger:
24-300 mg/50 ml containere NDC 0009-3381-02
24-600 mg/50 ml containere NDC 0009-3375-02
24-900 mg/50 ml containere NDC 0009-3382-02
Eksponering af farmaceutiske produkter for varme bør minimeres. Det anbefales, at galakseplastbeholdere opbevares ved stuetemperatur (25 ° C). Undgå temperaturer over 30 ° C.
Distribueret af: Pfizer Pharmacia
Bivirkninger for Cleocin I.V.
Følgende reaktioner er rapporteret ved anvendelse af clindamycin.
Infektioner og angreb: Clostridium difficile colitis
Gastrointestinal: Antibiotikumassocieret colitis (se ADVARSELS ) Pseudomembranøs colitis abdominal smerte kvalme og opkast. Indtræden af pseudomembranøse colitis -symptomer kan forekomme under eller efter antibakteriel behandling (se ADVARSELS ). An unpleasant or metallic taste has been reported after intravenous administration of The higher doses of clindamycin phosphate.
Overfølsomhedsreaktioner: Makulopapulært udslæt og urticaria er blevet observeret under lægemiddelterapi. Generaliserede milde til moderat morbilliformlignende hududslæt er de hyppigst rapporteret af alle bivirkninger.
Alvorlige hudreaktioner såsom toksisk epidermal nekrolyse nogle med dødeligt resultat er rapporteret (se ADVARSELS ). Cases of Acute Generelized ExanThematous Pustulosis (AGEP) eryThema multiforme some resembling Stevens-Johnson syndrome have been associated wiTh clindamycin. Anaphylactic shock anaphylactic reaction and hypersensitivity have also been reported (se ADVARSELS ).
Hud og slimhinder: Pruritus vaginitis angioødem og sjældne tilfælde af eksfoliativ dermatitis er rapporteret (se Overfølsomhedsreaktioner ).
Lever: Gulsot og abnormiteter i leverfunktionstest er blevet observeret under clindamycin -terapi.
Nyre: Selvom der ikke er etableret noget direkte forhold mellem clindamycin til nyreskade, er nyredysfunktion, som det fremgår af azotæmi oliguri og/eller proteinuri, observeret.
Hæmatopoietisk: Forbigående neutropeni (leukopeni) og eosinophilia er rapporteret. Rapporter om agranulocytose og thrombocytopeni er blevet foretaget. Intet direkte etiologisk forhold til samtidig clindamycin -terapi kunne foretages i nogen af de foregående.
Immunsystem: Lægemiddelreaktion med eosinophilia og systemiske symptomer (kjole) tilfælde er rapporteret.
Lokale reaktioner: Injektionsstedets irritationssmerter Induration og steril abscess er rapporteret efter intramuskulær injektion og thrombophlebitis efter intravenøs infusion. Reaktioner kan minimeres eller undgås ved at give dybe intramuskulære injektioner og undgå langvarig anvendelse af indbyggede intravenøse katetre.
Muskuloskeletal: Der er rapporteret om polyarthritis.
Kardiovaskulær: Kardiopulmonal arrestation og hypotension er rapporteret efter for hurtig intravenøs administration (se Dosering og administration ).
Lægemiddelinteraktioner for Cleocin I.V.
Det har vist sig, at clindamycin har neuromuskulære blokeringsegenskaber, der kan forbedre virkningen af andre neuromuskulære blokeringsmidler. Derfor bør det bruges med forsigtighed hos patienter, der får sådanne midler.
moteller billigt
Clindamycin metaboliseres overvejende af CYP3A4 og i mindre grad af CYP3A5 til den vigtigste metabolit clindamycin-sulfoxid og mindre metabolit N-desmethylclindamycin. Derfor kan hæmmere af CYP3A4 og CYP3A5 øge plasmakoncentrationer af clindamycin og inducerere af disse isoenzymer kan reducere plasmakoncentrationer af clindamycin. I nærvær af stærke CYP3A4 -hæmmere overvåger for bivirkninger. I nærvær af stærke CYP3A4 -inducere såsom rifampicinmonitor for tab af effektivitet.
In vitro Undersøgelser indikerer, at clindamycin ikke hæmmer CYP1A2 CYP2C9 CYP2C19 CYP2E1 eller CYP2D6 og hæmmer kun moderat CYP3A4.
Antagonisme er blevet demonstreret mellem clindamycin og erythromycin In vitro . På grund af mulig klinisk betydning bør de to lægemidler ikke administreres samtidigt.
Advarsler for Cleocin I.V.
Se Boksadvarsel .
Clostridium Difficile Associated Diarrhea
Clostridium difficile Tilknyttet diarré (CDAD) er rapporteret ved anvendelse af næsten alle antibakterielle midler, herunder cleocinphosphat og kan variere i sværhedsgrad fra mild diarré til dødelig colitis. Behandling med antibakterielle midler ændrer den normale flora i tyktarmen, der fører til overvækst af C. vanskelig .
C. vanskelig Producerer toksiner A og B, der bidrager til udviklingen af CDAD. Hypertoxinproducerende stammer af C. vanskelig Årsag øget sygelighed og dødelighed, da disse infektioner kan være ildfaste over for antimikrobiel terapi og kan kræve kolektomi. CDAD skal overvejes hos alle patienter, der præsenterer med diarré efter antibiotisk brug. Omhyggelig medicinsk historie er nødvendig, da CDAD er rapporteret at forekomme over to måneder efter administration af antibakterielle midler.
Hvis CDAD er mistænkt eller bekræftes ved løbende antibiotikamisbrug, der ikke er rettet mod C. vanskelig kan være nødvendigt at afbryde. Passende væske- og elektrolytstyringsproteintilskud Antibiotikabehandling af C. vanskelig og kirurgisk evaluering bør indføres som klinisk indikeret.
Anafylaktiske og alvorlige overfølsomhedsreaktioner
Der er rapporteret om anafylaktisk chok og anafylaktiske reaktioner (se Bivirkninger ).
Alvorlige overfølsomhedsreaktioner, herunder alvorlige hudreaktioner, såsom toksisk epidermal nekrolyse (ti) lægemiddelreaktion med eosinophilia og systemiske symptomer (kjole) og Stevens-Johnson syndrom (SJS) Nogle med dødeligt resultat er rapporteret (se (se Bivirkninger ).
I tilfælde af en sådan anafylaktisk eller alvorlig overfølsomhedsreaktion ophører behandling permanent og indfører passende terapi.
Der bør foretages en omhyggelig undersøgelse af tidligere følsomheder over for medikamenter og andre allergener.
Benzylalkoholtoksicitet hos pædiatriske patienter (gispende syndrom)
Dette produkt indeholder benzylalkohol som konserveringsmiddel. Det konserveringsmiddel benzylalkohol har været forbundet med alvorlige bivirkninger, herunder GGASPING -syndrom og død hos pædiatriske patienter. Selvom normale terapeutiske doser af dette produkt normalt leverer mængder af benzylalkohol, der er væsentligt lavere end dem, der er rapporteret i forbindelse med asping -syndromet, er det ikke kendt, at det minimale beløb af benzylalkohol er, ved hvilken toksicitet kan forekomme.
Risikoen for benzylalkoholtoksicitet afhænger af den administrerede mængde og leveren og nyrernes kapacitet til at afgifte kemikaliet. For tidlige spædbørn med lav fødselsvægt kan være mere tilbøjelige til at udvikle toksicitet.
Brug i meningitis
Da clindamycin ikke diffunderer tilstrækkeligt ind i cerebrospinalvæsken, bør lægemidlet ikke bruges til behandling af meningitis.
Forholdsregler for Cleocin I.V.
Generel
Gennemgang af erfaring til dato antyder, at en undergruppe af ældre patienter med tilhørende svær sygdom kan tolerere diarré mindre godt. Når clindamycin er indikeret hos disse patienter, skal de overvåges omhyggeligt for ændring i tarmfrekvens.
Cleocin -phosphat products should be prescribed wiTh caution in individuals wiTh a history of gastrointestinal disease particularly colitis.
Cleocin -phosphat should be prescribed wiTh caution in atopic individuals.
Visse infektioner kan kræve snit og dræning eller andre indikerede kirurgiske procedurer ud over antibiotikabehandling.
Anvendelsen af cleocinphosphat kan resultere i overvækst af ikke-optagelige organismer-partikulært gær. Hvis superinfektioner forekommer, skal der træffes passende foranstaltninger som angivet af den kliniske situation.
Cleocin -phosphat should not be injected intravenously undiluted as a bolus but should be infused over at least 10-60 minutes as directed in The Dosering og administration afsnit.
Clindamycin -doseringsmodifikation er muligvis ikke nødvendig hos patienter med nyresygdom. Hos patienter med moderat til svær leversygdom er der fundet forlængelse af clindamycin-halveringstid. Imidlertid blev det postuleret fra undersøgelser, at når de blev givet hver otte timers ophobning, skulle sjældent forekomme. Derfor er doseringsmodifikation hos patienter med leversygdom muligvis ikke nødvendig. Imidlertid bør periodiske leverenzymbestemmelser foretages, når man behandler patienter med svær leversygdom.
Det er usandsynligt, at ordinering af cleocinphosphat i fravær af en påvist eller stærkt mistænkt bakterieinfektion eller en profylaktisk indikation giver fordel for patienten og øger risikoen for udviklingen af lægemiddelresistente bakterier.
Information til patienter
Patienter skal rådes om, at antibakterielle lægemidler inklusive cleocin -phosphat kun bør bruges til behandling af bakterieinfektioner. De behandler ikke virusinfektioner (f.eks. Koldkølelsen). Når cleocin -phosphat er ordineret til behandling af en bakterieinfektion, skal patienterne fortælles, at selv om det er almindeligt at føle sig bedre tidligt i løbet af terapien, skal medicinen tages nøjagtigt som anført. Spring over doser eller ikke gennemførelse af det fulde terapiforløb kan (1) mindske effektiviteten af den øjeblikkelige behandling og (2) øge sandsynligheden for, at bakterier vil udvikle resistens og ikke kan behandles med cleocinphosphat eller andre antibakterielle lægemidler i fremtiden.
Diarré er et almindeligt problem forårsaget af antibiotika, som normalt slutter, når antibiotikumet afbrydes. Undertiden efter start af behandling med antibiotika kan patienter udvikle vandige og blodige afføring (med eller uden mavekramper og feber), selv så sent som to eller flere måneder efter at have taget den sidste dosis af antibiotikumet. Hvis dette forekommer, skal patienter kontakte deres læge så hurtigt som muligt.
Laboratorieundersøgelser
Under langvarig terapi skal periodiske lever- og nyrefunktionstest og blodtællinger udføres.
Karcinogenese mutagenese nedskrivning af fertilitet
Langtidsundersøgelser hos dyr er ikke blevet udført med clindamycin for at evaluere kræftfremkaldende potentiale. Genotoksicitetstest, der blev udført, omfattede en rotte micronucleus -test og en Ames Salmonella -reversionstest. Begge test var negative.
Fertilitetsundersøgelser hos rotter behandlet oralt med op til 300 mg/kg/dag (ca. 1,1 gange den højest anbefalede voksne menneskelige dosis baseret på mg/m 2 ) afslørede ingen effekter på fertilitet eller parringsevne.
Graviditet
Teratogene effekter
I kliniske forsøg med gravide kvinder har den systemiske administration af clindamycin i løbet af anden og tredje trimestere ikke været forbundet med en øget hyppighed af medfødte abnormiteter.
Clindamycin skal kun bruges i løbet af den første trimester af graviditeten, hvis det er klart nødvendigt. Der er ingen tilstrækkelige og godt kontrollerede studier hos gravide kvinder i første trimester af graviditeten. Fordi dyreproduktionsundersøgelser ikke altid er forudsigelige for den menneskelige respons, skal dette lægemiddel kun bruges under graviditet, hvis det er klart nødvendigt.
Reproduktionsundersøgelser udført i rotter og mus ved hjælp af orale doser af clindamycin op til 600 mg/kg/dag (NULL,1 og 1,1 gange den højest anbefalede voksne menneskelige dosis baseret på mg/m 2 henholdsvis) eller subkutane doser af clindamycin op til 250 mg/kg/dag (NULL,9 og 0,5 gange den højest anbefalede voksne menneskelige dosis baseret på mg/m 2 henholdsvis) afslørede intet bevis for teratogenicitet.
Cleocin -phosphat Sterile Solution contains benzyl alcohol. Benzyl alcohol can cross The placenta. see ADVARSELS .
Sygeplejerske mødre
Det er rapporteret, at clindamycin vises i modermælk i området 0,7 til 3,8 mcg/ml ved doseringer på 150 mg oralt til 600 mg intravenøst. Clindamycin har potentialet til at forårsage bivirkninger på det ammede spædbarns gastrointestinale flora. Hvis oral eller intravenøs clindamycin er påkrævet af en sygeplejemor, er det ikke en grund til at afbryde amning, men et alternativt stof kan foretrækkes. Overvåg spædbarnet for mulige bivirkninger på mave-tarmfloraen, såsom diarré candidiasis (thrush bleudslæt) eller sjældent blod i afføringen, hvilket indikerer mulig antibiotikasassocieret colitis.
De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med mors kliniske behov for clindamycin og eventuelle bivirkninger på det ammede barn fra clindamycin eller fra den underliggende moderlige tilstand.
san diego hostel
Pædiatrisk brug
Når cleocin -phosphat -steril opløsning administreres til den pædiatriske population (fødsel til 16 år), er passende overvågning af organsystemfunktioner ønskeligt.
Brug hos nyfødte og spædbørn
Dette produkt indeholder benzylalkohol som konserveringsmiddel. Benzylalkohol har været forbundet med et dødeligt 'gispende syndrom' hos for tidlige spædbørn. se ADVARSELS .
Potentialet for den toksiske virkning i den pædiatriske population fra kemikalier, der kan udvaskes fra den enkelte dosis forblandet IV -præparat i plast, er ikke blevet evalueret. se ADVARSELS .
Geriatrisk brug
Kliniske undersøgelser af clindamycin inkluderede ikke tilstrækkeligt antal patienter i alderen 65 år og derover for at afgøre, om de reagerer forskelligt fra yngre patienter. Imidlertid indikerer anden rapporteret klinisk erfaring, at antibiotisk associeret colitis og diarré (på grund af Clostridium difficile ) set i forbindelse med de fleste antibiotika forekommer hyppigere hos ældre (> 60 år) og kan være mere alvorlige. Disse patienter skal overvåges omhyggeligt for udviklingen af diarré.
Farmakokinetiske undersøgelser med clindamycin har ikke vist nogen klinisk vigtige forskelle mellem unge og ældre individer med normal leverfunktion og normal (aldersjusteret) nyrefunktion efter oral eller intravenøs administration.
Overdoseringsoplysninger til cleocin i.v.
Betydelig dødelighed blev observeret hos mus i en intravenøs dosis på 855 mg/kg og hos rotter ved en oral eller subkutan dosis på ca. 2618 mg/kg. I musene blev der observeret kramper og depression.
Hæmodialyse og peritoneal dialyse er ikke effektive til at fjerne clindamycin fra serumet.
Kontraindikationer for cleocin i.v.
Dette lægemiddel er kontraindiceret hos personer med en historie med overfølsomhed over for præparater, der indeholder clindamycin eller Lincomycin.
Klinisk farmakologi for Cleocin I.V.
Fordeling
Biologisk inaktiv clindamycin -phosphat omdannes til aktiv clindamycin. Ved afslutningen af kortvarig intravenøs infusions-spids serumniveauer af aktivt clindamycin nås.
Efter intramuskulær injektion af clindamycin -phosphat -spidsniveauer af aktivt clindamycin nås inden for 3 timer hos voksne og 1 time hos pædiatriske patienter. Kurver på serumniveau kan konstrueres fra IV-spidserumniveauer som angivet i tabel 1 ved anvendelse af eliminering af halveringstider (se Udskillelse ).
Serumniveauer af clindamycin kan opretholdes over In vitro Minimum inhiberende koncentrationer for de fleste angivne organismer ved administration af clindamycin -phosphat hver 8. til 12. time hos voksne og hver 6. til 8. time hos pædiatriske patienter eller ved kontinuerlig intravenøs infusion. En ligevægtstilstand nås med den tredje dosis.
Der opnås ingen signifikante niveauer af clindamycin i cerebrospinalvæsken, selv i nærvær af betændte meninger.
Metabolisme
In vitro Undersøgelser i humane lever- og tarmmikrosomer indikerede, at clindamycin overvejende metaboliseres af cytochrome P450 3A4 (CYP3A4) med et mindre bidrag fra CYP3A5 til dannelse af clindamycinsulfoxid og en mindre metabolit N-desmethylclindamycin.
Udskillelse
Biologisk inaktiv clindamycin -phosphat forsvinder hurtigt fra serumet; Den gennemsnitlige eliminationshalveringstid er 6 minutter; Serum eliminering af halveringstid for aktiv clindamycin er imidlertid ca. 3 timer hos voksne og 2. timer hos pædiatriske patienter.
Særlige befolkninger
Nyre/leverdæmpning
Eliminationshalveringstiden for clindamycin øges lidt hos patienter med markant reduceret nyre- eller leverfunktion. Hæmodialyse og peritoneal dialyse er ikke effektive til at fjerne clindamycin fra serumet. Doseringsplaner behøver ikke ændres i nærvær af mild eller moderat nyre- eller leversygdom.
Brug hos ældre
Farmakokinetiske undersøgelser hos ældre frivillige (61-79 år) og yngre voksne (18-39 år) indikerer, at alder alene ikke ændrer clindamycin farmakokinetik (clearance eliminering halveringstid for distribution og område under serumkoncentrationstidskurve) efter IV-administration af clindamycin-fosfat. Efter oral administration af clindamycinhydrochlorid eliminering af halveringstiden øges til ca. 4,0 timer (område 3,4-5,1 timer) hos ældre sammenlignet med 3,2 timer (område 2,1-4,2 timer) hos yngre voksne. Omfanget af absorption 1 .
Serumassays til aktivt clindamycin kræver en hæmmer for at forhindre In vitro Hydrolyse af clindamycin -phosphat.
Tabel 1. Gennemsnitlig top- og trug -serumkoncentration af aktiv clindamycin efter dosering med clindamycin -phosphat
| Dosering Regimen | Spids MCG/ML | Trug MCG/ML |
| Raske voksne mænd (post ligevægt) | ||
| 10.9 | 2.0 | |
| 10.8 | 1.1 | |
| 14.1 | 1.7 | |
| 9 | ||
| Pædiatriske patienter (første dosis)* | ||
| 5-7 mg/kg IV in 1 hour | 10 | |
| 5-7 mg/kg IM | 8 | |
| 3-5 mg/kg IM | 4 | |
| *Data i denne gruppe fra patienter, der behandles for infektion. |
Mikrobiologi
Handlingsmekanisme
Clindamycin inhiberer bakteriel proteinsyntese ved binding til 23S RNA i 50S -underenheden af ribosomet. Clindamycin er bakteriostatisk.
Modstandsmodstand mod clindamycin er oftest forårsaget af modifikation af specifikke baser af 23S ribosomalt RNA. Krydsresistens mellem clindamycin og Lincomycin er komplet. Fordi bindingsstederne for disse antibakterielle lægemidler overlapper krydsresistensen, observeres undertiden blandt Lincosamides makrolider og streptogramin B.macrolidinducerbar resistens over for clindamycin forekommer i nogle isolater af makrolidresistente bakterier. Makrolidresistente isolater af staphylococci og beta-hemolytiske streptokokker skal screenes for induktion af clindamycin-resistens ved anvendelse af D-zone-testen.
Antimikrobiel aktivitet
Clindamycin har vist sig at være aktiv mod de fleste af isolaterne af følgende mikroorganismer begge In vitro og i kliniske infektioner som beskrevet i Indikationer og brug afsnit.
Gram-positive bakterier
Staphylococcus aureus (methicillin-følsomme stammer)
Streptococcus pneumoniae (penicillin-følsomme stammer)
Streptococcus pyogenes
Anaerobe bakterier
Clostridium perfringens
Fusobacterium necrophorum
Fusobacterium nucleatum
Peptostreptococcus Anaerobius
Prevotella melaninogenica
Mindst 90% af de mikroorganismer, der er anført nedenfor, udstiller In vitro Minimum inhiberende koncentrationer (MIC'er) mindre end eller lig med clindamycin-modtagelige mikrofon breakpoint for organismer af en lignende type som dem, der er vist i tabel 2. Imidlertid er effektiviteten af clindamycin til behandling af kliniske infektioner på grund af disse mikroorganismer ikke blevet etableret i tilstrækkelig og godt kontrollerede kliniske forsøg.
Gram-positive bakterier
Staphylococcus epidermidis (methicillin-følsomme stammer)
Streptococcus agalactiae
Streptococcus drypper
Streptococcus mild
Oral Streptococcus
Anaerobe bakterier
Actinomyces israelii
Clostridium clostridioforme
Eggerthella Lenta
FineGoldia (Peptostreptococcus) Fantastisk
Micromonas (Peptostreptococcus) Micros
Prevotella Bivia
Prevetella Intermedia
Propionibacterium acnes
Metoder for følsomhedstest
Når det er tilgængeligt, skal det kliniske mikrobiologilaboratorium give kumulativt In vitro Resultaterne af følsomhedstest for antimikrobielle lægemidler, der bruges i lokale hospitaler og praksisområder til lægen som periodiske rapporter, der beskriver modtagelighedsprofilen for nosokomiale og erhvervede patogener. Disse rapporter skal hjælpe lægen med at vælge et antibakterielt lægemiddel til behandling.
Fortyndingsteknikker
Kvantitative metoder anvendes til at bestemme antimikrobielle minimumshæmmende koncentrationer (MIC'er). Disse MIC'er tilvejebringer estimater af bakteriers følsomhed over for antimikrobielle forbindelser. MIC'erne skal bestemmes ved hjælp af en standardiseret testmetode 23 (bouillon og/eller agar). MIC -værdierne skal fortolkes i henhold til kriterierne, der er angivet i tabel 2.
Teknisk formidling
Kvantitative metoder, der kræver måling af zonediametre, kan også tilvejebringe reproducerbare estimater af bakteriers følsomhed for antimikrobielle forbindelser. Zonestørrelsen skal bestemmes ved hjælp af en standardiseret metode 25 . Denne procedure bruger papirdiske imprægneret med 2 mcg clindamycin til at teste bakteriers følsomhed over for clindamycin. Diskdiffusionsbrudpunkterne er tilvejebragt i tabel 2.
Anaerobe teknikker
For anaerobe bakterier kan modtageligheden for clindamycin bestemmes ved en standardiseret testmetode 24 . De opnåede MIC -værdier skal fortolkes i henhold til kriterierne, der er angivet i tabel 2.
Tabel 2. Modtagelighedstest Tolkende kriterier for clindamycin
| Patogen | Modtagelighedstolkningskriterier | |||||
| Minimale hæmmende koncentrationer (MIC i MCG/ML) | Diskdiffusion (Zonediametre i mm) | |||||
| S | I | R | S | I | R | |
| Staphylococcus spp. | ≤0,5 | 1-2 | ≥4 | ≥21 | 15–20 | ≤14 |
| Streptococcus pneumoniae og andet Streptococcus spp. | ≤0,25 | 0.5 | ≥1 | ≥19 | 16–18 | ≤15 |
| Anaerobe bakterier | ≤2 | 4 | ≥8 | Na | Na | Na |
| Na=not applicable |
En rapport om Modtagelige (r) Angiver, at det antimikrobielle lægemiddel sandsynligvis vil hæmme væksten af patogenet, hvis det antimikrobielle lægemiddel når koncentrationen, der normalt opnås på infektionsstedet. En rapport om Mellemliggende (i) Angiver, at resultatet skal betragtes som tvetydigt, og hvis mikroorganismen ikke er fuldt ud modtagelig for alternative klinisk gennemførlige lægemidler, skal testen gentages. Denne kategori indebærer mulig klinisk anvendelighed på kropssteder, hvor lægemidlet er fysiologisk koncentreret eller i situationer, hvor høj dosering af lægemiddel kan bruges. Denne kategori giver også en bufferzone, der forhindrer små ukontrollerede tekniske faktorer i at forårsage store uoverensstemmelser i fortolkningen. En rapport om Resistent (R) indikerer, at det antimikrobielle lægemiddel ikke sandsynligvis vil hæmme væksten af patogenet, hvis det antimikrobielle lægemiddel når koncentrationen, der normalt opnås på infektionsstedet; Anden terapi skal vælges.
Kvalitetskontrol
Standardiserede følsomhedstestprocedurer kræver anvendelse af laboratoriekontroller for at overvåge og sikre nøjagtigheden og præcisionen af de forsyninger og reagenser, der anvendes i analysen og teknikkerne for de personer, der udfører testen 2345 . Standard clindamycin -pulver skal tilvejebringe MIC -områderne i tabel 3. for diskdiffusionsteknikken ved anvendelse af 2 mcg clindamycin -disken skal kriterierne angivet i tabel 2 opnås.
Tabel 3. Acceptabel kvalitetskontrolintervaller for clindamycin
| QC -stamme | Acceptabel kvalitetskontrolintervaller | |
| Minimum hæmmende koncentrationsområde (MCG/ML) | Diskdiffusion Range (Zonediametre i mm) | |
| Enterococcus faecalis 1 ATCC 29212 | 4-16 | Na |
| Staphylococcus aureus ATCC 29213 | 06-0.25 | Na |
| Staphylococcus aureus ATCC 25923 | Na | 24-30 |
| Streptococcus pneumoniae ATCC 49619 | 0,03-0,12 | 19-25 |
| Bacteroides fragilis ATCC 25285 | 0,5-2 | Na |
| Bacteroides thetaiotaomicron ATCC 29741 | 2-8 | Na |
| Clostridium difficile 2 ATCC 700057 | 2-8 | Na |
| Eggerthella Lenta ATCC 43055 | 06-0.25 | Na |
| 1. Enterococcus faecalis er kun inkluderet i denne tabel til kvalitetskontrolformål. 2. Kvalitetskontrol for C. vanskelig udføres ved hjælp af Agar -fortyndingsmetoden kun alle andre obligatoriske anaerober kan testes ved enten bouillonmikrodilution eller agarfortyndingsmetoder. Na=Not applicable ATCC ® er et registreret varemærke til den amerikanske type kulturkollektion |
Referencer
1. Smith RB Phillips JP: Evaluering af cleocin HCI og cleocin -phosphat i en ældre population. Upjohn TR 8147-82-9122-021 december 1982.
2. CLSI. Præstationsstandarder for antimikrobiel følsomhedstest: 26 Th red. CLSI -supplement M100S. Wayne PA: Clinical and Laboratory Standards Institute; 2016.
3. CLSI. Metoder til fortynding af antimikrobielle følsomhedstest for bakterier, der vokser aerobt; Godkendt standard -Tende udgave. CLSI-dokument M07-A10. Wayne PA: Clinical and Laboratory Standards Institute; 2015.
4. CLSI. Metoder til antimikrobiel følsomhedstest af anaerobe bakterier; Godkendt standard-ottende udgave. CLSI-dokument M11-A8. Wayne PA: Clinical and Laboratory Standards Institute; 2012.
5. CLSI. Præstationsstandarder for antimikrobiel diskfølsomhedstest; Godkendte standard -T -WELVTH EDITION. CLSI-dokument M02-A12. Wayne PA: Clinical and Laboratory Standards Institute; 2015.
Patientinformation til cleocin i.v.
Patienter skal rådes om, at antibakterielle lægemidler inklusive cleocin -phosphat kun bør bruges til behandling af bakterieinfektioner. De behandler ikke virusinfektioner (f.eks. Koldkølelsen). Når cleocin -phosphat er ordineret til behandling af en bakterieinfektion, skal patienterne fortælles, at selv om det er almindeligt at føle sig bedre tidligt i løbet af terapien, skal medicinen tages nøjagtigt som anført. Spring over doser eller ikke gennemførelse af det fulde terapiforløb kan (1) mindske effektiviteten af den øjeblikkelige behandling og (2) øge sandsynligheden for, at bakterier vil udvikle resistens og ikke kan behandles med cleocinphosphat eller andre antibakterielle lægemidler i fremtiden.
Diarré er et almindeligt problem forårsaget af antibiotika, som normalt slutter, når antibiotikumet afbrydes. Undertiden efter start af behandling med antibiotika kan patienter udvikle vandige og blodige afføring (med eller uden mavekramper og feber), selv så sent som to eller flere måneder efter at have taget den sidste dosis af antibiotikumet. Hvis dette forekommer, skal patienter kontakte deres læge så hurtigt som muligt.
Instruktioner til brug til tilføjelsessystem.For IV Brug kun IV
Cleocin -phosphat ®
Clindamycin steril opløsning til injektion USP
I tilføjelse ® Hætteglas
For at åbne fortyndingsbeholder:
Skræl overpakke fra hjørnet og fjern beholderen. Nogle opacitet af plasten på grund af fugtabsorption under steriliseringsprocessen kan observeres. Dette er normalt og påvirker ikke løsningskvaliteten eller sikkerheden. Opaciteten mindskes gradvist.
Hvor skal man anvende gærinfektionscreme
At samle hætteglas og fleksibel fortyndingsbeslutning:
(Brug aseptisk teknik)
- Fjern beskyttelsesdækslerne fra toppen af hætteglasset og hætteglasporten på fortyndingsbeholderen som følger:
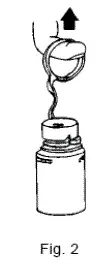
- For at fjerne udbruddet hætteglasskapsving sving trækringen over toppen af hætteglasset og træk langt nok ned til at starte åbningen (se figur 1.) og træk derefter lige op for at fjerne hætten. (Se figur 2.) NOTE: Når udbryderhætten er blevet fjernet Adgang ikke hætteglas med sprøjte.
- For at fjerne hætteglas havnedækslet skal du gribe fat i fanen på trækringen, træk op for at bryde de tre slipsstrenge og træk derefter tilbage for at fjerne dækslet. (Se figur 3.)

- Skru hætteglasset ind i hætteglasset, indtil den ikke går længere. Hætteglasset skal skrues tæt ind for at sikre et segl. Dette forekommer cirka 1/2 drejning (180 °) efter det første hørbare klik. (Se figur 4.) Kliklyden sikrer ikke et tætning; Hætteglasset skal drejes så langt, som det vil gå. NOTE: Når hætteglasset sidder, skal du ikke forsøge at fjerne det. (Se figur 4.)
- Kontroller hætteglasset for at sikre, at det er stramt ved at prøve at vende det længere i retning af samlingen.
- Etiket korrekt.
 |
 |
At forberede blanding:
- Klem bunden af fortyndingsbeholderen forsigtigt for at oppustes den del af beholderen, der omgiver slutningen af lægemiddelhætteglasset.
- Med den anden hånd skubber lægemidlet hætteglas ned i beholderen teleskopering af beholderens vægge. Tag fat i den indre hætte i hætteglasset gennem beholderens vægge. (Se figur 5.)
- Træk det indre hætte fra stoffet hætteglas. (Se figur 6.) Kontroller, at gummipropen er trukket ud, så lægemidlet og fortyndingsmidlet blandes.
- Bland containerindhold grundigt og brug inden for det specificerede tidspunkt.
 |
 |
Forberedelse til administration: (Brug aseptisk teknik)
- Bekræft aktivering og blanding af hætteglas indhold.
- Kontroller for lækager ved at klemme containeren fast. Hvis der findes lækager, kan der kasseres, da sterilitet kan være nedsat.
- Luk flowkontrolklemme af administrationssæt.
- Fjern dækslet fra udløbsporten i bunden af beholderen.
- Indsæt piercingstiften af administration, der er indstillet i port med en vridende bevægelse, indtil stiften sidder fast. Bemærk: Se fulde retninger på administrationssæt karton.
- Løft den frie ende af hængersløjfen på bunden af hætteglasset, der bryder de to slipsstrenge. Bøj løkken udad for at låse den i den lodrette position og derefter suspendere beholderen fra bøjlen.
- Klem og frigør dryppekammeret for at etablere korrekt væskeniveau i kammeret.
- Åben flowkontrolklemme og klar luft fra sæt. Luk klemme.
- Vedhæft indstillet til venipunkturindretning. Hvis enheden ikke er indbygget prime og laver venipunktur.
- Regulere administrationshastighed med flowkontrolklemme.
ADVARSEL: Do not use flexible container in series connections.


