Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
ErgotderivaterSandheda
Resume af lægemiddeloversigt
Hvad er Trudhesa?
Trudhesa (dihydroergotamin mesylat) næsespray er et ergotaminderivat, der bruges til behandling af migræne med eller uden aura hos voksne.
Hvad er bivirkninger af Trudhesa?
Sandheda
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- Langsom eller hurtig hjerteslag
- Svaghed i benene
- Muskelsmerter i armene eller benene
- prikken eller følelsesløshed
- Koldhed i hænder og fødder
- blå fingre og tæer
- Alvorlig mavesmerter
- kæbe eller venstre arm smerte
- brystsmerter eller pres
- Pludselig træthed
- Svaghed på den ene side af kroppen
- problemer med at tale
- Vision ændres
- Mental eller humørændringer
- forvirring
- udslæt
- kløe og
- Alvorlig svimmelhed
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Bivirkninger af Trudhesa inkluderer:
- løbende næse
- kvalme
- ændret følelse af smag
- Reaktioner på applikationsstedet
- svimmelhed
- opkast
- døsighed
- ondt i halsen og
- diarre.
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; Og pludselig svimmelhed Lightheadedness eller gå ud;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til Trudhesa
Den anbefalede dosis trudhesa nasal spray er 1,45 mg (indgivet som en målt spray på 0,725 mg i hver næsebor). Dosis kan gentages om nødvendigt mindst 1 time efter den første dosis.
Trudhesa hos børn
Sikkerhed og effektivitet af Trudhesa nasal spray er hos pædiatriske patienter er ikke blevet fastlagt.
Hvilke stoffer stoffer eller kosttilskud interagerer med Trudhesa?
Trudhesa nasal spray kan interagere med andre lægemidler, såsom:
- Betablokkere
- nikotin
- Selektiv serotonin genoptagelsesinhibitor ( Hvis ) Antidepressiva (f.eks. Fluoxetin fluvoxamin paroxetin sertralin)
- Proteaseinhibitorer (f.eks. Ritonavir Nelfinavir Indinavir)
- makrolid Antibiotika (f.eks. erythromycin Clarithromycin)
- Antifungals (f.eks. Ketoconazol itraconazol)
- triptans og
- Vasokonstriktorer.
Fortæl din læge alle medicin og kosttilskud, du bruger.
Trudhesa under graviditet og amning
Fortæl din læge, hvis du er gravid eller planlægger at blive gravid, før du bruger Trudhesa nasal spray. Det kan øge risikoen for for tidlig levering og kan skade et foster. Det er ukendt, om Trudhesa nasal spray passerer til modermælk; Imidlertid er ergotamin et beslægtet lægemiddel til stede i modermælk. På grund af potentialet for reduceret mælkeforsyning og alvorlige bivirkninger i det ammede spædbarn inklusive diarré, der opkastes svag puls og ustabil blodtryk, anbefales ikke under behandling under behandling med Trudhesa nasal spray og i 3 dage efter den sidste dosis. Brystmælkeforsyning i løbet af denne tid skal pumpes og kasseres.
Yderligere oplysninger
Vores Trudhesa (Dihydroergotamine mesylat) Nasal Spray Bivirkninger Drug Center giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.
Dette er ikke en komplet liste over bivirkninger, og andre kan forekomme. Ring til din læge for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Lægemiddelinteraktioner
- Advarsler
- Overdosis
- Kontraindikationer
- Klinisk farmakologi
- Medicin vejledning
ADVARSEL
Perifer iskæmi efter samtidig administration med stærke CYP3A4 -hæmmere
Alvorlig og/eller livstruende perifer iskæmi har været forbundet med samtidig administration af dihydroergotamin med stærke CYP3A4-hæmmere. Fordi CYP3A4 -hæmning øger serumniveauerne af dihydroergotamin, øges risikoen for vasospasme, der fører til cerebral iskæmi og/eller iskæmi af ekstremiteterne. Derfor er samtidig brug af Trudhesa med stærke CYP3A4 -hæmmere kontraindiceret [se Kontraindikationer ADVARSELS AND PRECAUTIONS og Lægemiddelinteraktioner ].
Beskrivelse af Trudhesa
Trudhesa (dihydroergotamin mesylat) næsespray er et enkeltdosis medikament-enhedskombinationsprodukt, der indeholder et dihydroergotamin-mesylat-lægemiddelbestanddel og en nasal spray-enhedsbestanddel.
Det kemiske navn for dihydroergotamin-mesylat er ergotaman-3 '6' 18-trione 910-dihydro- 12'-hydroxy-2'-methyl-5'- (phenylmethyl)-(5'a)-monomethanesulfonate. Dens molekylvægt er 679,78, og dens molekylære formel er C 33 H 37 N 5 O 5 • Ch 4 O 3 S.
Den kemiske struktur er:
 |
Lægemiddelbestanddelen er en dihydroergotamin -mesylatopløsning. Hver milliliter (ml) opløsning indeholder dihydroergotamin mesylat 4,0 mg (svarende til 3,43 mg dihydroergotamin) og følgende inaktive ingredienser: koffein (NULL,0 mg) kuldioxid (q.s.) dextrose (NULL,0 mg) og vand (q.s. til 1,0 ml).
Trudhesa nasal spray efter samling og priming leverer 0,725 mg dihydroergotamin mesylat pr. Spray. En samlet dosis på 1,45 mg dihydroergotamin -mesylat leveres i 2 spray. Nasal sprayindretning indeholder Hydrofluoroalkane-134A (HFA) drivmiddel.
Bruger til Trudhesa
Trudhesa er indikeret til akut behandling af migræne med eller uden aura hos voksne.
Begrænsninger af brug
Trudhesa er ikke indikeret til forebyggende behandling af migræne.
Trudhesa er ikke indikeret til håndtering af hemiplegisk eller basilar migræne.
Dosering til Trudhesa
Doseringsoplysninger
Den anbefalede dosis trudhesa er 1,45 mg indgivet som to målte spray i næsen (en spray på 0,725 mg i hver næsebor).
Dosis kan gentages om nødvendigt mindst 1 time efter den første dosis. Brug ikke mere end 2 doser Trudhesa inden for en 24-timers periode eller 3 doser inden for en 7-dages periode.
Vurdering inden den første dosis
Før påbegyndelse af Trudhesa anbefales en kardiovaskulær evaluering [se ADVARSELS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Vigtige administrationsinstruktioner
Trudhesa er kun til næseadministration og må ikke injiceres.
Trudhesa skal samles inden brug (se Brug til brug ). Brug eller kasser Trudhesa inden for 8 timer, når hætteglasset er åbnet, eller produktet er samlet.
Prime den samlede Trudhesa inden den første brug ved at frigive 4 spray. Brug Trudhesa umiddelbart efter priming. Kasser Trudhesa umiddelbart efter brug. Åbn og forbered en ny Trudhesa, hvis der er behov for en yderligere dosis.
Hvor leveret
Doseringsformularer og styrker
Trudhesa (dihydroergotamin mesylat) nasal spray er et enkeltdosis medikament-enhedskombinationsprodukt, der indeholder et hætteglas med dihydroergotamin-mesylat med en klar og farveløs til svagt gul opløsning og en intranasal leveringsenhed. Hver spray leverer 0,725 mg dihydroergotamin -mesylat.
Trudhesa (dihydroergotamin mesylat) næsespray (NULL,725 mg pr. Spray) leveres som en pakke med 4 enkeltdosisenheder ( NDC 77530-725-04). Hver enkelt dosisenhed indeholder:
- Et Amber Glass Vial ( NDC 77530-725-01) indeholdende 4 mg dihydroergotamin-mesylat i en 1 ml klar og farveløs til svagt gul opløsning. Stopperen er ikke lavet med naturgummi latex.
- En nasal spray -enhed.
Opbevaring og håndtering
Opbevar Trudhesa ved kontrolleret stuetemperatur 20 ° C til 25 ° C (68 ° F til 77 ° F) med udflugter tilladt mellem 15 ° C til 30 ° C (59 ° F til 86 ° F). Køl ikke køleskab eller frys.
Fremstillet af: Mipharm S.P.A. Milano Italien. Revideret: SEP 2021
Bivirkninger for Trudhesa
Følgende klinisk signifikante bivirkninger er beskrevet andetsteds i mærkningen:
- Perifer iskæmi efter samtidig administration med stærke CYP3A4 -hæmmere [se Boksadvarsel og ADVARSELS AND PRECAUTIONS ]
- Myocardial iskæmi og/eller infarkt andre bivirkninger ADVARSELS AND PRECAUTIONS ]
- Cerebrovaskulære bivirkninger og dødsfald [se ADVARSELS AND PRECAUTIONS ]
- Andre vasospasme relaterede bivirkninger [se ADVARSELS AND PRECAUTIONS ]
- Stigning i blodtrykket [se ADVARSELS AND PRECAUTIONS ]
- Medicin overforbrug hovedpine [se ADVARSELS AND PRECAUTIONS ]
- For tidligt arbejde [se ADVARSELS AND PRECAUTIONS ]
- Fibrotiske komplikationer [se ADVARSELS AND PRECAUTIONS ]
- Lokal irritation [se ADVARSELS AND PRECAUTIONS ]
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, kan der ikke sammenlignes bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte med hastigheder i de kliniske forsøg med et andet lægemiddel og muligvis ikke afspejler de satser, der er observeret i praksis.
Bivirkninger i placebo-kontrollerede forsøg med dihydroergotamin (DHE) mesylat næsespray [se Kliniske studier ]
Af de 1796 patienter og forsøgspersoner, der blev behandlet med DHE nasal spray -doser 2 mg eller mindre i amerikanske og udenlandske kliniske studier 26 (NULL,4%), ophørte på grund af bivirkninger. De bivirkninger, der er forbundet med seponering, var i faldende rækkefølge af frekvens: rhinitis (13) svimmelhed (2) ansigtsødem (2) og en patient hver på grund af kolde sved utilsigtet traumepression valgfri kirurgi somnolens allergi opkast hypotension og paraesthesia.
seroquel hvad bruges det til
Tabel 1 opsummerer forekomsten af bivirkninger rapporteret af mindst 1% af patienterne, der modtog DHE-næsespray til behandling af migræne under placebo-kontrollerede dobbeltblinde kliniske studier og var hyppigere end hos de patienter, der fik placebo. De mest almindeligt rapporterede bivirkninger (større end 1% af patienterne, der modtog DHE nasal spray), var rhinitis kvalme ændret følelse af smagsapplikationsreaktioner svimmelhed opkast somnolens pharyngitis og diarré. I de fleste tilfælde var disse begivenheder kortvarige og selvlimiterede og resulterede ikke i patientens seponering fra en undersøgelse.
Tabel 1 Bivirkninger rapporteret af mindst 1% af de næse-spray-behandlede patienter i DHE og forekom hyppigere end i placebo-gruppen i migræne placebokontrollerede forsøg
| Og nasal spray N = 597 % | Placebo N = 631 % | |
| Åndedrætssystem | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Gastrointestinalt system | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Specielle sanser andre | ||
| Altered Sense of Taste | 8 | 1 |
| Applikationswebsted | ||
| Applikationswebsted Reaction | 6 | 2 |
| Central og perifert nervesystem | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Krop som helhed general | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Muskuloskeletalsystem | ||
| Stiffness | 1 | <1 |
Bivirkninger i undersøgelser med Trudhesa
En åben-label-undersøgelse hos voksne (18 til 66 år) blev udført for at evaluere sikkerheden og tolerabiliteten af Trudhesa gentagen brug af Trudhesa blev tilladt i løbet af 6 til 12 måneder. I alt 354 patienter med migræne modtog mindst en dosis Trudhesa. Et hundrede og femogfirs patienter, der blev behandlet i gennemsnit mindst to migræne pr. Måned i 6 måneder og 55 patienter, der blev behandlet i gennemsnit mindst to migræne pr. Måned i 12 måneder. Af de patienter, der modtog mindst en dosis Trudhesa 185 (NULL,3%), oplevede patienter lokale irriterende symptomer. Af disse var de mest almindelige lokale irriterende symptomer nasopharyngitis rhinitis nasalt ubehagsprodukt smag unormal/dysgeusia bihulebesid ADVARSELS AND PRECAUTIONS ].
Oplevelse af postmarketing
Følgende bivirkninger er blevet identificeret under postapproval brug af dihydroergotamin -mesylat. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at pålideligt estimere deres frekvens eller etablere et årsagsforhold til eksponering for lægemidler:
Vasospasm Paræstesi Hypertension Dizziness Angst Dyspnø Hovedpine Flushing Diarré Rash Øget sved og pleural og retroperitoneal fibrose efter langvarig brug af dihydroergotamin. Tilfælde af myokardieinfarkt og slagtilfælde er rapporteret efter brugen af dihydroergotamin -mesylat [se ADVARSELS AND PRECAUTIONS ].
Lægemiddelinteraktioner for Trudhesa
CYP3A4 -hæmmere
Der har været sjældne rapporter om alvorlige bivirkninger i forbindelse med samtidig administration af intravenøs administration af dihydroergotamin og stærke CYP3A4 -hæmmere, såsom proteaseinhibitorer (f.eks. Ritonavir nelfinavir indinavir) makrolidantibiotika (f.eks itraconazol) resulterede i vasospasme, der førte til cerebral iskæmi og/eller iskæmi af ekstremiteterne [se ADVARSELS AND PRECAUTIONS ]. The use of strong CYP3A4 hæmmere with dihydroergotamine is contraindicated [see Kontraindikationer ]. Administer moderate CYP3A4 hæmmere (e.g. saquinavir Nefazodon Fluconazol grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Triptans
Triptans (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm og its effect could be additive with TRUDHESA. Therefore triptans og TRUDHESA should not be taken within 24 timer of each other [see Kontraindikationer ].
Betablokkere
Der har været rapporter om, at propranolol kan styrke den vasokonstriktive virkning af ergotamin ved at blokere den vasodilerende egenskab for epinephrin.
Vasokonstriktorer
Trudhesa er kontraindiceret til brug med perifere og centrale vasokonstriktorer, fordi kombinationen kan forårsage synergistisk forhøjelse af blodtrykket [se ADVARSELS AND PRECAUTIONS ].
Nikotin
Nikotin may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see ADVARSELS AND PRECAUTIONS ].
Selektiv serotonin genoptagelsesinhibitorer
Svaghedshyperreflexia og usikorering er sjældent rapporteret, når 5-HT 1 Agonister er blevet coadministreret med selektive serotonin genoptagelsesinhibitorer (f.eks. Fluoxetin fluvoxamin paroxetin sertralin).
Stofmisbrug og afhængighed
Kontrolleret stof
Trudhesa indeholder dihydroergotamin (som mesylatsalt), som ikke er et kontrolleret stof.
Misbrug
Misbrug is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Afhængighed
Fysisk afhængighed er en tilstand, der udvikler sig som et resultat af fysiologisk tilpasning som respons på gentagen stofbrug manifesteret ved tilbagetrækningstegn og symptomer efter pludselig seponering eller en betydelig dosisreduktion af et lægemiddel. I øjeblikket tilgængelige data har ikke vist fysisk eller psykologisk afhængighed med dihydroergotamin. Imidlertid er der rapporteret om tilfælde af psykologisk afhængighed hos patienter på andre former for ergotterapi.
Advarsler for Trudhesa
Inkluderet som en del af 'FORHOLDSREGLER' Afsnit
Forholdsregler for Trudhesa
Perifer iskæmi efter samtidig administration med stærke CYP3A4 -hæmmere
Alvorlig og/eller livstruende perifer iskæmi har været forbundet med samtidig administration af dihydroergotamin med stærke CYP3A4-hæmmere, herunder proteaseinhibitorer makrolidantibiotika og antifungals. Fordi CYP3A4 -hæmning øger serumniveauerne af dihydroergotamin, øges risikoen for vasospasme, der fører til cerebral iskæmi og/eller iskæmi af ekstremiteterne. Derfor er samtidig brug af Trudhesa med stærke CYP3A4 -hæmmere kontraindiceret [se Kontraindikationer og Lægemiddelinteraktioner ].
Myocardial iskæmi og/eller infarkt andre hjertesmålsreaktioner og dødsfald
Potentialet for bivirkninger af hjertesygdomme eksisterer med Trudhesa -behandling. Alvorlige bivirkninger, herunder nogle, der har været dødelige, har fundet sted efter brug af dihydroergotamin -mesylat. Disse begivenheder har inkluderet akut myokardieinfarkt livetsforstyrrende forstyrrelser af hjertehytme (f.eks. Ventrikulær takykardi og ventrikelflimmer) koronar arterie vasospasme og transient myokardial iskæmi.
Før påbegyndelse af Trudhesa anbefales en kardiovaskulær evaluering for at bestemme, om patienten er fri for koronararterie og iskæmisk myokardial sygdom eller anden signifikant underliggende hjerte -kar -sygdom. Hvis patientens medicinske historie (inklusive risikofaktorer) eller elektrokardiografiske undersøgelsesresultater er i overensstemmelse med koronararterien Vasospasme eller myokardie -iskæmi Trudhesa, bør ikke administreres [Se under den kardiovaskulære evaluering. Kontraindikationer ].
For patients with risk factors predictive of coronary artery disease (e.g. hypertension hypercholesterolemia smoker obesity diabetes strong family history of coronary artery disease females who are surgically or physiologically postmenopausal or males who are over 40 years of age) who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in Indstillingen af en udstyret sundhedsfacilitet, medmindre patienten tidligere har modtaget dihydroergotamin -mesylat. Under intervallet umiddelbart efter den første anvendelse af Trudhesa anbefales et elektrokardiogram hos de patienter med risikofaktorer, fordi iskæmi kan forekomme i fravær af kliniske symptomer.
Cerebrovaskulære bivirkninger og dødsfald
Potentialet for ugunstige cerebrovaskulære bivirkninger eksisterer med Trudhesa -behandling. Cerebral blødning subarachnoid blødning slagtilfælde og andre cerebrovaskulære begivenheder er rapporteret hos patienter behandlet med dihydroergotamin -mesylat; Og nogle har resulteret i dødsfald. I en række tilfælde ser det ud til, at de cerebrovaskulære begivenheder var primære, at dihydroergotamin -mesylatet var blevet administreret i den forkerte tro på, at de oplevede symptomer var en konsekvens af migræne, når de ikke var det. Det skal bemærkes, at patienter med migræne kan have en øget risiko for visse cerebrovaskulære begivenheder (f.eks. Slag blødning forbigående iskæmisk angreb). Afbryd Trudhesa, hvis der er mistanke om en cerebrovaskulær begivenhed.
Andre vasospasme -relaterede bivirkninger
Trudhesa som andre ergot -alkaloider kan forårsage andre vasospastiske reaktioner end koronar arterie vasospasme. Myocardial perifer vaskulær og kolonisk iskæmi er rapporteret med dihydroergotamin -mesylat.
Dihydroergotamin mesylatassocierede vasospastiske fænomener kan også forårsage muskelsmerter følelsesløsheds koldhed blekhed og cyanose af cifrene. Hos patienter med kompromitteret cirkulation kan vedvarende vasospasme resultere i gangren eller død. Trudhesa skal ophøres med det samme, hvis der udvikles tegn eller symptomer på vasokonstriktion.
Patienter, der oplever andre symptomer eller tegn, der tyder på nedsat arteriel strømning, såsom iskæmisk tarmsyndrom eller Raynauds syndrom efter brugen af enhver 5-HT-agonist, inklusive Trudhesa, bør evalueres af en sundhedsudbyder.
Stigning i blodtrykket
Der er rapporteret om betydelig højde i blodtrykket ved sjældne tilfælde hos patienter med og uden en historie med hypertension behandlet med dihydroergotamin -mesylat. Trudhesa er kontraindiceret hos patienter med ukontrolleret hypertension [se Kontraindikationer ].
En stigning på 18% i det gennemsnitlige pulmonale arterietryk blev set efter dosering med yderligere 5-ht 1 AGONIST I en undersøgelse, der evaluerer personer, der gennemgår hjertekateterisering.
Medicin overforbrug hovedpine
Overforbrug af akutte migrænemedicin (f.eks. Ergotaminer triptans opioider eller en kombination af disse lægemidler i 10 eller flere dage om måneden) kan føre til forværring af hovedpine (dvs. medicinsk overforbrug hovedpine). MEDICINICER Overforbrug Hovedpine kan præsentere som migræne-lignende daglig hovedpine eller som en markant stigning i hyppigheden af migræneangreb. Afgiftning af patienter, herunder tilbagetrækning af de overbrugte lægemidler og behandling af abstinenssymptomer (som ofte inkluderer en kortvarig forværring af hovedpine) kan være nødvendig.
For tidlig arbejdskraft
Baseret på virkningsmekanismen for dihydroergotamin og fund fra den offentliggjorte litteratur kan Trudhesa forårsage for tidlig arbejdskraft. Undgå brug af Trudhesa under graviditet [se Brug i specifikke populationer ]
Fibrotiske komplikationer
Potentialet for fibrotiske komplikationer findes ved Trudhesa -behandling. Der har været rapporter om pleural og retroperitoneal fibrose hos patienter efter langvarig daglig brug af dihydroergotamin -mesylat. Sjældent langvarig daglig brug af andre ergot -alkaloidlægemidler har været forbundet med hjerte -valvulær fibrose. Sjældne tilfælde er også rapporteret i forbindelse med brugen af dihydroergotamin -mesylat; I disse tilfælde modtog patienter imidlertid også lægemidler, der vides at være forbundet med hjertevævular fibrose.
Administration af Trudhesa bør ikke overstige doseringsretningslinjerne og bør ikke bruges til kronisk daglig administration [se Dosering og administration ].
Lokal irritation
Lokale irriterende symptomer blev rapporteret hos 52% af patienterne behandlet med mindst en dosis Trudhesa i et åbent forsøg, der muliggjorde gentagen brug af Trudhesa over 6 til 12 måneder. The most common local irritative symptoms (at least 1% of patients) were nasopharyngitis (21%) rhinitis (19%) nasal discomfort (7%) product taste abnormal/dysgeusia (6%) sinusitis (5%) sinus discomfort (4%) olfactory test abnormal [defined based on a change in score at a prespecified threshold on the University of Pennsylvania Smell Identifikationstest (UPSIT)] (4%) epistaxis (3%) Pharyngitis (3%) nasal slimhindeforstyrrelse (2%) ændring i lugt (1%) øre ubehag (1%) og rhinorrhea (1%). Hvis der opstår en alvorlig lokal irritationsbegivenhed af ingen andre tilskrivbare grunde, bør Trudhesa midlertidigt suspenderes, indtil begivenheden løser. Hvis begivenheden ikke løser, eller den gentages med genudfordring Trudhesa, skal der afbrydes permanent. Administration af Trudhesa bør ikke overstige doseringsretningslinjerne og bør ikke bruges til kronisk daglig administration [se Dosering og administration ].
Nasalt væv hos dyr behandlet med dihydroergotamin mesylat dagligt viste mild slimhindeirritation kendetegnet ved slimcelle og overgangscellehyperplasi og pladecelle -metaplasi. Ændringer i rotte -nasal slimhinde ved 64 uger var mindre alvorlige end ved 13 uger. Lokale effekter på luftvejsvæv efter kronisk intranasal dosering hos dyr er ikke blevet evalueret.
Oplysninger om patientrådgivning
Rådgiv patienten om at læse den FDA-godkendte patientmærkning ( Medicin vejledning og Brug til brug ).
losartan kalium 25 mg bivirkninger
Alvorlige og/eller livstruende reaktioner med samtidig administration af CYP3A4-hæmmere
Informer patienter om, at alvorlig og/eller livstruende perifer iskæmi (cerebral iskæmi og/eller iskæmi af ekstremiteterne) har været forbundet med samtidig administration af dihydroergotamin-mesylat og stærke CYP3A4-hæmmere, såsom makrolidantibiotika og proteaseinhibitorer [se Kontraindikationer ADVARSELS AND PRECAUTIONS og Lægemiddelinteraktioner ].
Myocardial iskæmi og/eller infarkt Andre hjertebegivenheder Cerebrovaskulære begivenheder og dødsfald
Informer patienter om risikoen for alvorlig hjertecerebrovaskulær og andre vasospasme -relaterede begivenheder. Rådgive patienter om at underrette deres sundhedsudbyder, hvis de udvikler nogen risikofaktorer eller symptomer, mens de tager Trudhesa. Informer patienter om, at nikotin kan provokere vasokonstriktion, der disponerer for en større iskæmisk respons [se ADVARSELS AND PRECAUTIONS ].
Medicin overforbrug hovedpine
Informer patienter om brug af lægemidler til behandling ADVARSELS AND PRECAUTIONS ].
Lokal irritation
Rådgive patienter om at underrette deres sundhedsudbyder, hvis de har generende lokal irritation [se ADVARSELS AND PRECAUTIONS ].
Lægemiddelinteraktioner
Rådgive patienter om at informere deres sundhedsudbydere, hvis de tager eller planlægger at tage nogen recept eller over-the-counter medicin, da der er et potentiale for interaktioner [se Lægemiddelinteraktioner ].
Graviditet
Rådgiv patienter om risikoen for for tidlig fødsel. Rådgive kvinder om at informere deres sundhedsudbyder, hvis de er gravide eller har til hensigt at blive gravide [se ADVARSELS AND PRECAUTIONS Brug i specifikke populationer ]
Amning
Rådgive patienter om ikke at amme under behandling med Trudhesa [se Brug i specifikke populationer ].
Vigtige administrationsinstruktioner
Rådgive patienter om, at Trudhesa skal samles inden brug, og at enheden inden administration skal primes (dvs. pumpes 4 gange). Instruer patienter om at bruge eller kassere Trudhesa inden for 8 timer, når hætteglasset er åbnet, eller produktet er samlet.
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
Carcinogenese
Vurdering af det kræftfremkaldende potentiale af dihydroergotamin -mesylat hos mus og rotter er ikke blevet vurderet.
Mutagenese
Dihydroergotamin mesylat var negativt i en In vitro mutagenicitet (ames) assay og positiv i In vitro Kromosomal afvigelse (V79 kinesisk hamstercelleassay med metabolisk aktivering og human perifere blodlymfocyt) assays. Dihydroergotamin var negativ i forgæves Micronucleus -assays i mus og hamster.
Værdiforringelse af fertiliteten
Der var ingen tegn på forringelse af fertiliteten hos rotter, der blev givet intranasale doser af dihydroergotamin mesylat op til 1,6 mg/dag, hvilket var forbundet med plasma -eksponeringer (AUC) ca. 3 gange det hos mennesker i den maksimale anbefalede humane dosis på 2,9 mg/dag.
Brug i specifikke populationer
Graviditet
Risikooversigt
Tilgængelige data fra offentliggjort litteratur indikerer en øget risiko for for tidlig levering med Trudhesa -brug under graviditet. Undgå brug af Trudhesa under graviditet [se ADVARSELS AND PRECAUTIONS ]. Data collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
In animal studies adverse effects on embryofetal development were observed following administration of dihydroergotamine mesylate during pregnancy (decreased fetal body weight and/or skeletal ossification) in rats and rabbits or during pregnancy and lactation in rats (decreased body weight and impaired reproductive function in the offspring) in rats at doses less than those used clinically and which were not associated with maternal toxicity (see Data ).
Den estimerede sats for større fødselsdefekter (NULL,2%til 2,9%) og spontanabort (17%) blandt leverancer til kvinder med migræne svarer til de rapporterede satser hos kvinder uden migræne. Alle graviditeter har en baggrundsrisiko for tab af fødselsdefekt eller andre bivirkninger. I den amerikanske generelle befolkning er den estimerede baggrundsrisiko for større fødselsdefekter og aborter i klinisk anerkendte graviditeter henholdsvis 2% til 4% og 15% til 20%.
Data
Dyredata
Intranasal administration af dihydroergotamin -mesylat til gravide rotter i hele perioden med organogenese resulterede i nedsat føtal kropsvægt og/eller skelet -ossifikation ved doser på 0,16 mg/dag (forbundet med plasma -eksponeringer [AUC] mindre end det hos mennesker ved den maksimale anbefalede humane dosis [MRHD] på 2,9 mg) eller større. Et no-virkningsniveau for embryofetal-toksicitet blev ikke identificeret hos rotter. Intranasal administration af dihydroergotamin -mesylat til gravide kaniner i hele organogenese resulterede i nedsat skelet -ossifikation ved 3,6 mg/dag. Ved dosis uden virkning (NULL,2 mg/dag) for bivirkninger på embryofetaludvikling hos kaniner var plasmaeksponeringer (AUC) mindre end hos mennesker ved MRHD.
Intranasal administration af dihydroergotamin -mesylat til hunrotter under hele graviditet og amning resulterede i nedsat kropsvægt og nedsat reproduktionsfunktion (nedsatte parringsindeks) blev observeret i afkom i doser på 0,16 mg/dag eller større. En dosis uden virkning til ugunstige udviklingseffekter hos rotter blev ikke fastlagt.
Effekter på udvikling forekom i doser under dem, der frembragte bevis for betydelig moderlig toksicitet i disse undersøgelser.
Dihydroergotamin-induceret intrauterin væksthæmning er blevet tilskrevet reduceret uteroplacental blodstrømning som følge af langvarig vasokonstriktion af livmoderfartøjer og/eller øget myometrial tone.
Amning
Risikooversigt
Der er ingen data om tilstedeværelsen af dihydroergotamin i human mælk; Imidlertid er ergotamin et beslægtet lægemiddel til stede i human mælk. Der er rapporter om diarré opkast svag puls og ustabilt blodtryk hos ammede spædbørn udsat for ergotamin. Trudhesa kan reducere mælkeforsyningen, fordi det kan reducere prolactinniveauerne. På grund af potentialet for reduceret mælkeforsyning og alvorlige bivirkninger i det ammede spædbarn inklusive diarré, der opkaster svag puls og ustabil blodtryk, rådgiver patienter om ikke at amme under behandling med Trudhesa og i 3 dage efter den sidste dosis. Brystmælkeforsyning i løbet af denne tid skal pumpes og kasseres.
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke etableret.
Geriatrisk brug
Kliniske undersøgelser af Trudhesa og andre dihydroergotamin -mesylatprodukter inkluderede ikke tilstrækkeligt antal forsøgspersoner i alderen 65 år og ældre til at afgøre, om de reagerer forskelligt fra yngre individer. Generelt skal valg af dosis for en ældre patient være forsigtig, der normalt starter ved den lave ende af doseringsområdet, der afspejler den større hyppighed af nedsat leverrenal eller hjertefunktion og af samtidig sygdom eller anden lægemiddelterapi.
Overdosis Information for Trudhesa
Symptomer
Overdrevne doser af dihydroergotamin kan resultere i perifere tegn og symptomer på ergotisme. Generelt ligner symptomerne på en akut Trudhesa -overdosis som en ergotamin overdosis, selvom der kan være mindre udtalt kvalme og opkast med Trudhesa. Symptomerne på en ergotamin overdosis inkluderer følgende: følelsesløshed prikkende smerte og cyanose i ekstremiteterne forbundet med formindskede eller fraværende perifere pulser; åndedrætsdepression; en stigning og/eller fald i blodtrykket normalt i denne rækkefølge; forvirring delirium kramper og koma; og/eller en vis grad af kvalme opkast og mavesmerter.
Hos laboratoriedyr blev dihydroergotamin dødbringende, når den blev givet ved intravenøse doser på 44 mg/kg hos mus 130 mg/kg hos rotter og 37 mg/kg hos kaniner.
Behandling
Behandling includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators og nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Kontraindikationer for Trudhesa
Trudhesa er kontraindiceret hos patienter:
ting at lave i Nashville, Tennessee
- med samtidig anvendelse af stærke CYP3A4 -hæmmere såsom proteaseinhibitorer (f.eks. Ritonavir nelfinavir eller indinavir) makrolidantibiotika (f.eks. Erythromycin eller clarithromycin) og antifungals (ketoconazol eller itraconazol) [se ADVARSELS AND PRECAUTIONS og Lægemiddelinteraktioner ]
- med iskæmisk hjertesygdom (angina pectoris historie om myokardieinfarkt eller dokumenteret tavs iskæmi) eller patienter, der har kliniske symptomer eller fund, der er i overensstemmelse med koronararterien vasospasme inklusive Prinzmetals variant angina [se ADVARSELS AND PRECAUTIONS ]
- med ukontrolleret hypertension [se ADVARSELS AND PRECAUTIONS ]
- med perifer arteriel sygdom
- med sepsis
- efter vaskulær kirurgi
- med alvorlig nedsat leverfunktion
- med alvorlig nedsat nyrefunktion
- med kendt overfølsomhed over for ergot alkaloider
- med nylig brug (dvs. inden for 24 timer) af andre 5-HT 1 Agonister (f.eks. Sumatriptan) eller ergotaminholdig eller ergot-type medicin [se Lægemiddelinteraktioner ]
- Med samtidig brug af perifere og centrale vasokonstriktorer, fordi kombinationen kan resultere i additiv eller synergistisk forhøjelse af blodtrykket [se ADVARSELS AND PRECAUTIONS ]
Klinisk farmakologi for Trudhesa
Handlingsmekanisme
Dihydroergotamin binder med høj affinitet til 5-HT 1da og 5-HT 1db receptorer. Den terapeutiske aktivitet af dihydroergotamin i migræne tilskrives generelt agonistvirkningerne ved 5-HT 1d receptorer.
Farmakodynamik
Der er rapporteret en betydelig højde i blodtrykket hos patienter med og uden en historie med hypertension [se ADVARSELS AND PRECAUTIONS ].
Dihydroergotamine besidder oxytociske egenskaber [se ADVARSELS AND PRECAUTIONS ].
Farmakokinetik
Absorption
Den gennemsnitlige tid fra dosering til maksimal plasmakoncentration efter Trudhesa -administration var ca. 0,5 timer.
Fordeling
Dihydroergotamin -mesylat er 93% plasmaprotein bundet. Det tilsyneladende steady-state-volumen af distribution er cirka 800 liter.
Eliminering
Metabolisme
Fire dihydroergotamin -mesylatmetabolitter er blevet identificeret i humant plasma efter oral administration. Den vigtigste metabolit 8'-ß-hydroxy-dihydroergotamin udviser affinitet svarende til dets forælder for adrenergiske og 5-HT-receptorer og demonstrerer ækvivalent styrke i flere Venoconstrictor-aktivitetsmodeller forgæves og In vitro . De andre metabolitter, dvs. dihydrolyserginsyre -dihydrolysergisk amid og en metabolit dannet ved oxidativ åbning af prolinringen, er af mindre betydning. Efter næseadministration repræsenterer samlede metabolitter kun 20% til 30% af plasma AUC. Den systemiske clearance af dihydroergotamin -mesylat efter intravenøs og intramuskulær administration er 1,5 l/min. Kvantitativ farmakokinetisk karakterisering af de fire metabolitter er ikke blevet udført.
Udskillelse
Den største udskillelsesrute for dihydroergotamin er via galden i fæces. Den samlede kropsafstand er 1,5 l/min, hvilket hovedsageligt reflekterer leverclearance. Kun 6% til 7% af uændret dihydroergotamin udskilles i urinen efter intramuskulær injektion. Nyreklarering (NULL,1 l/min) påvirkes ikke af ruten for Dihydroergotamine -administration.
Den gennemsnitlige tilsyneladende halveringstid for Trudhesa nasal administration hos raske forsøgspersoner er cirka 12 timer.
Specifikke populationer
Der er ikke foretaget undersøgelser af effekten af nyre eller lever for nedsat køns race etnicitet eller graviditet på dihydroergotamin farmakokinetik [se Kontraindikationer Brug i specifikke populationer ].
Lægemiddelinteraktionsundersøgelser
CYP3A4 -hæmmere
Sjældne rapporter om ergotisme er opnået fra patienter behandlet med dihydroergotamin og makrolidantibiotika (f.eks. Clarithromycin erythromycin) og fra patienter, der blev behandlet med dihydroergotamin og proteaseinhibitorer (f.eks. Ritonavir), formodentlig på grund af inhibering af Cyp3a -metabolism af åotamin (ser på åtamin (ser på åotamin (se på åotamine (see (ser på åotamine (ser på åotamin af engamin af åotamin af oGotamine af engamin af åotamin af åotamin af åotamin af åotamin af åotamin af åtamin af åtamin af åtaminet Kontraindikationer ].
Andre stoffer
Farmakokinetikken af dihydroergotamin syntes ikke at være signifikant påvirket af den samtidige anvendelse af en lokal vasokonstriktor.
Flere orale doser af ß-adrenoceptorantagonisten propranolol anvendt til migræneprofylakse havde ingen signifikant indflydelse på Cmax Tmax eller AUC af dihydroergotamindoser op til 4 mg. Propranolol kan dog forstærke den vasokonstriktive virkning af ergotamin [se Lægemiddelinteraktioner ].
Effekten af orale prævention på farmakokinetikken i Trudhesa er ikke undersøgt.
Kliniske studier
Effektiviteten af Trudhesa er baseret på den relative biotilgængelighed af Trudhesa nasal spray sammenlignet med dihydroergotamin mesylatnasal spray hos raske individer.
De kliniske undersøgelser beskrevet nedenfor blev udført under anvendelse af dihydroergotamin mesylatnasal spray.
Effektiviteten af dihydroergotamin-mesylatnasal spray til akut behandling af migrænehovedpine blev evalueret i fire randomiserede dobbeltblinde placebo-kontrollerede studier i USA Patientpopulationen i forsøgene var overvejende kvinder (87%) og kaukasiske (95%) med en gennemsnitlig alder på 39 år (række 18 til 65 år). Patienter behandlede en enkelt moderat til svær migrænehovedpine med en enkelt dosis af studiemedicin og vurderede smerter i smerter i løbet af 24 timer efter behandlingen. Hovedpine -respons blev bestemt 0,5 1 2 3 og 4 timer efter dosering og blev defineret som en reduktion i hovedpineens sværhedsgrad til mild eller ingen smerter. I undersøgelser 1 og 2 blev der anvendt en fire-punkts smerteintensitetsskala; I undersøgelser 3 og 4 blev der anvendt en fem-punkts skala til at registrere smerterespons. Selvom redningsmedicin var tilladt hos alle fire studier, blev patienter instrueret om ikke at bruge dem i den fire timers observationsperiode. I undersøgelser 3 og 4 blev en total dosis på 2 mg sammenlignet med placebo. I undersøgelser 1 og 2 doser på 2 og 3 mg blev evalueret og viste ingen fordel ved den højere dosis til en enkelt behandling. I alle undersøgelser modtog patienter et regime bestående af 0,5 mg i hver næsebor, der blev gentaget på 15 minutter (og igen på yderligere 15 minutter for 3 mg dosis i undersøgelser 1 og 2).
Procentdelen af patienter, der opnåede hovedpine -respons 4 timer efter behandling, var signifikant større hos patienter, der fik 2 mg doser af dihydroergotamin -mesylatnasal spray sammenlignet med dem, der modtog placebo i 3 af de 4 undersøgelser (se tabel 2 og tabel 3 og figur 1 og figur 2).
Tabel 2 Undersøgelser 1 og 2: Procentdel af patienter med hovedpine -respons a 2 og 4 timer efter en enkelt behandling af studiemedicin (dihydroergotamin mesylat nasal spray eller placebo)
| N | 2 timer | 4 timer | ||
| Undersøgelse 1 | Dihydroergotamin mesylat næsespray | 105 | 61%** | 70%** |
| Placebo | 98 | 23% | 28% | |
| Forskel fra placebo | 37% | 42% | ||
| Undersøgelse 2 | Dihydroergotamin mesylat næsespray | 103 | 47% | 56%* |
| Placebo | 102 | 33% | 35% | |
| Forskel fra placebo | 14% | 21% | ||
| a Hovedpine -respons blev defineret som en reduktion i hovedpineens sværhedsgrad til mild eller ingen smerter. Hovedpine-respons var baseret på smerteintensitet som fortolket af patienten ved hjælp af en fire-punkts smerteintensitetsskala. *P -værdi <0.01 ** P -værdi <0.001 |
Tabel 3 Undersøgelser 3 og 4: Procentdel af patienter med hovedpine -respons a 2 og 4 timer efter en enkelt behandling af studiemedicin (dihydroergotamin mesylat nasal spray eller placebo)
| N | 2 timer | 4 timer | ||
| Undersøgelse 3 | Dihydroergotamin mesylat næsespray | 50 | 32 | 48%* |
| Placebo | 50 | 20% | 22% | |
| Forskel fra placebo | 12% | 26% | ||
| Undersøgelse 4 | Dihydroergotamin mesylat næsespray | 47 | 30% | 47% |
| Placebo | 50 | 20% | 30% | |
| Forskel fra placebo | 10% | 17% | ||
| a Hovedpine -respons blev defineret som en reduktion i hovedpineens sværhedsgrad til mild eller ingen smerter. Hovedpine-respons blev evalueret på en fem-punkts skala, der omfattede smerterespons. *P -værdi <0.01 |
Kaplan-Meier-plottet nedenfor (figur 1 og figur 2) giver et skøn over sandsynligheden for, at en patient har reageret på en enkelt 2 mg dosis dihydroergotamin-mesylatnasal spray som en funktion af den tid, der er gået siden påbegyndelse af behandlingen.
Figur 1 Estimeret sandsynlighed for, at en patient reagerede i løbet af de fire timer efter en enkelt 2 mg dosis dihydroergotamin mesylatnasal spray som en funktion af den tid, der er gået siden påbegyndelse af behandlingen*
| *Figuren viser sandsynligheden over tid for at opnå et svar efter behandling med dihydroergotamin mesylatnasal spray. Hovedpine -respons var baseret på smerteintensitet som fortolket af patienten ved hjælp af en firpoint smerteintensitetsskala. Patienter, der ikke opnåede respons inden for 4 timer, blev censureret til 4 timer. |
Figur 2 estimeret sandsynlighed for, at en patient reagerer på dihydroergotamin mesylatnasal spray i løbet af de fire timer efter dosering*
| *Figuren viser sandsynligheden over tid for at opnå et svar efter behandling med dihydroergotamin mesylatnasal spray. Hovedpine-respons blev evalueret på en fem-punkts skala, der omfattede smerterespons. Patienter, der ikke opnåede respons inden for 4 timer, blev censureret til 4 timer. |
For patienter med migræne-associeret kvalmefotofobi og fonofobi ved baseline var der en lavere forekomst af disse symptomer ved 2 og 4 timer efter administration af dihydroergotamin mesylatnasal spray sammenlignet med placebo.
Patienter fik ikke lov til at bruge yderligere behandlinger i 8 timer før undersøgelsen af medicinering af medicin og i løbet af 4-timers observationsperiode efter undersøgelsesbehandling. Efter den 4-timers observationsperiode fik patienterne lov til at bruge yderligere behandlinger. For alle undersøgelser er den estimerede sandsynlighed for patienter, der bruger yderligere behandlinger til deres migræne i løbet af 24 timer efter den enkelte 2 mg dosis af undersøgelsesbehandling, opsummeret i figur 3 nedenfor.
Figur 3 estimeret sandsynlighed for en patient ved anvendelse af yderligere behandlinger til migræne i løbet af 24 timer efter enten dihydroergotamin mesylat nasal spray 2 mg (eller placebo)*
| *Kaplan-Meier-plot baseret på data opnået fra alle undersøgelser med patienter, der ikke bruger yderligere behandlinger censureret til 24 timer. Alle patienter fik en enkelt behandling af undersøgelsesmedicin til deres migræneangreb. Handlingen inkluderer også patienter, der ikke havde noget svar på den indledende dosis. |
Hverken alder eller køn ser ud til at påvirke patientens respons på dihydroergotamin mesylatnasal spray. Racedistributionen af patienter var utilstrækkelig til at bestemme virkningen af race på effektiviteten af dihydroergotamin mesylatnasal spray.
Patientinformation til Trudhesa
Trusta ™
(Trae - DEH - en)
(dihydroergotamin mesylat) næsespray
Hvad er de vigtigste oplysninger, jeg skal vide om Trudhesa?
Trudhesa kan forårsage alvorlige bivirkninger, herunder:
- Alvorlige problemer med blodcirkulation til dine ben og fødder (perifer iskæmi). Trudhesa kan forårsage perifer iskæmi, når du tager den med visse lægemidler kendt som CYP3A4 -hæmmere. Perifer iskæmi kan føre til et slagtilfælde og død. Stop med at tage Trudhesa og få akutmedicinsk hjælp med det samme, hvis du har nogen af følgende symptomer:
- Krampe og smerter i dine ben eller hofter
- følelse af tyngde eller tæthed i dine benmuskler
- brændende eller ømme smerter i dine fødder eller tæer, mens du hviler
- følelsesløshed prikken eller svaghed i dine ben
- kold følelse eller farveændringer i 1 eller begge ben eller fødder
- sløret tale
- Pludselig svaghed
Tag ikke medicin kendt som stærke CYP3A4 -hæmmere som:
-
- Ritonavir
- erythromycin
- ketoconazol
- Netfinavir
- Clarithromycin
- itraconazol
Dette er ikke alle de medicin, der kan påvirke, hvordan Trudhesa fungerer. Din sundhedsudbyder kan fortælle dig, om det er sikkert at tage Trudhesa med andre medicin.
Hvad er Trudhesa?
Trudhesa er en receptpligtig medicin, der bruges til akut behandling af migræne med eller uden aura hos voksne.
- Trudhesa bruges ikke til at forhindre migræne.
- Trudhesa bruges ikke til at behandle andre typer hovedpine såsom hemiplegisk (der gør dig ikke i stand til at bevæge sig på den ene side af din krop) eller basilar (sjælden form for migræne med aura) migræne.
Det vides ikke, om Trudhesa er sikker og effektiv hos børn.
Tag ikke Trudhesa, hvis du:
- tager medicin kendt som stærke CYP3A4 -hæmmere.
- har hjerteproblemer eller en historie med hjerteproblemer.
- har ukontrolleret højt blodtryk.
- har indsnævring af blodkar i dine ben arme mave eller nyrer (perifer vaskulær sygdom).
- har sepsis.
- har haft vaskulær kirurgi.
- har alvorlige leverproblemer.
- har alvorlige nyreproblemer.
- er allergiske over for dihydroergotamin mesylat ergot -alkaloider eller ingredienser i Trudhesa. Se slutningen på denne medicinvejledning for en komplet liste over ingredienser.
- har taget nogen af følgende lægemidler inden for de sidste 24 timer:
- Sumatriptan
- Almotriptan
- Eletriptan
- Frovatriptate
- Naratriptan
- Rizatriptan
- Ergotamin eller ergotamin-medicin
- har taget medicin, der indsnævrer dine blodkar eller hæver dit blodtryk.
Spørg din sundhedsudbyder, om du ikke er sikker på, om du tager nogen af disse medicin. Din sundhedsudbyder kan fortælle dig, om det er sikkert at tage Trudhesa med andre medicin.
Før du tager Trudhesa, fortæl din sundhedsudbyder om alle dine medicinske tilstande, herunder hvis du:
- har højt blodtryk.
- har leverproblemer.
- har nyreproblemer.
- røg.
- er gravide eller planlægger at blive gravid. Trudhesa kan forårsage for tidlig arbejdskraft. Trudhesa bør undgås under graviditet. Tal med din sundhedsudbyder med det samme, hvis du er gravid eller vil blive gravid.
- er amning eller planlægger at amme. Trudhesa kan reducere modermælkforsyningen og passere ind i din modermælk. Trudhesa kan være skadelig for din baby. Amm ikke din baby, mens du tager Trudhesa, og i 3 dage efter du har brugt Trudhesa. Tal med din sundhedsudbyder om den bedste måde at fodre din baby på, hvis du tager Trudhesa.
Fortæl din sundhedsudbyder om alle de medicin, du tager inklusive receptpligtige og over-the-counter medicin vitaminer og urtetilskud. Din sundhedsudbyder vil beslutte, om du kan tage Trudhesa med dine andre medicin.
Fortæl især din sundhedsudbyder, hvis du tager:
-
- Sumatriptan
- Fluconazol
- propranolol eller andre lægemidler, der kan sænke din hjerterytme
- Ergot-type medicin o grapefrugtjuice o enhver medicin, der kan øge dit blodtryk
- saquinavir o zileuton o selektiv serotonin Genoptag hæmmere
- Nefazodon
- nikotin
Dette er ikke alle de medicin, der kan påvirke, hvordan Trudhesa fungerer. Din sundhedsudbyder kan fortælle dig, om det er sikkert at tage Trudhesa med andre medicin.
Hvordan skal jeg tage Trudhesa?
- Visse mennesker bør tage deres første dosis Trudhesa på deres lægekontor eller i en anden medicinsk ramme. Spørg din læge, om du skal tage din første dosis i en medicinsk ramme.
- Brug Trudhesa nøjagtigt, som din sundhedsudbyder fortæller dig at bruge den. Læs og følg instruktionerne i Brug til brug som er forsynet med Trudhesa -pakken før brug.
- Du skal bruge Trudhesa, så snart symptomerne på din hovedpine starter, men det kan gives til enhver tid under en migræne.
- Efter at have sammensat Trudhesa og priming af enheden spray 1 gang i hver næsebor (en komplet dosis).
- Hvis din hovedpine kommer tilbage efter den første komplette dosis, eller du kun får en vis lettelse fra din hovedpine, kan du bruge en anden dosis 1 time efter den første komplette dosis. Brug en ny Trudhesa nasal spray -enhed til den anden dosis.
- Brug ikke mere end 2 doser Trudhesa inden for en 24-timers periode eller 3 doser inden for en 7-dages periode.
- Hvis du bruger for meget Trudhesa, skal du ringe til din sundhedsudbyder eller gå til det nærmeste hospitalets alarmrum med det samme.
- At tage Trudhesa i 10 eller flere dage om 1 måned kan gøre din hovedpine værre. Du skal skrive ned, når du har hovedpine, og når du tager Trudhesa, så du kan tale med din sundhedsudbyder om, hvordan Trudhesa fungerer for dig.
Hvad er de mulige bivirkninger af Trudhesa?
Trudhesa kan forårsage alvorlige bivirkninger, herunder:
Se 'Hvad er de vigtigste oplysninger, jeg burde vide om Trudhesa?'
- Hjerteanfald og andre hjerteproblemer. Hjerteproblemer kan føre til død. Stop med at tage Trudhesa og få akutmedicinsk hjælp med det samme, hvis du har nogen af følgende symptomer på en hjerteanfald :
- Ubehag i midten af dit bryst, der varer i mere end et par minutter, eller som går væk og kommer tilbage
- Alvorlig stramhedssmerter eller tyngde i din brysthalshals eller kæbe
- Smerter eller ubehag i dine arme tilbagehals kæbe eller mave
- åndenød med eller uden ubehag i brystet
- Bryder ud i en kold sved
- kvalme or opkast
- Føler sig let
Trudhesa er ikke for mennesker med risikofaktorer for hjertesygdomme, medmindre en hjerteeksamen er udført og ikke viser noget problem. Du har en højere risiko for hjertesygdomme, hvis du:
-
- har højt blodtryk
- har høje kolesterolniveauer
- røg
- er overvægtige
- har diabetes
- har en familiehistorie med hjertesygdomme
- Slag. Stop med at tage Trudhesa og få akutmedicinsk hjælp med det samme, hvis du har nogen af følgende symptomer på et slagtilfælde:
- ansigt hængende
- usædvanlig svaghed eller følelsesløshed
- sløret tale
- Ændringer i farve eller fornemmelse i dine fingre og tæer (Raynauds syndrom).
- Mave og tarmproblemer (Gastrointestinal og colonic iskæmiske begivenheder). Symptomer på gastrointestinale og koloniske iskæmiske begivenheder inkluderer:
- Pludselig eller svær mavesmerter
- forstoppelse eller diarré
- Mavesmerter efter måltider
- Blodig diarré
- vægttab
- feber
- kvalme or opkast
- Forøg blodtrykket.
- Medicin overforbrug hovedpine. Nogle mennesker, der bruger for meget Trudhesa, kan gøre deres hovedpine værre (medicin overforbrug hovedpine). Hvis din hovedpine bliver værre, kan din sundhedsudbyder beslutte at stoppe din behandling med Trudhesa.
- For tidlig arbejdskraft.
- Vævsændringer (fibrotiske komplikationer). Nflammation og fiberlignende væv, der ikke er normalt (fibrose), kan forekomme omkring lungerne og maven.
- Brændende følelser i din næse mund og hals og unormal smag.
De mest almindelige bivirkninger af Trudhesa inkluderer:
- løbende næse
- Reaktioner på applikationsstedet
- søvnighed
- kvalme
- svimmelhed
- ondt i halsen
- unormal smag
- opkast
- diarre
Dette er ikke alle de mulige bivirkninger Trudhesa.
Ring til din læge for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare Trudhesa?
Hold Trudhesa væk fra varme og lys.
- Opbevar Trudhesa ved stuetemperatur mellem 68 ° F til 77 ° F (20 ° C til 25 ° C).
- Køl ikke køleskab eller frys.
- Efter at et Trudhesa -hætteglas er åbnet, skal den smides væk efter 8 timer.
Hold Trudhesa og alle medicin uden for børns rækkevidde.
Kast ikke Trudhesa i brand eller forbrændingsanlæg, da beholderen inde i enheden kan eksplodere.
Generel information om sikker og effektiv anvendelse af Trudhesa.
Medicin er undertiden ordineret til andre formål end dem, der er anført i en medicinguide. Brug ikke Trudhesa til en betingelse, som den ikke blev ordineret til. Giv ikke Trudhesa til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem. Du kan bede din farmaceut eller sundhedsudbyder om information om Trudhesa, der er skrevet til sundhedsfagfolk.
Hvad er ingredienserne i Trudhesa?
Aktiv ingrediens: Dihydroergotamin mesylat
Inaktive ingredienser: Koffeindioxid dextrose og vand. Nasal sprayenhedsbeholderen indeholder Hydrofluoroalkane-134a (HFA) drivmiddel. Hætteglasstoppen er ikke lavet med naturgummi latex. Trudhesa er et varemærke til Impel Neuropharma Inc.
Denne medicinguide er godkendt af U.S. Food and Drug Administration.
Brug til brug
Trusta ™
(Roe-sa)
(dihydroergotamin mesylat)
nasal spray
Kun til nasal brug
Indledning
Læs disse instruktioner til brug, før du begynder at bruge Trudhesa, og hver gang du får en receptpligtig påfyldning. Der kan være ny information.
Disse oplysninger indtager ikke stedet for at tale med din sundhedsudbyder om din medicinske tilstand eller behandling. Du og din sundhedsudbyder skal tale om Trudhesa, når du begynder at tage den og ved regelmæssige kontrol.
Det er vigtigt at følge disse retninger nøjagtigt for at modtage den rigtige dosis. Kontakt din sundhedsudbyder, hvis du har spørgsmål til, hvordan du bruger dette produkt.
 |
Nasal spray -enhedsdele
 |
Glashætteglas
 |
Vigtige oplysninger, du har brug for, inden du doserer med Trudhesa
- Kun til næsebrug.
- Prime altid næsesprayenheden inden dosering ved at pumpe fingergreb og glashætteglas sammen nøjagtigt 4 gange
- Formålet med priming er at bringe medicinen til spidsen af sprøjtedysen. Du kan muligvis ikke se væske eller spray komme ud af dysen under hver priminghandling.
- Under priming kan du helt sikkert målrette sprøjtedysen væk fra dit ansigt og alt, hvad du ikke ønsker at komme i kontakt med sprayen af medicin.
- En komplet dosis er 2 spray; 1 spray i hver næsebor.
- Gør ikke Tag mere end 2 doser inden for en 24-timers periode. Gør ikke Tag mere end 3 doser i en 7-dages periode.
- Hold altid næse sprayenheden perfekt lodret, når du er priming, og når du doserer.
- Sniffing, mens dosering ikke er nødvendig. Howeversniffing vil ikke skade dig eller gøre medicinen mindre effektiv.
- Dette næsesprayenhedsprodukt er enkeltdosis (kun for en komplet dosis) og bør kastes væk (kasseres) efter brug. Du har brug for et nyt sæt til hver dosis.
- Hold produktet i sagen, indtil den er klar til brug.
- Efter at et Trudhesa -hætteglas er åbnet, skal det kastes væk efter 8 timer.
- Gør ikke Åbn glashætteglasset og udsæt for luften, indtil den er klar til brug.
- Opbevares ved stuetemperatur i et rent tørt område.
- Gør ikke Brug, hvis produktet er beskadiget.
- Gør ikke Brug, hvis produktet udløb.
- Hvert glashætteglas og nasal spray -enhed kan kun bruges 1 gang. Kast hele næsesprayenheden efter dosering uden at fjerne glashætteglasset.
- Du kan tage en anden komplet dosis mindst 1 time efter din første dosis, hvis dine symptomer fortsætter.
Opbevaring af Trudhesa
- Opbevar Trudhesa ved stuetemperatur mellem 68 ° F til 77 ° F (20 ° C til 25 ° C).
- Opbevar Trudhesa i den originale emballage i et rent område væk fra varme og lys ( Figur a ).
- Hold Trudhesa i den originale emballage, indtil du er klar til brug.
- Gør ikke Køleskab eller frys Trudhesa.
- Hold Trudhesa og alle medicin uden for børns rækkevidde.
 |
Forbereder sig på dosis med Trudhesa
Trin 1: Saml og tjek forsyninger
 |
 |
- Kontroller, at du bruger den rigtige medicin til din migræne (se Figur b ).
- Kontroller for at sikre, at Trudhesa ikke er udløbet (EXP) (se Figur c ).
- Hvis udløbet kast væk og få et nyt glashætteglas.
- Kontroller, at glashætteglas og blå plastikdæksel ikke ser beskadiget ud.
Trin 2: Fjern blå plastikdækketalfolie og grå gummiprop fra glashætteglas
 |
 |
 |
- Fjern (vend op) det blå plastikdæksel fra glashætteglasset (se Figur d ).
- Brug det blå plastdæksel til langsomt at skrælle metalfolien fra den grå gummiprop i en cirkulær bevægelse (se Figur e ).

- Træk den grå gummi stopper op og ud af glashætteglasset ( Figur f og Figur g ).
- Kast væk (kasser) dækfolie og grå gummiprop i papirkurven.
Trin 3: Fjern det klare plastikdæksel fra næsesprayenheden
- Hold nasal sp -rupray -enhed lodret.
- Træk ned på det klare plastikdæksel, og fjern det fra næsesprayenheden ( Figur h ).
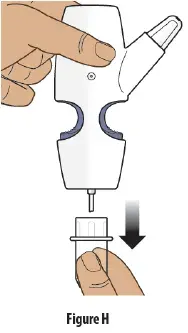
- Kast den kære plastikafdækning væk.
Trin 4: Skru glashætteglasset ind i næsesprayenheden
 |
 |
- Hold næsesprayenheden lodret.
- Push glashætteglas forsigtigt i bunden af nasal sparay -enheden (se Figur i ) og skru den på, indtil det er sikret som vist i Figur j .
Trin 5: Prime næsesprayenheden ved at pumpe fire gange med fingre og tommelfinger
 |
- Hold næsesprayenheden lodret .
- Peg spray -dysen væk fra dit ansigt.
- Placer tommelfingeren på bunden af glashætteglasset, og placer din markør (indeks) og langfingre på fingergrebet (se Figur k ).
- Pump nasal spray -enhed nøjagtigt 4 gange.
- For at pumpe næsesprayenheden trækker fingeren på fingergriberen dowm fast og tryk på glashætteglasset op på samme tid. Slip derefter (se Figur k )
- Du kan se noget medicin sprøjte ud under priming. Dette er normalt. Det er okay, hvis du ikke ser medicin sprøjte ud på de første par pumper.
Vigtigt tip: Formålet med priming er at bringe medicinen til spidsen af sprøjtedysen. Hvis du ikke primerer nasal spray -enhed, får du ikke din korrekte dosis medicin.
Premer altid nasal spray -enhed før brug ved pumpning nøjagtigt 4 gange.
Under grundning skal du sørge for at sigte dysen væk fra dit ansigt og alt hvad du ikke ønsker at komme i kontakt med medicinsk spray.
Brug af Trudhesa
Trin 6: Placer næsesprayenheden
 |
- Drej eller greb den næse sprey-enhed, så sprøjtedysen vender mod dig.
- Sørg for, at dit hoved er lige, og at næsesprayenheden er lodret.
- Indsæt sparay -dysen i dit første næsebor så langt som behageligt (se Figur l ).
Trin 7: Sprøjt den første spray i 1 næsebor
- Tryk fast på fingergreb Figur m ).Then release.
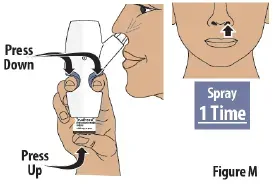
- Lever kun 1 spray ind i denne næsebor.
Trin 8: Sprøjt den anden spray ind i anden næsebor
- Flyt sprøjtedysen ind i din anden næsebor.
- Tryk fast på fingergrebet og tryk på glashætteglasset på samme tid for at levere den anden spray (se Figur n ).Then release.
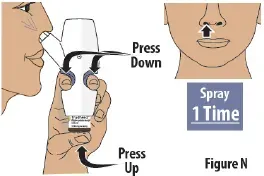
- Lever kun 1 spray ind i denne næsebor.
Vigtigt tip: En komplet dosis er 2 spray; 1 spray i hver næsebor.
Hvilken type antibiotikum er nitrofurantoin
Gør ikke Tag mere end 2 doser inden for en 24-timers periode. Gør ikke Tag mere end 3 doser i en 7-dages periode.Please refer to the prescribing information for more information.
Sniffing, mens eller efter dosering er ikke nødvendig. Howeversniffing vil ikke skade dig eller gøre medicinen mindre effektiv.
Vigtige ofte stillede spørgsmål (ofte stillede spørgsmål)
Spørgsmål: Kan jeg gemme medicin ved at springe de 4 pumper over i 'Trin 5: Prime Nasal Spray Device'?
Svar: Ingen springer over de 4 pumper for at prime nasal spray -enhed kan resultere i, at du ikke får din korrekte dosis medicin.
Spestion: Da jeg først pumpede næsesprayenheden til Prime, syntes intet at ske. Hvorfor?
Svar: Formålet med priming er at bringe medicinen op til spidsen af dysen. Selvom du muligvis ikke ser eller hører noget på din første pumpe eller to, vil pumpehandlingen bevæge medicinen fra glashætteglasset gennem indersiden af næsesprayenheden og ind i dysen. Du skal se en spray ved dit fjerde pumpeforsøg. Altid prime ved at pumpe nøjagtigt 4 gange inden dosering.
Spørgsmål: Kan jeg genbruge næsesprayenheden med et nyt glashætteglas?
Svar: Nothe nasal spray-enhed er kun til engangsbrug og skal smides væk, når du er lukket (1 spray i hver næsebor). Dette skyldes, at enheden kan tilstoppe. Efter dosering af glasset hætteglas skruet fast på nasal spray-enhed og kast den samlede nasale sprayenhed i papirkurven. Genbrug ikke nogen del af produktet.
Spørgsmål: Kan jeg bruge den medicin, der forbliver i glashætteglasset til en senere dosis?
Svar: Det er, selvom det er nrmal for noget medicin at forblive i glashætteglasset, kan det ikke bruges til senere dosering. Enhver rester vil blive ineffektiv.
Spørgsmål: Hvad sker der, hvis jeg Sparay mere end én gang i den samme næsebor?
Svar: En komplet og korrekt dosis er en spray ind i hver næsebor. Dosis ikke i dig anden næsebor, hvis du allerede sprøjtede to gange i en næsebor. Tal til din sundhedsudbyder, hvis du har moderat til svær irritation i din næse eller ændringer i lugt.
Spørgsmål: Hvor hurtigt kan jeg tage en anden dosis, hvis jeg ikke får lettelse fra min migræne?
Svar: Du kan tage en anden dosis AR mindst 1 time efter din første dosis, hvis dine symptomer fortsætter. Gør ikke Tag mere end 2 doser inden for en 24-timers periode. Gør ikke Tag mere end 3 doser i en 7-dages periode.Please refer to the prescribing information for more information.
Denne brugsanvisning er godkendt af U.S.Food og Drug Administration.




