Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
Anticonvulsiva, andreFinTepla
Resume af lægemiddeloversigt
Hvad er FinTepla?
FinTepla (fenfluramine) er en Anticonvulsant Bruges til behandling af anfald forbundet med Dravet -syndrom hos patienter 2 år og ældre.
Hvad er bivirkninger af FinTepla?
FinTepla
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- Humør- eller adfærdsændringer
- angst
- Panikanfald
- problemer med at sove
- impulsivitet
- Agitation
- fjendtlighed
- aggressioner
- rastløshed
- Hyperaktivitet (mentalt eller fysisk)
- øget depression
- Tanker om selvskading
- brystsmerter
- PUNKING HJERDEBESKRIVNINGER
- Fladere i dit bryst
- åndenød
- Blå farvet hud eller læber
- Hævelse i dine underben
- usædvanlig træthed
- svaghed
- Lightheadedness
- Tab af appetit
- vægttab
- forværring af anfald
- sløret vision
- Tunnelvision
- Øjensmerter eller rødme
- At se haloer omkring lys
- kvalme
- opkast
- Alvorlig hovedpine
- sløret vision
- dunkende i din hals eller ører
- næseblødning
- feber
- sved
- Hallucinationer
- ryster
- Hurtig hjerterytme
- Muskelstivhed
- rykker
- Savnet vækst (hos børn)
- tab af koordinering og
- diarre
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Bivirkninger af FinTepla inkluderer:
- nedsat appetit
- døsighed
- sedation
- sløvhed
- diarre
- forstoppelse
- unormalt ekkokardiogram
- træthed
- Følelse uvel (ubehag)
- svaghed
- Problemer med muskelkoordination
- Balanceforstyrrelse
- Gangforstyrrelse
- øget blodtryk
- Slyngende/overskydende spyt
- feber
- Infektion i øvre luftvejsinfektion
- opkast
- vægttab
- falder og
- Status epilepticus
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; og pludselig svimmelhed letthed eller udlevering;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til FinTepla
Den indledende start- og vedligeholdelsesdosis af FinTepla er 0,1 mg/kg to gange dagligt, hvilket kan øges ugentligt baseret på effektivitet og tolerabilitet.
FinTepla hos børn
Sikkerheden og effektiviteten af FinTepla til behandling af anfald forbundet med Dravet -syndrom er blevet fastlagt hos patienter 2 år og ældre. Sikkerhed og effektivitet af FinTepla hos patienter, der er mindre end 2 år gammel, er ikke blevet fastlagt.
Dystonias og andre ekstrapyramidale symptomer forbundet med metoclopramid er mere almindelige hos pædiatriske patienter end hos voksne. Derudover har nyfødte reducerede niveauer af NADH-Cytochrome B5-reduktase, hvilket gør dem mere modtagelige for methemoglobinæmi til en mulig bivirkning af metoclopramidbrug hos nyfødte.
Hvilke stoffer stoffer eller kosttilskud interagerer med FinTepla?
FinTepla kan interagere med andre lægemidler, såsom:
- Rifampin
- Stiripentol plus clobazam
- Cyproheptadin
- Potent 5-HT1A 5- HT1D 5-HT2A eller 5-HT2C serotonin receptorantagonister og
- Medikamenter over-the-counter medicin eller urtetilskud, der øger serotonin, såsom selektive serotonin genoptagelsesinhibitorer (SSRI'er) serotonin-norepinephrin genoptagelsesinhibitorer (SNRI'er) Tricykliske antidepressiva Monoaminoxidaseinhibitorer
Fortæl din læge alle medicin og kosttilskud, du bruger.
FinTepla under graviditet og amning
Fortæl din læge, hvis du er gravid eller planlægger at blive gravid, før du bruger FinTepla; Det er ukendt, hvordan det ville påvirke et foster. Der er et graviditetseksponeringsregister, der overvåger graviditetsresultater hos kvinder, der udsættes for antiepileptiske stoffer (AED'er), såsom FinTepla under graviditet. Det er ukendt, om FinTepla passerer til modermælk. Kontakt din læge inden amning.
Yderligere oplysninger
Vores FinTepla (Fenfluramine) Oral Solution Civ Bivirkning Drug Center giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.
Dette er ikke en komplet liste over bivirkninger, og andre kan forekomme. Ring til din læge for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Lægemiddelinteraktioner
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
ADVARSEL
Valvulær hjertesygdom og pulmonal arteriel hypertension
Der er en sammenhæng mellem serotonergiske lægemidler med 5-HT2B-receptoragonistaktivitet inklusive fenfluramin (den aktive ingrediens i FinTepla) og valvulær hjertesygdom og pulmonal arteriel hypertension [se ADVARSELS AND PRECAUTIONS ].
Ekkokardiogramvurderinger er påkrævet før under og efter behandling med FinTepla. Fordelene kontra risikoen for at indlede eller fortsætte med FinTepla skal overvejes baseret på ekkokardiogramresultater [se Dosering og administration og ADVARSELS AND PRECAUTIONS ].
På grund af risikoen for valvulær hjertesygdom og pulmonal arteriel hypertension FinTepla er kun tilgængelig gennem et begrænset program under en risikovurderings- og afbødningsstrategi (REMS) kaldet FinTepla REMS [Se ADVARSELS AND PRECAUTIONS ].
Beskrivelse for FinTepla
FinTepla oral opløsning indeholder 2,2 mg/ml fenfluramin svarende til 2,5 mg/ml af hydrochloridsalt.
Den aktive ingrediens fenfluraminhydrochlorid betegnes kemisk som N-ethyl-a-methyl-3- (trifluormethyl) phenethylaminhydrochlorid.
Den strukturelle formel er:
| |
Fenfluraminhydrochlorid er et hvidt til off-white krystallinsk fast stof. PKA for fenfluramin er 10,2.
FinTepla er en klar farveløs opløsning pH 5.
FinTepla indeholder følgende inaktive ingredienser: kirsebærsmag citronsyreethylparaben hydroxyethylcellulose methylparaben kaliumcitrat sucralose og vand.
FinTepla indeholder ingen ingrediens fremstillet af glutenholdigt korn (hvedebyg eller rug).
Anvendelser til FinTepla
FinTepla er indikeret til behandling af anfald forbundet med Dravet Syndrome (DS) og Lennox-Gastaut-syndrom (LGS) hos patienter 2 år og ældre.
Dosering til FinTepla
Vurderinger inden indledningen af FinTepla
Før behandling med FinTepla startes med FinTepla, skal Vurderinger under og efter administration af FinTepla og ADVARSELS AND PRECAUTIONS ].
Doseringsoplysninger
FinTepla skal administreres mundtligt og kan tages med eller uden mad.
Dravet syndrom
- Den indledende start- og vedligeholdelsesdosering for patienter med Dravet -syndrom er 0,1 mg/kg to gange dagligt, hvilket kan øges ugentligt baseret på effektivitet og tolerabilitet. Tabel 1 indeholder den anbefalede titreringsplan, hvis det er nødvendigt.
- Patienter med dravet -syndrom, der ikke er på samtidig stiripentol, der tolererer fininepla ved 0,1 mg/kg to gange dagligt og kræver yderligere reduktion af anfald kan drage fordel af en doseringsstigning op til en maksimal anbefalet vedligeholdelsesdosering på 0,35 mg/kg to gange dagligt (maksimal daglig dosering på 26 mg).
- Patienter med Dravet -syndrom, der tager samtidig stiripentol plus clobazam, der tolererer fininepla ved 0,1 mg/kg to gange dagligt og kræver yderligere reduktion af anfaldet kan drage fordel af en doseringsstigning op til en maksimal anbefalet vedligeholdelsesdosis på 0,2 mg/kg to gange dagligt (maksimal daglig dosering på 17 mg) [se Lægemiddelinteraktioner ].
Lennox-Gastaut syndrom
- Den indledende startdosering for patienter med Lennox-Gastaut-syndrom er 0,1 mg/kg to gange dagligt, hvilket bør øges ugentligt baseret på tolerabilitet. Tabel 1 indeholder den anbefalede titreringsplan.
- Patienter med lennox-gastaut-syndrom, der ikke er på samtidig stiripentol, der tolererer fininepla, bør titreres til den anbefalede vedligeholdelsesdosering på 0,35 mg/kg to gange dagligt (maksimal daglig dosering på 26 mg).
- Patienter med Lennox-Gastaut-syndrom, der tager samtidig stiripentol plus clobazam, der tolererer FinTepla, skal titreres til den anbefalede vedligeholdelsesdosering på 0,2 mg/kg to gange dagligt (maksimal daglig dosering på 17 mg) [se Lægemiddelinteraktioner ].
Tabel 1: FinTepla anbefalet titreringsplan*
| Uden samtidig Stiripentol* | Med samtidig Stiripentol plus clobazam | |||
| Vægtbaseret dosering | Maksimal total daglig dosering ± | Vægtbaseret dosering | Maksimal dosering ± samlet dagligt | |
| Indledende dosering | 0,1 mg/kg to gange dagligt | 26 mg | 0,1 mg/kg to gange dagligt | 17 mg |
| Dag 7 | 0,2 mg/kg to gange dagligt | 26 mg | 0,15 mg/kg to gange dagligt | 17 mg |
| Dag 14 ** | 0,35 mg/kg to gange dagligt | 26 mg | 0,2 mg/kg to gange dagligt | 17 mg |
| * For patienter, der ikke er på samtidig stiripipentol, i hvilken en hurtigere titrering er berettiget, kan dosis øges hver 4. dag. For patienter med DAVET -syndrom kan doseringen øges baseret på klinisk respons på den maksimale anbefalede dosering efter behov. ** For patienter med lennox-gastaut-syndrom dosering bør øges som tolereres for den anbefalede vedligeholdelsesdosis (dvs. dag 14). ± for maksimal dosering med samtidig brug af stærk CYP1A2 eller CYP2D6 -hæmmere hos patienter med alvorlig nedsat nyrefunktion eller hos patienter med leverfunktion Doseringsændringer for patienter med samtidig brug af stærk CYP1A2- eller CYP2D6 -hæmmere (DS og LGS) doseringsmodifikationer til patienter med alvorlig nyrefunktion (DS og LGS) doseringsændringer for patienter med mild moderat og alvorlig levetisk nedsat (DS og LGS) |
Doseringsændringer for patienter med samtidig brug af stærk CYP1A2 eller CYP2D6 -hæmmere (DS og LGS)
For patienter med samtidig brug af FinTepla med en stærk CYP1A2 eller CYP2D6 -hæmmer en maksimal total daglig dosering på 20 mg uden samtidig Sturipentol og 17 mg med samtidig Sturipentol plus clobazam anbefales [se Lægemiddelinteraktioner ].
Doseringsændringer for patienter med alvorlig nedsat nyrefunktion (DS og LGS)
For patienter med alvorlig nedsat nyrefunktion (estimeret glomerulær filtreringshastighed (EGFR) 15 til 29 ml/min/1,73 m 2 ) En maksimal total daglig dosering på 20 mg uden samtidig stiripentol og 17 mg med samtidig Stiripentol plus clobazam anbefales [se Brug i specifikke populationer ].
Doseringsændringer for patienter med mild moderat og alvorlig leverfunktion (DS og LGS)
Se tabel 2 for doseringsjusteringer og anbefalinger til patienter med nedsat leverfunktion [se Brug i specifikke populationer ].
Tabel 2: Fintepla -doseringsændringer og anbefalinger til patienter med hepatisk svækkelse
| Hepatisk nedsat klassificering | Uden samtidig Stiripentol* | Med samtidig Stiripentol plus clobazam |
| Maksimal total daglig dosering | Maksimal total daglig dosering | |
| Mild (Child-Pugh A) | 20 mg | 13 mg* |
| Moderat (Child-Pugh B) | 20 mg | Brug ikke anbefalet |
| Alvorlig (Child-Pugh C) | 17 mg | Brug ikke anbefalet |
| * Titrat som anbefalet [se Doseringsoplysninger |
Vurderinger under og efter administration af FinTepla
For at evaluere for valvulær hjertesygdom og pulmonal arteriel hypertension skal du opnå en ekkokardiogramvurdering hver 6. måned under behandling med FinTepla og 3 til 6 måneder efter den endelige dosis af FinTepla [se ADVARSELS AND PRECAUTIONS ].
Administrationsinstruktioner
En kalibreret måleindretning (enten en 3 ml eller 6 ml oral sprøjte) vil blive leveret af apoteket og anbefales at måle og administrere den foreskrevne dosis nøjagtigt [se Hvor leveret ]. A household teaspoon or tablespoon is not an adequate measuring device og should not be used.
Kasser enhver ubrugt fininepla oral løsning tilbage efter 3 måneders første åbning af flasken eller kasser efter dato på flasken, alt efter hvad der er før.
FinTepla er kompatibel med kommercielt tilgængelige gastriske og nasogastriske fodringsrør.
Seponering af FinTepla
Ved ophør af fininepla skal dosis nedsættes gradvist. Som med alle antiepileptiske lægemidler bør pludselig seponering undgås, når det er muligt for at minimere risikoen for øget anfaldsfrekvens og status epilepticus [se ADVARSELS AND PRECAUTIONS ].
Hvor leveret
Doseringsformularer og styrker
Oral opløsning : 2,2 mg/ml fenfluramin som en klar farveløs kirsebærsmaget væske.
FinTepla Oral opløsning er en klar farveløs kirsebærsmaget væske indeholdende 2,2 mg/ml fenfluramin og leveres i en hvid plastflaske med en barnetresistent lukning som følger:
- Karton indeholdende en 360 ml flaske ( NDC 43376-322-36)
- Karton indeholdende en 30 ml flaske ( NDC 43376-322-30)
Før aflevering af apoteket indsætter en presse-in-flaskeadapter i dispenseringsflasken. Apoteket giver 3 ml eller 6 ml kalibrerede orale doseringssprøjter.
Opbevaring og håndtering
Opbevar FinTepla ved stuetemperatur mellem 20 ° C til 25 ° C (68 ° F til 77 ° F); Udflugter er tilladt mellem 15 ° C til 30 ° C (59 ° F til 86 ° F) [se USP -kontrolleret stuetemperatur].
Køl ikke køleskab eller frys. Opbevar flasken og sprøjten sammen.
Kasser enhver ubrugt del 3 måneder efter først at have åbnet flasken eller kasser efter dato på flasken, alt efter hvad der er før.
Procentdel reduktion fra baseline i drop anfaldsfrekvens
Andel af patienter (%)
Fremstillet til: UCB Inc. Smyrna GA 30080. Revideret: Apr 2025.
Bivirkninger for Fintepla
Følgende klinisk signifikante bivirkninger er beskrevet andetsteds ved mærkning:
- Valvulær hjertesygdom og pulmonal arteriel hypertension [se ADVARSELS AND PRECAUTIONS ]
- Nedsat appetit og nedsat vægt [se ADVARSELS AND PRECAUTIONS ]
- Somnolens sedation og sløvhed [se ADVARSELS AND PRECAUTIONS ]
- Selvmordsadfærd og ideation [se ADVARSELS AND PRECAUTIONS ]
- Tilbagetrækning af antiepileptiske stoffer [se ADVARSELS AND PRECAUTIONS ]
- Serotons syndrom [se ADVARSELS AND PRECAUTIONS ]
- Stigning i blodtrykket [se ADVARSELS AND PRECAUTIONS ]
- Glaukom [se ADVARSELS AND PRECAUTIONS ]
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, kan der ikke sammenlignes bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte med hastigheder i de kliniske forsøg med et andet lægemiddel og muligvis ikke afspejler de satser, der er observeret i praksis.
I kontrollerede og ukontrollerede forsøg hos patienter med Dravet Syndrome (DS) blev 341 patienter behandlet med FinTepla inklusive 312 patienter behandlet i mere end 6 måneder 284 patienter behandlet i mere end 1 år og 138 patienter behandlet i mere end 2 år.
I kontrollerede og ukontrollerede forsøg hos patienter med Lennox-Gastaut-syndrom (LGS) blev 262 patienter behandlet med FinTepla inklusive 219 patienter behandlet i mere end 6 måneder 172 patienter behandlet i mere end 1 år og 127 patienter behandlet i mere end 2 år.
Dravet syndrom
I placebo-kontrollerede forsøg med patienter med DS, der tog samtidig standard for pleje AEDS 122 patienter blev behandlet med FinTepla, og 84 patienter modtog placebo [se Kliniske studier ]. The duration of treatment in these trials was 16 weeks (Undersøgelse 1) or 17 weeks (Undersøgelse 2).
I undersøgelse 1 og undersøgelse 2 var middelalderen 9 år (område 2 til 19 år), og ca. 46% af patienterne var kvindelige og 74% var hvide. Alle patienter modtog mindst en anden AED.
I undersøgelse 1 og undersøgelse 2 var satserne for seponering som et resultat af enhver bivirkning 13% 0% og 7% for patienter behandlet med fininepla 0,7 mg/kg/dag 0,2 mg/kg/dag og 0,4 mg/kg/dag i kombination med stiripentol sammenlignet med henholdsvis 6% for patienter på placebo. Den hyppigste bivirkning, der førte til seponering hos de patienter, der blev behandlet med en hvilken som helst dosis fininepla, var somnolens (3%).
De mest almindelige bivirkninger, der forekom hos patienter behandlet med FinTepla (forekomst mindst 10% og større end placebo) blev reduceret appetitten; Somnolens sedation sløvhed; diarre; forstoppelse; unormalt ekkokardiogram; Træthedsmisbrug astheni; Ataksiabalanceforstyrrelse Gangforstyrrelse; Blodtrykket steg; Slyngende spythypersekretion; pyrexia; øvre luftvejsinfektion; opkast; nedsat vægt; falde; Status epilepticus.
Tabel 4 viser de bivirkninger, der blev rapporteret hos 5% eller flere af patienter behandlet med FinTepla og med en hastighed, der er større end dem på placebo under titrerings- og vedligeholdelsesfaserne i studie 1 og undersøgelse 2.
Tabel 4: Bivirkninger hos 5% eller flere af patienter behandlet med FinTepla og Greater end placebo i placebo-kontrollerede forsøg med Dravet-syndrom (undersøgelse 1 og 2)
| Bivirkning | FinTepla Dose Group | Kombineret placebogruppe (2) | ||
| Undersøgelse 1 | Undersøgelse 2 | |||
| 0,2 mg/kg/dag | 0,7 mg/kg/dag | 0,4 mg/kg/dag (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Nedsat appetit | 23 | 38 | 49 | 8 |
| Somnolens sedation sløv | 26 | 25 | 23 | 11 |
| Unormalt ekkokardiogram (3) | 18 | 23 | 9 | 6 |
| Diarre | 31 | 15 | 23 | 6 |
| Forstoppelse | 3 | 10 | 7 | 0 |
| Træthedsmisbrug astheni | 15 | 10 | 30 | 5 |
| Ataxia Balance Disorder Gangforstyrrelse | 10 | 10 | 7 | 1 |
| Unormal opførsel | 0 | 8 | 9 | 0 |
| Blodtrykket steg | 13 | 8 | 0 | 5 |
| Slyngende spythypersekretion | 13 | 8 | 2 | 0 |
| Hypotoni | 0 | 8 | 0 | 0 |
| Udslæt | 8 | 8 | 5 | 4 |
| Blodprolactin steg | 0 | 5 | 0 | 0 |
| Kulderystelser | 0 | 5 | 2 | 0 |
| Nedsat aktivitet | 0 | 5 | 0 | 1 |
| Dehydrering | 0 | 5 | 0 | 0 |
| Søvnløshed | 0 | 5 | 5 | 2 |
| Pyrexia | 15 | 5 | 21 | 14 |
| Stereotyper | 0 | 5 | 0 | 0 |
| Infektion i øvre luftvejsinfektion | 21 | 5 | 7 | 10 |
| Opkast | 10 | 5 | 5 | 8 |
| Vægten faldt | 13 | 5 | 7 | 1 |
| Croup | 5 | 3 | 0 | 1 |
| Øreinfektion | 8 | 3 | 9 | 5 |
| Gastroenteritis | 8 | 3 | 2 | 0 |
| Øget hjerterytme | 5 | 3 | 0 | 2 |
| Irritabilitet | 0 | 3 | 9 | 2 |
| Rhinitis | 8 | 3 | 7 | 2 |
| Rysten | 3 | 3 | 9 | 0 |
| Urininkontinens | 5 | 3 | 0 | 0 |
| Nedsat blodsukker | 0 | 0 | 9 | 1 |
| Bronchitis | 3 | 0 | 9 | 1 |
| Kontusion | 5 | 0 | 0 | 0 |
| Eksem | 0 | 0 | 5 | 0 |
| Enuresis | 5 | 0 | 0 | 0 |
| Falde | 10 | 0 | 0 | 4 |
| Hovedpine | 8 | 0 | 0 | 2 |
| Laryngitis | 0 | 0 | 5 | 0 |
| Negativisme | 5 | 0 | 0 | 0 |
| Status epilepticus | 3 | 0 | 12 | 2 |
| Urinvejsinfektion | 5 | 0 | 5 | 0 |
| Viral infektion | 0 | 0 | 5 | 1 |
| (1) 0,4 mg/kg/dag was not an intermediate dose. Patients on the 0,4 mg/kg/dag dose were also taking concomitant Stiripentol plus clobazam which increases exposure of FinTepla. (2) Patienter i placebogrupper fra undersøgelser 1 og 2 blev samlet. (3) Bestod af spor og mild mitral regurgitation og spore aorta -regurgitation, der betragtes som fysiologisk |
Lennox-Gastaut syndrom
I det placebo-kontrollerede forsøg med patienter med LGS, der tog samtidig standard for pleje AEDS (undersøgelse 3) 176 patienter blev behandlet med FinTepla, og 87 patienter modtog placebo [se Kliniske studier ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) og 29% of patients were at least 18 years of age 45% of patients were female og 79% were White. All patients were receiving at least one other AED.
Strømmene for seponering som et resultat af enhver bivirkning var 6% og 5% for patienter behandlet med FinTepla 0,7 mg/kg/dag og 0,2 mg/kg/dag sammenlignet med 1% for patienter på placebo. De hyppigste bivirkninger, der førte til seponering hos de patienter, der blev behandlet med enhver dosis af FinTepla, var anfald (2%) og somnolens (2%).
De almindelige bivirkninger, der opstod hos patienter behandlet med FinTepla (forekomst mindst 10% og større end placebo) var diarré; nedsat appetit; træthed; Somnolence; opkast.
Tabel 5 viser de bivirkninger, der blev rapporteret hos 5% eller flere af patienter, der blev behandlet med FinTepla og med en hastighed, der er større end dem på placebo under titrerings- og vedligeholdelsesfaserne i studiet 3.
Tabel 5: Bivirkninger hos 5% eller flere af patienter behandlet med FinTepla og større end placebo i det placebo-kontrollerede forsøg for Lennox Gastaut-syndrom (undersøgelse 3)
| Bivirkning | FinTepla Dose Group | ||
| Undersøgelse 3 | Placebo -gruppe | ||
| 0,2 mg/kg/dag | 0,7 mg/kg/dag | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Nedsat appetit | 20 | 36 | 12 |
| Træthedsmisbrug astheni | 14 | 24 | 16 |
| Somnolens sedation sløv | 12 | 22 | 16 |
| Diarre | 11 | 13 | 5 |
| Forstoppelse | 6 | 9 | 6 |
| Opkast | 14 | 8 | 6 |
| Vægten faldt | 2 | 8 | 2 |
| Infektion i øvre luftvejsinfektion | 8 | 7 | 3 |
| Anfald | 9 | 5 | 7 |
| Irritabilitet | 8 | 3 | 6 |
Ekkokardiografiske sikkerhedsvurderinger af valvulær hjertesygdom og pulmonal arteriel hypertension
Valvulær hjertesygdom og pulmonal arteriel hypertension blev evalueret i placebokontrollerede og åbne udvidelsesundersøgelser via ekkokardiografi i op til 3 år i varighed for 341 DS-patienter og 263 LGS-patienter [se ADVARSELS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation og assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
I disse kliniske studier udviste to patienter med LGS mild aorta -regurgitation (AR), men ingen af patienten havde nogen hjerte -tegn eller symptomer eller bevis for valvulære strukturelle ændringer.
Ingen af patienten havde VHD. Hastighederne for milde AR er i overensstemmelse med dem, der ses i screeningsperioden før behandlingen (3 patienter i LGS og 1 patient i DS kliniske forsøg).
Oplevelse af postmarketing
Følgende bivirkninger er blevet identificeret under postapproval brug af FinTepla. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at pålideligt estimere deres frekvens eller etablere et årsagsforhold til eksponering for lægemidler.
Psykiatriske lidelser : aggression
Lægemiddelinteraktioner for Fintepla
Effekt af andre lægemidler på FinTepla
Stiripentol plus clobazam
Samtidig administration af FinTepla med Stiripentol plus clobazam med eller uden valproat øger fenfluraminplasmakoncentrationer [se Klinisk farmakologi ]. If FinTepla is coadministered with Stiripentol plus clobazam the maximum daily dosage of FinTepla is 0,2 mg/kg to gange dagligt (maximum daily dosage of 17 mg) [see Dosering og administration ].
Stærk CYP1A2 CYP2B6 eller CYP3A -inducere
Samtidig administration af FinTepla med stærke CYP1A2 CYP2B6 eller CYP3A -inducere vil reducere fenfluraminklasmakoncentrationer, hvilket kan sænke effektiviteten af FinTepla [Se Klinisk farmakologi ].
Det anbefales at undgå samtidig administration af stærk CYP1A2 CYP2B6 eller CYP3A -inducere. Hvis samtidig administration af en stærk CYP1A2 CYP2B6 eller CYP3A -inducer med FinTepla er nødvendig med at overvåge patienten for reduceret effektivitet og overveje at øge doseringen af FinTepla efter behov; Imidlertid overstiger ikke den maksimale daglige dosering af FinTepla [se Dosering og administration ].
Hvis en stærk CYP1A2 CYP2B6 eller CYP3A -inducer er afbrudt under vedligeholdelsesbehandling med FinTepla, skal du overveje gradvis reduktion i FinTepla -doseringen til den indgivne dosis, inden indledningen påbegyndes [se ADVARSELS AND PRECAUTIONS ].
Stærke CYP1A2 eller CYP2D6 -hæmmere
Samtidig administration af FinTepla med stærke CYP1A2- eller CYP2D6 -hæmmere vil øge fenfluraminklasmakoncentrationer [se Klinisk farmakologi ]. If FinTepla is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of FinTepla is 20 mg [see Dosering og administration ].
Hvis en stærk CYP1A2- eller CYP2D6 -hæmmer afbrydes under vedligeholdelsesbehandling med FinTepla, skal du overveje gradvis stigning i fininepla -doseringen til den anbefalede dosis uden CYP1A2- eller CYP2D6 -hæmmere; Imidlertid overstiger ikke den maksimale daglige dosering af FinTepla [se Dosering og administration ].
Hvis FinTepla er coadministreret med Stiripentol og en stærk CYP1A2 eller CYP2D6 -hæmmer ikke overstiger den maksimale daglige dosering af FinTepla på 17 mg [se Dosering og administration ].
Effekter af serotoninreceptorantagonister
Cyproheptadin og potent 5-HT1A 5-HT1D 5-HT2A og 5-HT2C serotoninreceptorantagonister kan reducere effektiviteten af FinTepla. Hvis cyproheptadin eller potent 5-HT1A 5-HT1D 5-HT2A eller 5-HT2C serotoninreceptorantagonister samtidig administreres med FinTepla-patienter, skal overvåges korrekt.
Serotonergiske lægemidler
Samtidig administration af FinTepla og lægemidler (f.eks. SSRIS SNRIS TCAS MAO-hæmmere Trazodon osv.) Over-the-counter medicin (f.eks ADVARSELS AND PRECAUTIONS ]. Concomitant use of FinTepla is contraindicated within 14 days of taking MAOIs. Use FinTepla with caution in patients taking other medications that increase serotonin.
Advarsler for FinTepla
Inkluderet som en del af 'FORHOLDSREGLER' Afsnit
Forholdsregler for FinTepla
Valvulær hjertesygdom og pulmonal arteriel hypertension
FinTepla can cause valvular heart disease (VHD) og pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in FinTepla) og valvular heart disease og pulmonary arterial hypertension. Although no patients receiving FinTepla developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS og LGS of up to 3 years in duration cases of valvular heart disease og pulmonary arterial hypertension have been reported during use of FinTepla in the postmarketing setting [see Boksadvarsel og Bivirkninger ].
På grund af denne risiko, der er hjertets overvågning, kræves inden behandling under behandling og efter behandling med FinTepla afsluttes. Hjerteovervågning via ekkokardiogram kan identificere bevis for valvulær hjertesygdom og pulmonal arteriel hypertension, inden en patient bliver symptomatisk, der hjælper med tidlig påvisning af disse tilstande.
Overvågning
Før patienterne starter skal patienter gennemgå et ekkokardiogram for at evaluere for valvulær hjertesygdom og pulmonal arteriel hypertension.
Ekkokardiogrammer skal gentages hver 6. måned og en gang 3-6 måneder efter behandling med FinTepla.
Forbeskrivelsen skal overveje fordelene kontra risikoen for at indlede eller fortsætte behandling med FinTepla, hvis der observeres nogen af følgende tegn via ECHO:
- Valvulær abnormitet eller ny abnormitet via ekkokardiogram.
- VHD som indikeret af mild eller større aorta -regurgitation eller moderat eller større mitral regurgitation med yderligere egenskaber ved VHD (f.eks. Ventilfortykning eller restriktiv ventilbevægelse).
- PAH som indikeret af forhøjet højre hjerte/lungearterietryk (PASP> 35 mm Hg).
FinTepla is available only through a restricted program under a REMS [see FinTepla REMS Program ].
FinTepla REMS Program
FinTepla is available only through a restricted distribution program called the FinTepla REMS program because of the risk of valvular heart disease og pulmonary arterial hypertension [see Valvulær hjertesygdom og pulmonal arteriel hypertension ].
Bemærkelsesværdige krav fra FinTepla REMS -programmet inkluderer:
- Rekressører skal certificeres ved at tilmelde dig FinTepla REMS -programmet.
- PRESCRICREERS skal rådgive patienter, der får FinTepla om risikoen for valvulær hjertesygdom og pulmonal arteriel hypertension, hvordan man genkender tegn og symptomer på valvulær hjertesygdom og pulmonal arteriel hypertension behovet for baseline (forbehandling) og periodisk hjerteovervågning via echocardiogram under finepla -behandling og hjerteovervågning efter fintepla -behandling.
- Patienter skal tilmelde sig REMS -programmet og overholde løbende overvågningskrav [se Valvulær hjertesygdom og pulmonal arteriel hypertension ].
- Apoteket skal certificeres ved at tilmelde sig REMS -programmet og skal kun dispensere til patienter, der er autoriseret til at modtage FinTepla.
- Grossister og distributører må kun distribuere til certificerede apoteker.
Yderligere information er tilgængelig på www.finteplarems.com eller telefonisk på 1-877-964-3649.
Nedsat appetit og nedsat vægt
FinTepla can cause decreases in appetite og weight. In placebo-controlled studies for DS (Undersøgelse 1 og Undersøgelse 2 combined) approximately 37% of patients treated with FinTepla reported as an adverse reaction nedsat appetit og approximately 9% reported nedsat vægt as compared to 8% og 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Undersøgelse 3) approximately 28% of patients treated with FinTepla reported as an adverse reaction nedsat appetit og approximately 5% reported nedsat vægt as compared to 15% og 2% respectively of patients on placebo [see Bivirkninger ]. By the end of the controlled studies 19% (Studies 1 og 2 combined) of DS patients og 7% (Undersøgelse 3) of LGS patients treated with FinTepla had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Undersøgelse 1 og 2) og 0% (Undersøgelse 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on FinTepla 0,7 mg/kg/dag (Undersøgelse 1) 19% of patients on FinTepla 0,4 mg/kg/dag in combination with stiripentol (Undersøgelse 2) og 13% of patients taking FinTepla 0,2 mg/kg/dag (Undersøgelse 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on FinTepla 0,7 mg/kg/dag (Undersøgelse 3) og 6% of patients on FinTepla 0,2 mg/kg/dag (Undersøgelse 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS og most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with FinTepla should be carefully monitored. Weight should be monitored regularly during treatment with FinTepla og dose modifications should be considered if a decrease in weight is observed.
Somnolens sedation og sløvhed
FinTepla can cause somnolence sedation og sløvhed. In controlled studies for DS (Undersøgelse 1 og Undersøgelse 2 combined) the incidence of somnolence sedation og sløvhed was 25% in patients treated with FinTepla compared with 11% of patients on placebo. In the controlled study for LGS (Undersøgelse 3) the incidence of somnolence sedation og sløvhed was 19% in patients treated with FinTepla compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Bivirkninger ].
Andet centralnervesystem (CNS) depressiva inklusive alkohol kunne styrke disse effekter af FinTepla. Rekressører bør overvåge patienter for somnolens og sedation og bør rådgive patienter om ikke at køre eller betjene maskiner, før de har fået tilstrækkelig erfaring på FinTepla til at måle, om det påvirker deres evne til at køre eller betjene maskiner.
Selvmordsadfærd og ideation
Antiepileptiske lægemidler (AED'er) inklusive FinTepla øger risikoen for selvmordstanker eller adfærd hos patienter, der tager disse lægemidler til enhver indikation. Patienter, der behandles med en AED for enhver indikation, skal overvåges for fremkomsten eller forværring af depression selvmordstanker eller adfærd eller eventuelle usædvanlige ændringer i humør eller adfærd.
Samlede analyser af 199 placebokontrollerede kliniske forsøg (mono- og supplerende terapi) på 11 forskellige AED'er, der ikke omfattede FinTepla, viste, at patienter, der blev randomiseret til en af AED'erne, havde cirka dobbelt så stor risiko (justeret relativ risiko 1,8 95% CI: 1,2 2,7) af selvmåling eller adfærd sammenlignet med patienter, der blev tilfældigt til placering af placering. I disse forsøg, der havde en median behandlingsvarighed på 12 uger på den estimerede forekomst af selvmordsadfærd eller ideation blandt 27863 AED-behandlede patienter, var 0,43% sammenlignet med 0,24% blandt 16029 placebo-behandlede patienter, der repræsenterede en stigning på ca. et tilfælde af selvmordstænkning eller adfærd for hver 530 patienter behandlet. Der var fire selvmord hos lægemiddelbehandlede patienter i forsøgene og ingen i placebo-behandlede patienter, men antallet er for lille til at tillade enhver konklusion om lægemiddeleffekt på selvmord.
Den øgede risiko for selvmordstanker eller adfærd med AED'er blev observeret så tidligt som 1 uge efter start af lægemiddelbehandling med AED'er og vedvarede i den vurderede behandlings varighed. Fordi de fleste forsøg, der var inkluderet i analysen, ikke strækkede sig ud over 24 uger, kunne risikoen for selvmordstanker eller adfærd ud over 24 uger ikke vurderes.
Risikoen for selvmordstanker eller adfærd var generelt konsistent blandt lægemidler i de analyserede data. Fundet af øget risiko med AED'er med forskellige handlingsmekanismer og på tværs af en række indikationer antyder, at risikoen gælder for alle AED'er, der bruges til enhver indikation. Risikoen varierede ikke væsentligt efter alder (5-100 år) i de analyserede kliniske forsøg. Tabel 3 viser absolut og relativ risiko ved indikation for alle evaluerede AED'er.
Tabel 3: Risiko for selvmordstanker eller adfærd ved indikation for antiepileptiske lægemidler i den samlede analyse
| Tegn | Placebo -patienter med begivenheder pr. 1000 patienter | Lægemiddelpatienter med begivenheder pr. 1000 patienter | Relativ risiko: Forekomst af begivenheder hos lægemiddelpatienter/ forekomst hos placebo -patienter | Risikoforskel: Yderligere lægemiddelpatienter med begivenheder pr. 1000 patienter |
| Epilepsi | 1.0 | 3.4 | 3.5 | 2.4 |
| Psykiatrisk | 5.7 | 8.5 | 1.5 | 2.9 |
| Andre | 1.0 | 1.8 | 1.9 | 0.9 |
| Total | 2.4 | 4.3 | 1.8 | 1.9 |
Den relative risiko for selvmordstanker eller adfærd var højere i kliniske forsøg hos patienter med epilepsi end i kliniske forsøg hos patienter med psykiatriske eller andre tilstande, men de absolutte risikoforskelle var ens for epilepsi og psykiatriske indikationer.
Enhver, der overvejer at ordinere FinTepla eller enhver anden AED, skal afbalancere risikoen for selvmordstanker eller adfærd med risikoen for ubehandlet sygdom. Epilepsi og mange andre sygdomme, som AED'er er ordineret, er i sig selv forbundet med sygelighed og dødelighed og en øget risiko for selvmordstanker og adfærd. Hvis selvmordstanker og adfærd dukker op under behandlingen, skal du overveje, om fremkomsten af disse symptomer hos en given patient kan være relateret til den sygdom, der behandles.
Tilbagetrækning af antiepileptiske stoffer
Som med de fleste AED'er bør FinTepla generelt trækkes tilbage gradvist på grund af risikoen for øget anfaldsfrekvens og status epilepticus. Hvis der er behov for tilbagetrækning på grund af en alvorlig bivirkning, kan der overvejes hurtig seponering.
Serotons syndrom
Serotonin syndrome a potentially life-threatening condition may occur with FINTEPLA particularly with concomitant administration of FINTEPLA with other serotonergic drugs including but not limited to selective serotonin-norepinephrine reuptake inhibitors (SNRIs) selective serotonin reuptake inhibitors (SSRIs) tricyclic Antidepressiva (TCAS) bupropion triptans kosttilskud (f.eks. St. Johns Wort tryptophan) lægemidler, der forringer metabolismen af serotonin (inklusive monoaminoxidaseinhibitorer [Maois], som er kontraindiceret med FinTepla [se Kontraindikationer ] Dextromethorphan Lithium tramadol og antipsykotika med serotonerg agonistaktivitet. Patienter skal overvåges for fremkomsten af tegn og symptomer på serotonin -syndrom, som inkluderer ændringer i mental status (f.eks. Agitation Hallucinations Coma) autonom ustabilitet (f.eks. Tachycardia labile blodtrykshypertermi) neuromuskulære tegn (f.eks. Hyperrefleksi) og/eller gastrointestinalsymptomer (f.eks. NAUSEASE (f.eks. DIOPREFLEXIA. Hvis serotoninsyndrom mistænkes for behandling med FinTepla, skal der straks stoppes, og symptomatisk behandling skal startes.
Stigning i blodtrykket
FinTepla can cause an increase in blood pressure [see Bivirkninger ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving FinTepla developed a hypertensive crisis. Monitor blood pressure in patients treated with FinTepla.
Glaukom
Fenfluramin kan forårsage mydriasis og kan udfælde vinkellukning glaukom . Overvej at afbryde behandlingen med FinTepla hos patienter med akut fald i synsskarphed eller okulær smerte.
Oplysninger om patientrådgivning
Rådgiv patienten om at læse den FDA-godkendte patientmærkning ( Medicin vejledning og Instructions for Use ).
Administrationsoplysninger
Rådgiv patienter, der er ordineret FinTepla til at bruge de orale doseringssprøjter leveret af apoteket [se Dosering og administration og Brug til brug ]. Instruct patients to discard any unused FinTepla 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Hvor leveret ].
Valvulær hjertesygdom og pulmonal arteriel hypertension
Rådgiv patienter om, at hjerteovervågning skal udføres ved hjælp af ekkokardiografi for at overvåge for alvorlige hjerteklodseændringer eller højt blodtryk i arterierne i lungerne [se ADVARSELS AND PRECAUTIONS ].
FinTepla REMS Program
FinTepla is available only through a restricted program called the FinTepla REMS program [see ADVARSELS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- Patienter skal tilmelde sig programmet og overholde løbende krav til overvågning af ekkokardiogram [se ADVARSELS AND PRECAUTIONS ].
FinTepla is only prescribed by certified health care providers og only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number og website for information on how to obtain the product [see ADVARSELS AND PRECAUTIONS ].
Nedsat appetit og nedsat vægt
Rådgive patienter, der reducerede appetitten, er hyppigt under behandling med FinTepla, hvilket kan forårsage fald i vægt [se ADVARSELS AND PRECAUTIONS ].
Somnolens sedation og sløvhed
Informer patienter om, at FinTepla kan forårsage somnolens sedation og sløvhed. FORSIGTIGT PATIAGER OM BETJENINGSFARMERINGSMASKERIER INKLUDERET MOTORKØRER, TIL DE ER RYSE FORSIGTIGE, at FinTepla ikke påvirker dem negativt (f.eks. Virkningstænkning eller motoriske evner) [se ADVARSELS AND PRECAUTIONS ].
Selvmordstænkning og adfærd
Rådgiver patienter deres plejere og deres familier om, at antiepileptiske lægemidler kan øge risikoen for selvmordstanker og adfærd og rådgive dem om at være opmærksomme på fremkomsten eller forværring af symptomer på depression eventuelle usædvanlige ændringer i humør eller adfærd eller fremkomsten af selvmordstankers adfærd eller tanker om selvharm. Instruer patienter plejere og familier til at rapportere adfærd af bekymring for sundhedsudbydere [se ADVARSELS AND PRECAUTIONS ].
Tilbagetrækning af antiepileptiske stoffer (AEDs)
Rådgiver patienter om ikke at afbryde brugen af FinTepla uden at konsultere deres sundhedsudbyder. FinTepla bør normalt gradvist trækkes tilbage for at reducere potentialet for øget anfaldsfrekvens og status epilepticus [se Dosering og administration og ADVARSELS AND PRECAUTIONS ].
Serotons syndrom
Informer patienter om risikoen for serotoninsyndrom, som kan være livstruende. Rådgiv patienter om tegn og symptomer på serotonin-syndrom, og at visse medicinske medicin og urtetilskud kan øge denne risiko [se ADVARSELS AND PRECAUTIONS ].
Stigning i blodtrykket
Informer patienter om, at FinTepla kan forårsage en stigning i blodtrykket [se ADVARSELS AND PRECAUTIONS ].
Glaukom
Informer patienter om, at FinTepla kan forårsage mydriasis og kan udfælde vinkellukning glaukom.
Instruer patienter om at kontakte deres sundhedsudbyder, hvis de har nogen akutte fald i synsskarphed eller okulær smerte [se ADVARSELS AND PRECAUTIONS ].
Graviditetsregister
Rådgive patienter om at underrette deres sundhedsudbyder, hvis de bliver gravide eller har til hensigt at blive gravide under FinTepla -terapi. Opmuntrer kvinder, der tager FinTepla til at tilmelde sig det nordamerikanske antiepileptiske stof (NAAED) graviditetsregister, hvis de bliver gravide.
Dette register indsamler oplysninger om sikkerheden ved antiepileptiske lægemidler under graviditet [se Brug i specifikke populationer ].
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
Carcinogenese
Oral administration af fenfluramin til Tg.Rash2-mus (0 4,3 13,0 34,6 eller 51,8 mg/kg/dag) i 26 uger og til mandlige og kvindelige rotter (0 0,9 2,2 eller 6,9 mg/kg/dag) i henholdsvis 89 og 97 uger resulterede ikke i bevis for lægemiddelinducerede tumorer i enten art. Hos rotter er plasmaeksponeringer (AUC) af fenfluramin og norfenfluramin (den største metabolit) i den højeste testede dosis ca. 5 og 11 gange dem hos mennesker ved den maksimale anbefalede humane dosis (MRHD) på 26 mg/dag.
Mutagenese
Fenfluramin var negativ i en In vitro Bakteriel mutation (Ames) assay og en forgæves Micronucleus og Comet Assay hos rotter.
Værdiforringelse af fertiliteten
Oral administration of fenfluramine (0 3.0 6.9 or 17.3 mg/kg/day) to male and female rats prior to and throughout mating and continuing in females to day 7 of gestation resulted in a decrease in fertility and increases in abnormal sperm and epithelial vacuolation of the epididymis at the highest dose tested and altered estrous cyclicity decreased corpora lutea and Implantationer og øget embryoletalitet i midten og høj dosis. Disse doser var forbundet med forældremæssige toksicitet. Doserne uden virkning for bivirkninger på fertilitet og reproduktiv ydeevne hos rotter (NULL,9 og 3,0 mg/kg/dag hos mænd og kvinder) var henholdsvis forbundet med henholdsvis plasma-fenfluramineksponeringer (AUC) ca. 3 og 0,6 gange og Norfenfluramine eksponeringer tilnærmelsesvis ca. 5 og 3 gange dem i HUMANS ved MRHD.
Brug i specifikke populationer
Graviditet
Graviditet Exposure Registry
Der er et graviditetseksponeringsregister, der overvåger graviditetsresultater hos kvinder, der udsættes for antiepileptiske stoffer (AED'er), såsom FinTepla under graviditet. Opmuntr kvinder, der tager FinTepla under graviditet til at tilmelde sig det nordamerikanske antiepileptiske lægemiddel (NAAED) graviditetsregister ved at ringe til det gratis nummer 1-888-233-2334 eller besøge https://www.aedpregnancyregistry.org.
Risikooversigt
Der er ingen data om FinTepla -brug hos gravide kvinder. Tilgængelige data fra epidemiologiske undersøgelser med fenfluramin eller dexfenfluramin er utilstrækkelige til at evaluere for en medikamentassocieret risiko for større fødselsdefekter spontanabort eller andre ugunstige moderlige eller føtalesultater. FinTepla kan forårsage nedsat appetit og nedsat vægt [se ADVARSELS AND PRECAUTIONS ]; Monitor for tilstrækkelig vægtøgning under graviditet. I dyreforsøg, som administration af fenfluramin i hele organogenese (rotte og kanin) eller gennem drægtighed og amning (rotte) resulterede i bivirkninger på udviklingen (føtal misdannelsesembryofetal- og afkomdødelighed og vækstdæmpning) i tilstedeværelsen af moderlig toksicitet ved klinisk relevante moderlige plasma -niveauer af fenfluramin og dens større aktive metabolit (se på Data ).
Den estimerede baggrundsrisiko for store fødselsdefekter og spontanabort for den angivne befolkning er ukendt. Alle graviditeter har en baggrundsrisiko for fødselsdefekt tab eller andre ugunstige resultater. I den amerikanske generelle befolkning er den estimerede baggrundsrisiko for større fødselsdefekter og spontanabort i klinisk anerkendte graviditeter henholdsvis 2 til 4% og 15 til 20%.
Data
Dyredata
Oral administration af fenfluramin (0 4,5 8,6 eller 34,6 mg/kg/dag) til gravide rotter under organogenese resulterede i nedsat føtal kropsvægt og markerede stigninger i føtal misdannelser (eksterne visceral og knogler) ved den højeste dosis testede, som var forbundet med maternal toksicitet. Ved dosis uden virkning (NULL,6 mg/kg/dag) for bivirkninger på embryofetaludvikling hos rotter var mødreplasmaeksponeringer (AUC) af fenfluramin og norfenfluramin (den største metabolit) ca. 2 og 5 gange dem, der var hos mennesker på den maksimale anbefalede humane dosis (MRHD) på 26 mg/dag.
Oral administration af fenfluramin (0 4,3 8,6 13,0 mg/kg/dag) til gravide kaniner i hele organogenese resulterede i øget embryofetaldødelighed i alle doser og stigninger i føtal misdannelser (ekstern og skelet) ved den højeste dosis testet, hvilket var forbundet med moderens toksicitet. En dosis uden adverseffekt til bivirkninger på embryofetaludvikling hos kaniner blev ikke identificeret. Ved den laveste dosis, der blev testet hos kaniner (NULL,3 mg/kg/dag), var moderens plasmaeksponeringer af fenfluramin og norfenfluramin lavere end dem hos mennesker ved MRHD.
Oral administration af fenfluramin (0 4,3 86 eller 34,6 mg/kg/dag) til kvindelige rotter i hele drægtighed og amning resulterede i markante stigninger i dødfødte hvalpe og neonatal afkom dødsfald i den højeste dosis, der blev testet og forsinket vækst og refleksudvikling i den forordningsperiode i alle doser. Mødre kropsvægtforøgelse blev reduceret i alle doser under graviditet og ved de to højeste doser under amning. En dosis uden virkning for bivirkninger på før- og postnatal udvikling hos rotter blev ikke bestemt. Ved den laveste dosis, der blev testet hos rotter (NULL,3 mg/kg/dag), var moderens plasmaeksponeringer af fenfluramin og norfenfluramin ca. 0,5 og 3 gange dem hos mennesker ved MRHD.
Amning
Risikooversigt
Der er ingen data om tilstedeværelsen af fenfluramin eller dets metabolitter i human mælk virkningerne på det ammede spædbarn eller virkningerne på mælkeproduktionen.
De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med mødrenes kliniske behov for FinTepla og eventuelle bivirkninger på det ammede spædbarn fra FinTepla eller fra den underliggende moderlige tilstand.
Kvinder og mænd med reproduktivt potentiale
Infertilitet
I dyreforsøg resulterede oral administration af fenfluramin i bivirkninger for reproduktive virkninger hos mænd og kvinder i klinisk relevante doser i nærvær af forældremæssig toksicitet [se Ikke -klinisk toksikologi ].
Pædiatrisk brug
Sikkerheden og effektiviteten af FinTepla til behandling af anfald, der er forbundet med DS og LGS, er blevet fastlagt hos patienter 2 år og ældre.
Anvendelse af fininepla til behandling af anfald forbundet med DS hos patienter 2 år og ældre understøttes af to randomiserede dobbeltblinde placebokontrollerede forsøg hos 202 patienter 2 til 18 år. Brug af FinTepla til behandling af anfald, der er forbundet med LGS, understøttes af en randomiseret dobbeltblind placebokontrolleret undersøgelse hos 263 patienter i alderen 2 til 35 år inklusive 187 patienter mindre end 18 år [se Boksadvarsel ADVARSELS AND PRECAUTIONS Bivirkninger og Kliniske studier ].
FinTepla can cause decreases in appetite og weight. The growth of pediatric patients treated with FinTepla should be carefully monitored.
Sikkerhed og effektivitet hos patienter, der er mindre end 2 år gammel, er ikke fastlagt.
Juvenile dyredata
Oral administration af fenfluramin (0 3,0 78 eller 17,3 mg/kg/dag) til unge rotter i 10 uger, der startede på postnatal dag 7, resulterede i reduceret kropsvægt og neurobehaviorale ændringer (nedsat lokomotorisk aktivitet og læring og hukommelsesunderskud) ved alle testede doser. Neurobehaviorale effekter vedvarede, efter at dosering blev afbrudt. Knoglestørrelse blev reduceret i midten og høje doser; Hjernestørrelse blev reduceret i den højeste dosis. Delvis eller komplet bedring blev set for disse slutpunkter. En dosis uden virkning til postnatal udviklingstoksicitet blev ikke identificeret. Den laveste testede dosis (NULL,0 mg/kg/dag) var forbundet med plasma -fenfluramineksponeringer (AUC) mindre end i mennesker ved den maksimale anbefalede humane dosis (MRHD) på 26 mg/dag og norfenfluramin (metabolit) eksponeringer (AUC) ca. 2 gange, der i mennesker ved MRHD.
Geriatrisk brug
Kliniske undersøgelser af FinTepla til behandling af DS eller LGS inkluderede ikke patienter 65 år og derover for at afgøre, om de reagerer forskelligt fra yngre patienter. Generelt skal valg af dosis for en ældre patient være forsigtig, der normalt starter ved den lave ende af doseringsområdet, der afspejler den større hyppighed af nedsat leverrenal eller hjertefunktion og af samtidig sygdom eller anden lægemiddelterapi.
Tegn og symptomer på phenobarbital overdosis
Nedskærmning af nyren
Hos patienter med estimeret glomerulær filtreringshastighed (EGFR) 15 til 29 ml/min/1,73 m 2 Overskrid ikke den maksimale daglige dosering af fininepla på 20 mg. Hos patienter med EGFR 15 til 29 ml/min/1,73m 2 og concomitant stiripentol use do not exceed the maximum daily dosage of FinTepla of 17 mg [see Dosering og administration og Klinisk farmakologi ].
FinTepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Leverskrivning i leveren
Kombinerede molære eksponeringer af fenfluramin og norfenfluramin blev forøget hos personer med forskellige grader af leverfunktion (børnepugh klasse A B og C) nødvendig for en doseringsjustering hos disse patienter [se Dosering og administration og Klinisk farmakologi ].
Overdoseringsoplysninger til FinTepla
Overdosis er ikke observeret i FinTepla klinisk forsøgsprogram. Imidlertid er der rapporteret om overdosis af fenfluramin, den aktive ingrediens i FinTepla er rapporteret i højere doser end dem, der er inkluderet i det kliniske forsøgsprogram. Nogle af sagerne var dødelige. Begivenheder rapporteret efter overdosis inkluderer mydriasis takykardi skylning af rystelser/rykning/muskelspasmer agitation/rastløshed/angst øget muskel tone/strenghed/opisthotonos respiratorisk nød eller fiasko og beslaglæggelse. Anfaldskoma og kardiorespiratorisk arrestation blev rapporteret i de fleste af de dødelige overdoser.
Der er ingen tilgængelig specifik modgift mod overdoseringsreaktioner fra FinTepla. I tilfælde af overdosering af standard medicinsk praksis til håndtering af overdosering af medikamenter bør anvendes. En tilstrækkelig luftvejsoxygenation og ventilation bør sikres; Overvågning af hjerterytme og måling af vital tegn anbefales. Et certificeret giftkontrolcenter skal kontaktes for opdaterede oplysninger om styring af overdosering med FinTepla.
Kontraindikationer for FinTepla
FinTepla is contraindicated in patients with:
- Overfølsomhed over for fenfluramin eller nogen af excipienserne i FinTepla [se BESKRIVELSE ]
- Samtidig brug eller inden for 14 dage efter administrationen af monoaminoxidaseinhibitorer på grund af en øget risiko for serotoninsyndrom [se ADVARSELS AND PRECAUTIONS ]
Klinisk farmakologi for Fintepla
Handlingsmekanisme
Den nøjagtige mekanisme, hvormed fenfluramin udøver sine terapeutiske virkninger i behandlingen af anfald forbundet med Dravet-syndrom og Lennox-Gastaut-syndrom, er ukendt. Fenfluramin og metaboliten Norfenfluramine udviser agonistaktivitet ved serotonin 5-HT2-receptorer. Der er en sammenhæng mellem serotonergiske medikamenter med 5-HT2B-receptoragonistaktivitet inklusive fenfluramin og norfenfluramin og valvulær hjertesygdom og pulmonal arteriel hypertension.
Farmakodynamik
Hjertelektrofysiologi
Ved en dosis 4 gange forlængede den maksimale anbefalede dosis FinTepla ikke QT -intervallet, når de blev testet i en voksenpopulation.
Farmakokinetik
Farmakokinetikken af fenfluramin og norfenfluramin blev undersøgt hos raske forsøgspersoner hos pædiatriske patienter med DS og hos pædiatriske og voksne patienter med LG'er. Den stabile statiske eksponering (CMAX og AUC) af fenfluramin var lidt større end dosisproportional i forhold til dosisområdet fra 13 til 51,8 mg to gange dagligt fenfluramin (dvs. 1 til 4 gange den maksimale anbefalede dosis). Hos pædiatriske patienter med DS, der modtog fininepla 0,7 mg/kg/dag op til en total daglig dosis på 26 mg fenfluramin Det geometriske gennemsnitlige steady-state fenfluramin (variationskoefficient) var 68,0 (41%) Ng/ml og AUC0-24H var 1390 (44%) ng*H/ml.
Absorption
Fenfluramine har en tid til maksimal plasmakoncentration (TMAX) på 3 til 5 timer ved stabil tilstand. Den absolutte biotilgængelighed af fenfluramin er ca. 68-74%. Der var ingen virkning af mad på farmakokinetikken af fenfluramin eller norfenfluramin.
Fordeling
Det geometriske middelværdi (CV%) tilsyneladende mængden af distribution (VZ/F) af fenfluramin er 11,9 (NULL,5%) L/kg efter oral administration af FinTepla hos raske forsøgspersoner. Fenfluramin er 50% bundet til humane plasmaproteiner In vitro og binding is independent of drug concentrations.
Eliminering
Eliminationshalveringstiden for fenfluramin var 20 timer, og det geometriske middelværdi (CV%) clearance (CL/F) var 24,8 (29%) L/H efter oral administration af FinTepla hos raske forsøgspersoner.
Metabolisme
Over 75% af fenfluramin metaboliseres til norfenfluramin inden eliminering primært af CYP1A2 CYP2B6 og CYP2D6. Andre CYP -enzymer involveret i mindre grad er CYP2C9 CYP2C19 og CYP3A4/5. Både fenfluramin og norfenfluramin er farmakologisk aktive. Norfenfluramin er yderligere deamineret og oxideret til dannelse af inaktive metabolitter.
Udskillelse
De fleste af en oralt indgivet dosis af fenfluramin (større end 90%) udskilles i urinen som fenfluramin norfenfluramin eller andre metabolitter med fenfluramin og norfenfluramin, der regnskaber for mindre end 25% af det samlede beløb; Mindre end 5% findes i fæces.
Specifikke populationer
Effekten af alder (rækkevidde: 2 til 50 år) køn og race havde ingen klinisk meningsfuld effekt på farmakokinetikken af fenfluramin.
Patienter med nedsat nyrefunktion
I en dedikeret klinisk undersøgelse, der sammenligner farmakokinetikken for en enkelt dosis på 0,35 mg/kg fininepla hos personer med alvorlig nedsat nyrefunktion (EGFR <30 mL/min/1.73m 2 Bestemmet af MDRD) og matchede raske frivillige Cmax og AUC0-INF for fenfluramin steg med henholdsvis 20% og 88% og Cmax og AUC0-INF for Norfenfluramine steg med henholdsvis 13% og 21% hos personer med alvorlig nyrefunktion [se Brug i specifikke populationer ].
FinTepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 (bestemt af MDRD). Det vides ikke, om fenfluramin eller norfenfluramin er dialyzbart.
Patienter med nedsat leverfunktion
I en undersøgelse, der sammenligner farmakokinetikken i en enkelt dosis på 0,35 mg/kg fininepla hos personer med mild moderat eller svær levernedsættelse (børnepugh-klasse A B eller C), og personer med normal leverfunktion AUC0-T af Fenfluramine steg med henholdsvis 95% 113% og 185% i personer med mild moderat og svær HEPATIC-nedsættelse. Cmax af fenfluramin steg med henholdsvis 19% 16% og 29% hos personer med mild moderat og alvorlig leverfunktion. AUC0-T af Norfenfluramine steg med 18% i mild leverfunktion 4% i moderat leverfunktion og faldt med 11% i alvorlig nedskrivning i leveren. Cmax af Norfenfluramine faldt med henholdsvis 21% 36% og 45% hos personer med mild moderat og alvorlig leverfunktion. Kombineret molær AUC0-T af fenfluramin og norfenfluramin steg med henholdsvis 55% 56% og 82% hos personer med mild moderat og alvorlig leverfunktion. Kombineret molær Cmax af fenfluramin og norfenfluramin steg med henholdsvis 7,5% 1,3% og 8% hos personer med mild moderat og alvorlig leverfunktion. Den maksimale daglige dosering af FinTepla skal reduceres hos patienter med mild leverfunktion med/uden Stiripentol plus clobazam. Den maksimale daglige dosering af FinTepla skal reduceres hos patienter med moderat eller alvorlig leverfunktion uden Stiripentol plus clobazam [se Dosering og administration og Brug i specifikke populationer ].
Lægemiddelinteraktionsundersøgelser
Kliniske studier
Effekt af en enkelt dosis af Stiripentol Clobazam og Valproinsyre -kombination
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination in healthy volunteers increased the AUC0-inf of fenfluramine by 69% and the Cmax by 18% and decreased the AUC0-72 hours of norfenfluramine by 41% and the Cmax by 42% as compared to FINTEPLA administreret alene.
Effekt af stabil tilstand Stiripentol plus clobazam med eller uden valproat
Fenfluramin farmakokinetiske data blev indsamlet fra patienter efter at have modtaget flere fenfluraminadministrationer i undersøgelse 1 såvel som undersøgelse 2. Population farmakokinetisk modellering og simulering blev anvendt til at vurdere virkningen af Stiripentol plus clobazam med eller uden valproat på fenfluramin farmakokinetik. Effekten af stiripentol plus clobazam med eller uden valproat på fenfluramin farmakokinetik er større, når FinTepla er i stabil tilstand end for den første dosis af FinTepla. Ved stabil tilstand i patientpopulationen er samtidig administration af 0,1 mg/kg to gange dagligt (NULL,2 mg/kg/dag) maksimalt 17 mg/dag med finepla med Stiripentol plus clobazam med eller uden valproat forventes at resultere i en 166% stigning i fenfluramin AUC0-24 og et 38% fald i norfenfluramin AUC0-24 som 0,2404 mg/kg/dag maksimalt 26 mg/dag FinTepla dosis administreret alene [se Dosering og administration og Lægemiddelinteraktioner ].
Effekt af stabil cannabidiol
Coadministration af en enkelt 0,35 mg/kg dosis fininepla med gentagne doser af cannabidiol øgede AUC0-INF af fenfluramin med 59% og Cmax med 10% og faldt AUC0-INF for Norfenfluramine med 22% og Cmax med 33% sammenlignet med fintepla, der blev administreret alene. Denne interaktion forventes ikke at være klinisk signifikant.
Effekt af stærk CYP1A2 eller CYP2D6 -hæmmere
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with fluvoxamine (a strong CYP1A2 inhibitor) at steady state (50 mg once daily) in healthy volunteers increased the AUC0- inf of fenfluramine by 102% and the Cmax by 22% and decreased the AUC0-inf of norfenfluramine by 22% and the Cmax by 44% as compared til FinTepla administreret alene [se Lægemiddelinteraktioner ].
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with paroxetine (a strong CYP2D6 inhibitor) at steady state (30 mg once daily) in healthy volunteers increased the AUC0-inf of fenfluramine by 81% and the Cmax by 13% and decreased the AUC0-inf of norfenfluramine by 13% and the Cmax by 29% as compared to FinTepla administreret alene [se Lægemiddelinteraktioner ].
Effekt af stærk CYP1A2 CYP2B6 eller CYP3A -inducere
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with rifampin (a CYP1A2 CYP2B6 and CYP3A inducer) at steady state (600 mg once daily) in healthy volunteers decreased the AUC0-inf of fenfluramine by 58% and the Cmax by 40% and decreased the AUC0-inf of norfenfluramine by 50% and increased Cmax af Norfenfluramine med 13% sammenlignet med FinTepla administreret alene [Se Lægemiddelinteraktioner ].
Effekt af FinTepla på andre stoffer
Samtidig administration af en enkelt 0,7 mg/kg dosis fininepla med en enkelt dosis af en stiripentol clobazam og valproinsyre-kombination påvirkede ikke farmakokinetikken i Stiripentol eller farmakokinetikken af clobazam eller dets n.dsmethyl-metabolit norclobazam eller farmakokinetikken i clobazam som sammenlignet med rørle-klobolit norclobazam eller farmakokinetikken af valprroic acid som sammenlignet til omrøring af stiripent rørle-kloblam ogolam og den rørne rørle-klobolit nor clobazam Valproinsyre -kombination alene. Coadministration af en enkelt 0,35 mg/kg dosis fininepla med gentagne doser af cannabidiol påvirkede ikke farmakokinetikken i cannabidiol sammenlignet med cannabidiol alene.
In vitro -undersøgelser
Fenfluramine metaboliseres primært af CYP1A2 CYP2B6 og CYP2D6 In vitro . Andre CYP -enzymer involveret i mindre grad er CYP2C9 CYP2C19 og CYP3A4/5.
Effekt af fenfluramin og norfenfluramin på CYP -substrater: fenfluramin og norfenfluramin er ikke hæmmere eller inducerere af CYP1A2 CYP2B6 CYP2C8 CYP2C9 CYP2C19 CYP2D6 eller CYP3A4 i klinisk relevante koncentrationer.
Effekt af transportører på fenfluramin og norfenfluramin: fenfluramin og norfenfluramin er ikke substrater af P-G BCRP OAT1 OAT3 Oct2 Mate1 eller Mate2-K-transportører.
Effekt af FinTepla på transportører: fenfluramin og norfenfluramin er ikke hæmmere af P-gp BCRP OAT1b1 OATP1B3 OAT1 OAT3 Oct2 MATE1 eller MATE2-K-transportører.
Kliniske studier
Dravet syndrom
Effektiviteten af FinTepla til behandling af anfald forbundet med DS hos patienter 2 år og ældre blev etableret i to randomiserede dobbeltblinde placebokontrollerede forsøg hos patienter 2 til 18 år.
Undersøgelse 1 (N=117) compared a 0,7 mg/kg/dag og a 0,2 mg/kg/dag dose of FinTepla with placebo in patients who were not receiving stiripentol (NCT02682927 og NCT02826863).
Undersøgelse 2 (N=85) compared a 0,4 mg/kg/dag dose of FinTepla with placebo in patients who were receiving stiripentol og either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS og were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic og focal with observable motor signs. The baseline period was followed by rogomization into a 2- week (Undersøgelse 1) or 3-week (Undersøgelse 2) titration period og a subsequent 12-week maintenance period where the dose of FinTepla remained stable.
I undersøgelse 1 98% af patienterne tog mellem 1 og 4 samtidige AED'er. De mest anvendte samtidige AED'er (hos mindst 25%af patienterne) var valproat (61%) clobazam (59%) og topiramat (25%). I undersøgelse 2 100% af patienterne tog mellem 2 og 4 samtidige AED'er. De hyppigst anvendte samtidige AED'er (hos mindst 25%af patienterne) var Stiripentol (100%) clobazam (94%) og valproat (89%).
Det primære effektendepunkt i begge undersøgelser var ændringen fra baseline i hyppigheden af krampagtige anfald pr. 28 dage i den kombinerede 14-ugers (undersøgelse 1) eller 15-ugers (undersøgelse 2) titrering og vedligeholdelsesperioder (dvs. behandlingsperiode). Det median længste interval mellem krampagtige anfald blev også vurderet.
I undersøgelse 1 og undersøgelse 2 var reduktionen i krampagtig anfaldsfrekvens pr. 28 dage statistisk signifikant større for alle dosisgrupper af FinTepla sammenlignet med placebo (tabel 6). En reduktion i krampagtige anfald blev observeret inden for 3 til 4 uger efter start af FinTepla, og effekten forblev generelt konsistent i løbet af 14- eller 15-ugers behandlingsperiode.
Tabel 6: Ændring i krampagtig anfaldsfrekvens i behandlingsperioden indpatienter med Dravet -syndrom (undersøgelse 1 og undersøgelse 2)
| Krampende anfaldsfrekvens (pr. 28 dage) | Placebo | FinTepla 0,2 mg/kg/dag | FinTepla 0,7 mg/kg/dag | FinTepla 0,4 mg/kg/dag |
| Undersøgelse 1 | N = 39 | N = 38 | N = 40 | Na |
| Baseline periode median | 29.4 | 18.1 | 18.7 | Na |
| % Forskel i forhold til placebo* | -31,7% | -70,0% | Na | |
| p-værdi sammenlignet med placebo | 0.043 | <0.001 | ||
| Undersøgelse 2 | N = 42 | Na | Na | N = 43 |
| Baseline periode median | 11.5 | Na | Na | 15.0 |
| % Forskel i forhold til placebo* | Na | -59,5% | ||
| p-værdi sammenlignet med placebo | <0.001 | |||
| *Afledt af den primære analysemodel ± alle 0,4 mg/kg/dagspatienter tog også samtidig Stiripentol, hvilket øger eksponeringen af fininepla. |
Figur 1 og figur 2 viser procentdelen af patienter efter kategori af anfaldsrespons fra baseline i krampagtig anfaldsfrekvens (pr. 28 dage) i behandlingsperioden i henholdsvis undersøgelse 1 og undersøgelse 2.
Figur 1: Andel af patienter efter kategori af anfaldsrespons for FinTepla og placebo hos patienter med Dravet -syndrom (undersøgelse 1)
| |
Figur 2: Andel af patienter efter kategori af anfaldsrespons for FinTepla og placebo hos patienter med Dravet -syndrom (undersøgelse 2)
| |
I undersøgelse 1 3 af 40 (8%) patienter i FinTepla 0,7 mg/kg/daggruppen og 3 ud af 38 (8%) patienter i FinTepla 0,2 mg/kg/daggruppen rapporterede ingen krampagtige anfald i løbet af den 14-ugers behandlingsperiode sammenlignet med 0 patienter i placebogruppen. I undersøgelse 2 1 af 43 (2%) patienter i FinTepla 0,4 mg/kg/daggruppen rapporterede ingen krampeanfald i den 15-ugers behandlingsperiode sammenlignet med 0 patienter i placebogruppen.
I undersøgelse 1 og undersøgelse 2 blev FinTepla forbundet med et statistisk signifikant længere interval mellem krampagtige anfald sammenlignet med placebo (figur 3).
Figur 3: Median længst interval mellem krampagtige anfald hos patienter med Dravet -syndrom (undersøgelse 1 og undersøgelse 2)
| |
Lennox-Gastaut syndrom
Effektiviteten af FinTepla til behandling af anfald forbundet med LGS hos patienter 2 år og ældre blev etableret i en randomiseret dobbeltblind placebokontrolleret undersøgelse hos 263 patienter 2 til 35 år (undersøgelse 3; NCT03355209).
Undersøgelse 3 compared a 0,7 mg/kg/dag og a 0,2 mg/kg/dag dose of FinTepla with placebo.
Patienter havde en diagnose af LG'er og blev utilstrækkeligt kontrolleret på mindst en AED med eller uden vagal nervestimulering og/eller ketogen diæt. Undersøgelsen havde en 4-ugers baseline-periode, hvor patienterne blev forpligtet til at have mindst 8 drop anfald, mens de var på stabil AED-terapi. Drop-anfald blev generaliserede tonic-kloniske sekundært generaliserede tonic-kloniske tonic atoniske eller tonic-atoniske anfald, der blev bekræftet at resultere i dråber. Baselineperioden blev efterfulgt af randomisering til en 2-ugers titreringsperiode og en efterfølgende 12-ugers vedligeholdelsesperiode, hvor dosis af FinTepla forblev stabil.
I undersøgelse 3 99% af patienterne tog mellem 1 og 4 samtidige AED'er. De mest anvendte samtidige AED'er (hos mindst 25%af patienterne) var clobazam (45%) lamotrigin (34%) og valproat (56%).
Det primære effektendepunkt i undersøgelse 3 var medianprocentændringen fra baseline i hyppigheden af drop-anfald pr. 28 dage i den kombinerede 14-ugers titrerings- og vedligeholdelsesperioder (dvs. behandlingsperiode). Andelen af patienter, der opnår forbedring (minimalt meget eller meget forbedret) i det kliniske globale indtryk af ændring (CGI-I) som vurderet af hovedundersøgeren var et sekundært slutpunkt.
I undersøgelse 3 ændres medianprocenten fra baseline (reduktion) i hyppigheden af drop -anfald pr. 28 dage signifikant større for 0,7 mg/kg/dag dosisgruppen af FinTepla sammenlignet med placebo (tabel 7). En reduktion i drop-anfald blev observeret inden for 2 uger efter påbegyndelse af behandling med FinTepla, og effekten forblev generelt konsistent i løbet af den 14-ugers behandlingsperiode.
Medianprocenten reduktion fra baseline i drop anfaldsfrekvens pr. 28 dage for den lavere dosis af fininepla (NULL,2 mg/kg/dag) nåede ikke statistisk signifikans sammenlignet med placebo (tabel 7).
Tabel 7: Ændring i drop anfaldsfrekvens i behandlingsperioden hos patient med Lennox-Gastaut-syndrom (undersøgelse 3)
| Drop anfaldsfrekvens (pr. 28 dage) | Placebo | FinTepla 0,2 mg/kg/dag | FinTepla 0,7 mg/kg/dag |
| Undersøgelse 3 | N = 85* | N = 86* | N = 83* |
| Baseline periode median Anfald Frequency | 55.0 | 77.8 | 80.0 |
| Medianprocentændring fra baseline under behandlingen | -8,7% | -13,2% | -23,7% |
| p-værdi sammenlignet med placebo | 0,1917 | 0.0037 | |
| *Det samlede antal patienter, hvorpå effektivitetsanalysen var baseret på, er mindre end det samlede antal randomiseret i den dobbeltblinde placebokontrollerede undersøgelse, fordi patienter med manglende data blev udelukket fra effektivitetsanalysen. |
Figur 4 viser procentdelen af patienter efter kategori af reduktion fra baseline i drop anfaldsfrekvens pr. 28 dage i behandlingsperioden i undersøgelse 3.
Figur 4: Andel af patienter efter kategori af anfaldsrespons for FinTepla og placebo hos patienter med lennox.gastaut syndrom (undersøgelse 3)
| |
Numerisk større forbedringer på CGI-I af efterforsker blev observeret hos patienter behandlet med FinTepla sammenlignet med placebo.
Patientinformation til FinTepla
FinTeplaR ®
(Fin-tep-la)
(fenfluramin) Oral opløsning
Læs denne medicin guide, inden du begynder at tage FinTepla, og hver gang du får en påfyldning. Der kan være nye oplysninger. Disse oplysninger indtager ikke stedet for at tale med din sundhedsudbyder om din medicinske tilstand eller behandling.
Hvad er de vigtigste oplysninger, jeg skal vide om FinTepla?
FinTepla can cause serious side effects including :
1. Problemer med ventilerne i hjertet (valvulær hjertesygdom) og højt blodtryk i arterierne i lungerne (pulmonal arteriel hypertension) har været forbundet med FinTepla. Din sundhedsudbyder udfører en test kaldet et ekkokardiogram for at kontrollere dit hjerte og for højt blodtryk i arterierne i lungerne, før du begynder at tage FinTepla igen hver 6. måned under behandlingen og en gang 3 til 6 måneder efter du har taget din sidste dosis FinTepla.
Ring til din sundhedsudbyder med det samme, hvis du udvikler nogen af disse tegn og symptomer på hjerte- eller lungeproblemer under behandling med FinTepla:
- åndenød
- brystsmerter
- træthed eller svaghed
- fornemmelser af en hurtig flagrende hjerteslag
- Især med øget aktivitet (hjertebanken)
- Lightheadedness or besvimende
- uregelmæssig puls
- hævede ankler eller fødder
- blålig farve til dine læber og hud (cyanose)
På grund af risikoen for problemer med hjerteventiler (valvulær hjertesygdom) og højt blodtryk i arterier af lunger (pulmonal arteriel hypertension) er FinTepla kun tilgængelig gennem et begrænset program kaldet FinTepla Risk Evaluation and Mitigation Strategy (REMS) -program. Før du eller dit barn modtager FinTepla, vil din sundhedsudbyder eller apotek sørger for, at du forstår, hvordan du tager FinTepla sikkert. Hvis du har spørgsmål om FinTepla, så spørg din sundhedsudbyder, besøg www.finteplarems.com eller ring 1-877-964-3649.
2. nedsat appetit og nedsat vægt. Nedsat appetit og nedsat vægt are both serious og common side effects of FinTepla in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Din vægt skal kontrolleres regelmæssigt under din behandling med FinTepla.
- Din sundhedsudbyder kan muligvis foretage ændringer i din FinTepla -dosis, hvis din vægt falder. I nogle tilfælde kan FinTepla muligvis stoppes.
3. Søvnelighedssedation og mangel på energi (sløvhed). Disse er både alvorlige og almindelige bivirkninger af FinTepla hos mennesker med Dravet Syndrome (DS) eller Lennox-Gastaut Syndrome (LGS). At tage FinTepla med CNS -depressiva (Central Nervous (CNS), inklusive alkohol, kan øge søvnigheden. Kør ikke til at betjene tunge maskiner eller udføre andre farlige aktiviteter, før du ved, hvordan FinTepla påvirker dig.
4. som alle andre antiepileptiske stoffer kan FinTepla forårsage selvmordstanker eller handlinger hos et meget lille antal mennesker (ca. 1 ud af 500).
Ring til din sundhedsudbyder med det samme, hvis du har nogen af disse symptomer, især hvis de er nye værre eller bekymrer dig:
- Tanker om selvmord eller døende
- ny eller værre angst
- Problemer med at sove (søvnløshed)
- Handler på farlige impulser
- Forsøg på at begå selvmord
- føler sig ophidset eller rastløs
- Ny eller værre irritabilitet
- En ekstrem stigning i aktivitet og tale (Mania)
- Ny eller værre depression
- Panikanfald
- handler aggressivt at være vred eller voldelig
- Andre usædvanlige ændringer i adfærd eller humør
Hvordan kan jeg se efter tidlige symptomer på selvmordstanker og handlinger?
- Vær opmærksom på ændringer, især pludselige ændringer i humøradfærdstanker eller følelser.
- Opbevar alle opfølgende besøg hos din sundhedsudbyder som planlagt.
Selvmordstanker eller handlinger kan være forårsaget af andre ting end medicin. Hvis du har selvmordstanker eller handlinger, kan din sundhedsudbyder tjekke for andre årsager.
5. Stop ikke med at tage FinTepla uden først at tale med din sundhedsudbyder. At stoppe en anfaldsmedicin som FinTepla kan pludselig få dig til at få anfald oftere eller anfald, der ikke stopper (status epilepticus).
Ring til din sundhedsudbyder mellem besøg efter behov, især hvis du er bekymret for symptomer.
Hvad er FinTepla?
- FinTepla is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) og Lennox- Gastaut syndrome (LGS) in patients 2 years of age og older.
- Det vides ikke, om FinTepla er sikker og effektiv hos børn under 2 år.
Tag ikke FinTepla, hvis du:
- er allergiske over for fenfluramin eller nogen af ingredienserne i FinTepla. Se slutningen af denne medicinvejledning for en komplet liste over ingredienser i FinTepla.
- tager eller er stoppet med at tage medicin kaldet monoaminoxidaseinhibitorer (MAOI) i de sidste 14 dage. Dette kan forårsage et alvorligt eller livstruende problem kaldet Serotonin-syndrom. Hvis du ikke er sikker på, om du tager en af disse medicin, skal du kontakte din sundhedsudbyder.
Før du tager FinTepla, fortæl din sundhedsudbyder om alle dine medicinske tilstande, herunder hvis du:
- har hjerteproblemer
- har eller har haft vægttab
- har eller har haft depression humørproblemer eller selvmordstanker eller opførsel
- har nyreproblemer
- har leverproblemer
- er gravide eller planlægger at blive gravid. Fortæl din sundhedsudbyder med det samme, hvis du bliver gravid, mens du tager FinTepla. Du og din sundhedsudbyder vil beslutte, om du skal tage FinTepla, mens du er gravid.
- Hvis du bliver gravid, mens du tager FinTepla, skal du tale med din sundhedsudbyder om at registrere sig hos det nordamerikanske antiepileptiske narkotika graviditetsregister. Du kan tilmelde dig dette register ved at ringe til 1-888-233-2334 eller gå til www.
- aedpregnancyregistry.org. Formålet med dette register er at indsamle information om sikkerheden ved antiepileptiske lægemidler under graviditet.
- er amning eller planlægger at amme. Det vides ikke, om FinTepla passerer ind i din modermælk. Tal med din sundhedsudbyder om den bedste måde at fodre din baby på, mens du tager FinTepla.
Fortæl din sundhedsudbyder om alle de medicin, du tager inklusive receptpligtige og over-the-counter medicin vitaminer og urtetilskud.
Kend de medicin, du tager. Opbevar en liste over dem for at vise din sundhedsudbyder eller apotek, når du får en ny medicin.
Hvordan skal jeg tage FinTepla?
- Læs Brug til brug I slutningen af denne medicinvuide til information på den rigtige måde at bruge FinTepla.
- Tag FinTepla nøjagtigt, som din sundhedsudbyder beder dig om at tage det.
- Din sundhedsudbyder fortæller dig, hvor meget FinTepla du skal tage, og hvornår du skal tage det.
- FinTepla may be taken with or without food.
- Mål din dosis fininepla ved hjælp af den doseringssprøjte, der leveres af apoteket. Brug ikke en husholdningsteskefuld eller spiseskefuld.
- FinTepla can be given through gastric og nasogastric feeding tubes
Hvad skal jeg undgå, mens jeg tager FinTepla?
- Gør ikke Kør driver tunge maskiner eller udfør andre farlige aktiviteter, indtil du ved, hvordan FinTepla påvirker dig. FinTepla kan få dig til at føle dig søvnig.
Hvad er de mulige bivirkninger af FinTepla?
FinTepla may cause serious side effects including:
Ring til din sundhedsudbyder med det samme, hvis du har nogen af følgende symptomer på serotonin -syndrom.
- Se 'Hvad er de vigtigste oplysninger, jeg burde vide om FinTepla?'
- serotonin syndrome. Serotonin-syndrom er et livstruende problem, der kan ske hos mennesker, der tager FinTepla, især hvis FinTepla tages med visse andre lægemidler til at inkludere:
- Antidepressiv medicin kaldet SSRIS SNRIS TCAS og MAOIS
- St. Johns Wort
- Tryptophan
- Dextromethorphan
- lithium
- tramadol
- Antipsykotika
- Mental status ændres såsom at se ting, der ikke er der (hallucinationer) agitation eller koma
- Hurtig hjerteslag
- Kvalme opkast diarré
- Ændringer i blodtrykket
- høj kropstemperatur
- stramme muskler
- problemer med at gå
- Højt blodtryk (hypertension). Hypertension er både en alvorlig og almindelig bivirkning. FinTepla kan få dit blodtryk til at stige, selvom du aldrig har haft højt blodtryk før. Din sundhedsudbyder tjekker dit blodtryk, mens du tager FinTepla.
- Øget tryk i dit øje (glaukom). Symptomer på glaukom kan omfatte:
- Røde øjne
- nedsat vision
- At se haloer eller lyse farver omkring lys
- øjesmerter eller ubehag
- kvalme eller opkast
- sløret vision
Hvis du har nogen af disse symptomer, skal du ringe til din sundhedsudbyder med det samme.
De mest almindelige bivirkninger af FinTepla, når de bruges til behandling af Dravet Syndrome (DS), inkluderer:
- nedsat appetit
- diarre
- lav energi
- søvnighed
- Problemer med bevægelsesbalance og gåture
- øget droole
- luftvejsinfektion
- øget blodtryk
- nedsat vægt
- opkast
- feber
- falder
- forstoppelse
- anfald, der ikke stopper
- unormalt ekkokardiogram
- svaghed
De mest almindelige bivirkninger af FinTepla, når de bruges til behandling af Lennox-Gastaut-syndrom (LGS), inkluderer:
- diarre
- træthed
- opkast
- søvnighed
- nedsat appetit
Dette er ikke alle de mulige bivirkninger af FinTepla. For mere information, spørg din sundhedsudbyder eller apotek.
Fortæl din sundhedsudbyder, hvis du har nogen bivirkning, der generer dig, eller som ikke forsvinder.
Ring til din læge for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088.
Hvordan skal jeg opbevare FinTepla?
- Opbevar FinTepla ved stuetemperatur mellem 68 ° F til 77 ° F (20 ° C og 25 ° C).
- Gør ikke Køleskab eller frys.
- Opbevar FinTepla -flasken og sprøjte sammen i et rent område.
- Kast væk (kasser) enhver ubrugt FinTepla 3 måneder efter først åbningen af flasken, eller hvis kasser efter dato på pakken eller flasken er gået. Uanset hvilken der kommer først.
Hold FinTepla og alle medicin uden for børns rækkevidde.
Medicin er undertiden ordineret til andre formål end dem, der er anført i en medicinguide. Brug ikke FinTepla til en betingelse, som den ikke blev ordineret til. Giv ikke FinTepla til andre mennesker, selvom de har de samme symptomer, som du har. Det kan skade dem.
Du kan bede din farmaceut eller sundhedsudbyder om information om FinTepla, der er skrevet til sundhedsfagfolk.
Hvad er ingredienserne i FinTepla?
Aktiv ingrediens: Fenfluraminhydrochlorid
Inaktive ingredienser: Kirsebærsmag citronsyreethylparaben hydroxyethylcellulose methylparaben kaliumcitrat sucralose og vand.
FinTepla contains no ingredient made from gluten-containing grain (wheat barley or rye) og contains not more than 0.1% of kulhydrater hvilket er fra kirsebærsmag.
Denne medicinguide er godkendt af U.S. Food and Drug Administration.
Brug til brug
FinTepla ®
(Fin-tep-la)
(fenfluramin) Oral opløsning 2.2 mg/mL
Sørg for, at du læser forstå og følger disse instruktioner, inden du begynder at bruge FinTepla Oral Solution, og hver gang du får en påfyldning. Der kan være nye oplysninger.
Denne brugsanvisning indeholder oplysninger om, hvordan man tager FinTepla. Disse oplysninger indtager ikke stedet for at tale med din sundhedsudbyder om din medicinske tilstand eller behandling.
Hvad er inkluderet i FinTepla?
Følgende poster er inkluderet for at forberede og give en oral dosis af FinTepla:
- 1 flaske fininepla oral opløsning (NULL,2 mg/ml)
- 2 Genanvendelige orale sprøjter
| |
Ring til apoteket på 1-844-288-5007, hvis du ikke modtog de varer, der er anført ovenfor, eller hvis du har brug for hjælp til at bruge dem.
Vigtig information om FinTepla
- FinTepla is an oral medicine (taken by mouth) og is given 2 gange hver dag . Følg dine sundhedsudbydere instruktioner til at tage eller give doser af FinTepla.
- Hvis du har spørgsmål om, hvordan du forbereder eller giver FinTepla, skal du kontakte din sundhedsudbyder eller ringe til din farmaceut.
- Brug altid de orale sprøjter, der leveres med FinTepla for at sikre, at den rigtige dosis gives. Hvis du har brug for en ny sprøjte, skal du kontakte din farmaceut. Gør ikke Brug en husholdningsteskefuld eller spiseskefuld.
Orale sprøjter forsynet med FinTepla af apoteket.
Med FinTepla modtager du 2 genanvendelige orale sprøjter.
2 mundtlige sprøjter, der kan måle op til 3 ml
ELLER
2 mundtlige sprøjter, der kan måle op til 6 ml
| |
Ring til apoteket på 1-844-288-5007, hvis du har spørgsmål om sprøjterne, der er forsynet med FinTepla.
Dele af den orale sprøjte
| |
Forberedelse af en dosis
Trin 1 . Sørg for, at du har:
- Flasken med FinTepla oral opløsning og
- En ren tør genanvendelig oral sprøjte, der blev forsynet med FinTepla.
Trin 2. Kontroller kasser efter dato (mm/dd/åååå).
| |
- Gør ikke Brug medicinen, hvis kastet væk (kasser) dato er gået.
- Hvis datoen er i nærheden af, skal du kontakte din apotek eller sundhedsudbyder for at få en påfyldning eller en ny recept.
- Hvis datoen er vedtaget bortskaffelse af ubrugt FinTepla.
Trin 3. Tryk ned og vend den børnefasthætte til venstre (mod uret), og fjern den fra flasken.
- Sæt hætten til side (smid ikke væk).
| |
Trin 4. Sørg for, at adapteren er på flasken.
- Hvis flasken ikke har en adapter, skal du kontakte farmaceut.
- Efterlad altid adapteren på plads i flasken medicin.
| |
Trin 5. Fjern en oral sprøjte fra dens emballage om nødvendigt.
Brug kun de orale sprøjter, der er forsynet med FinTepla.
Hvis en oral sprøjte er beskadiget, eller du ikke kan læse dosismarkeringerne:
- Brug den anden orale sprøjte tilvejebragt eller
- Kontakt farmaceut for at få en ny.
| |
Trin 6. Sørg for, at stemplet skubbes helt ind i den orale sprøjte.
| |
Trin 7. Hold flasken med medicin fast på en hård flad overflade.
Trin 8. Skub spidsen af den orale sprøjte ind i åbningen af adapteren, indtil den ikke kan skubbes yderligere.
| |
Trin 9. Hold den orale sprøjte og flaske sammen, og vend på hovedet.
| |
Trin 10. Træk langsomt stemplet i den orale sprøjte for at trække den foreskrevne dosis tilbage.
| |
| |
| |
Forberedelse af en dosis (fortsat)
Trin 11. Line op i slutningen af stemplet med mærket for den foreskrevne dosis på den orale sprøjte.
Tips til at få den rigtige dosis
- Hvis du tegner for meget medicin:
- Skub stemplet langsomt tilbage i sprøjten, indtil du når den foreskrevne dosis.
- Hvis du ser luftbobler i medicinen:
- Træk stemplet længere ned.
- Lad boblerne stige til spidsen af sprøjten.
- Skub stemplet i hele vejen.
- Træk langsomt stemplet ud til den foreskrevne dosis.
Note: Meget små bobler i væsken er normale.
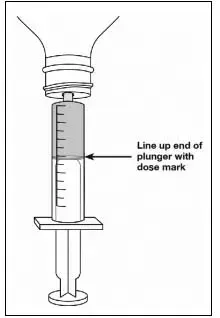
Trin 12. Hold den orale sprøjte og flaske sammen, og drej derefter flasken højre side op.
| |
Trin 13. Holde flasken fast forsigtigt træk den orale sprøjte ud af flaskeadapteren.
| |
Trin 14. Sørg for, at dosis i den orale sprøjte stadig matcher den foreskrevne dosis.
Hvis dosis ikke stemmer overens:
- Sæt sprøjten tilbage i adapteren.
- Se trin 9 til 11 for at justere dosis efter behov.
Giver FinTepla
Trin 15. Placer spidsen af den orale sprøjte mod indersiden af kinden.
Trin 16. Skub forsigtigt stemplet ind, indtil al medicin i den orale sprøjte er givet.
| |
- Gør ikke Sprøjt eller skubbe medicinen kraftigt ind i bagsiden af halsen. Dette kan forårsage kvælning.
Trin 17. Læg hætten tilbage på flasken tæt ved at dreje hætten til højre (med uret), indtil den stopper.
- Efterlad altid adapteren på plads in the bottle
- Hætten passer over det.
| |
Rengøring af sprøjten
- Skyl den orale sprøjte med rent ledningsvand og lad den lufttørres efter hver brug.
- Sørg for at skylle indersiden af sprøjten og stemplet.
Rengøringstips:
- Træk rent vand fra hanen ind i sprøjten med stemplet, og skub den ud flere gange for at rense sprøjten.
- Fjern stemplet fra tønden på den orale sprøjte
- Skyl begge dele under ledningsvand
- Sørg for, at sprøjten og stemplet er helt tørre inden den næste brug.
- Sprøjten er også sikker at rengøre i opvaskemaskinen.
| |
Hvordan skal jeg opbevare FinTepla?
- Opbevar FinTepla ved stuetemperatur mellem 68 ° F til 77 ° F (20 ° C til 25 ° C).
- Gør ikke Køleskab eller frys.
- Hold hætten tæt lukket og flasken lodret.
- Opbevar FinTepla -flasken og sprøjte sammen i et rent område.
- Kast væk (kasser) enhver ubrugt FinTepla 3 måneder efter først åbningen af flasken, eller hvis kasser efter dato på pakken eller flasken er gået. Uanset hvilken der kommer først.
- Hold FinTepla og alle medicin uden for børns rækkevidde.
Denne brugsanvisning er godkendt af U.S. Food and Drug Administration.
