Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
KoagulationsfaktorerEsperoct
Resume af lægemiddeloversigt
Hvad er Esperoct?
Esperoct [Antihemophilic Factor (rekombinant) glycopegyleret-exei] er en Koagulation Faktor VIII-koncentrat indikeret til brug hos voksne og børn med hæmofili A til on-demand-behandling og kontrol af blødningspisoder Perioperativ håndtering af blødning og rutinemæssig profylakse for at reducere hyppigheden af blødningsepisoder. Esperoct er ikke indikeret til behandling af von Willebrand sygdom.
Hvad er bivirkninger af Esperoct?
Esperoct topper
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- kløe
- udslæt
- følelsesløshed
- prikken
- feber
- svimmelhed
- kvalme
- Hurtige hjerteslag
- brysttæthed
- hvæsende
- Bleg hud
- kold sved
- Lightheadedness
- besvimende
- Forøgede blødningspisoder
- enhver blødning, der ikke stopper og
- brystsmerter
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Almindelige bivirkninger af esperoct inkluderer:
- udslæt
- rødme
- kløe og
- reaktioner på injektionsstedet
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; og pludselig svimmelhed letthed eller udlevering;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til esperoct
Dosis af esperoct afhænger af brugen.
Hvilke stoffer stoffer eller kosttilskud interagerer med Esperoct?
Esperoct kan interagere med andre lægemidler. Fortæl din læge alle medicin og kosttilskud, du bruger.
Esperoct under graviditet eller amning
Fortæl din læge, hvis du er gravid eller planlægger at blive gravid, før du bruger Esperoct; Det er ukendt, hvordan det ville påvirke et foster. Det er ukendt, om Esperoct passerer ind i modermælk, eller om det vil påvirke et sygeplejemiddel. Kontakt din læge inden amning.
Yderligere oplysninger
Vores esperoct [antihemofil faktor (rekombinant) glycopegyleret-exei] lyofiliseret pulver til opløsning til intravenøs brug bivirkninger lægemiddelcenter giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager dette medicin.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
Beskrivelse for esperoct
Esperoct er en steril konserveringsfri ikke-pyrogen lyofiliseret pulver til intravenøs injektion efter rekonstitution med det medfølgende saltvandsmiddel. Den aktive ingrediens i Esperoct er en rekombinant analog af human koagulationsfaktor VIII (FVIII) konjugeret med en 40-kDa polyethylenglycol (PEG) molekyle. Esperoct er formuleret med følgende excipienser: natriumchlorid L-histidin sucrose polysorbat 80 l-methionin og calciumchlorid.
FVIII -aktivitet i Esperoct bestemmes ved anvendelse af det kromogene assay beskrevet i den europæiske farmakopé. Aktivitetsopgaven anvender et FVIII -referencemateriale, der kan spores til den nuværende Verdenssundhedsorganisation (WHO) international standard for FVIII -koncentrat og evalueret ved passende metoder for at sikre nøjagtigheden af resultaterne. Esperoct fås i enkeltdosis hætteglas, der indeholder nominelt 500 1000 1500 2000 eller 3000 IE FVIII. Hvert hætteglas med esperoct er mærket med den faktiske FVIII -aktivitet. Efter rekonstitution med det medfølgende fortyndingsmiddel (NULL,9% saltvand) indeholder hver ML af opløsningen henholdsvis ca. 125 250 375 500 eller 750 IE FVIII.
FVIII-proteinet i Esperoct produceres i kinesiske hamster-ovarieceller (CHO) -celler ved anvendelse af rekombinant DNA-teknologi og indeholder et trunkeret B-domæne, der er O-glycosyleret. Polypeptiddelen af molekylet har en molekylær masse på 166 kDa (beregnet eksklusive post-translationelle modifikationer) og repræsenterer en heterodimer af en tung kæde og en let kæde, der holdes sammen af ikke-kovalente interaktioner. Det rekombinante FVIII -protein renses ved anvendelse af en række kromatografiske trin, hvoraf det ene er affinitetskromatografi ved anvendelse af et monoklonalt antistof til selektivt at isolere RFVIII fra cellekulturmediet. Det 40-kDa PEG-molekyle konjugeres til O-glycan-gruppen af B-domænet ved anvendelse af en enzymatisk reaktion for at producere en glycopegyleret FVIII (FVIII-PEG). Oprensningsprocessen inkluderer to virale clearance-trin, nemlig vaskemiddel (Triton X-100) -behandling til inaktivering af indhyllede vira og 20-nm filtrering til fjernelse af indhyllede og ikke-indhyllede vira. Ingen tilsætningsstoffer af menneskelig eller dyrs oprindelse bruges under fremstillingsprocessen og formulering af Esperoct.
I blodcirkulationen, når FVIII-PEG aktiveres af thrombin, er B-domæne-delen med den vedhæftede PEG-del spaltet af, og den resulterende aktiverede FVIII (FVIIIa) ligner struktur og funktion som indfødte FVIIIa.
Anvendelser til Esperoct
Esperoct ® [Antihemofil faktor (rekombinant) glycopegyleret-exei] er en rekombinant DNA-afledt koagulationsfaktor VIII-koncentrat, der er angivet til brug hos voksne og børn med hæmofili A for:
- On-demand-behandling og kontrol af blødende episoder
- Perioperativ håndtering af blødning
- Rutinemæssig profylakse for at reducere hyppigheden af blødningspisoder
Begrænsning af brug
Esperoct ® er ikke indikeret til behandling af von Willebrand sygdom. (1)
Dosering til esperoct
Til intravenøs infusion efter kun rekonstitution.
Dosis
- Dosering og behandlingsvarighed afhænger af sværhedsgraden af faktor VIII -mangel på placering og omfang af blødning og af patientens kliniske tilstand. Omhyggelig overvågning af erstatningsterapi er nødvendig i tilfælde af større kirurgi eller livstruende blødningsepisoder.
- Hvert hætteglas med esperoct ® Indeholder den mærkede mængde rekombinant faktor VIII i internationale enheder (IU). En IU af faktor VIII -aktivitet svarer til mængden af faktor VIII i en milliliter af normalt humant plasma. Beregningen af den krævede dosering af faktor VIII er baseret på den empiriske konstatering af, at en IU af faktor VIII pr. Kg kropsvægt hæver plasmafaktoren VIII -aktiviteten med to IU/DL.
On - efterspørgsel
Tabel 1 kan bruges til at guide dosering af esperoct ® Til behandling af blødende episoder.
Tabel 1: Dosering af Esperoct ® At kontrollere blødningsepisoder
| Type blødning | Ungdom/ voksne ≥12 år Dosis (IU/kg) | Børn <12 years Dosis (IU/kg) | Yderligere doser |
| Mindre | |||
| Tidlig hæmarthrose mild muskelblødning eller oral blødning | 40 | 65 | En dosis skal være tilstrækkelig |
| Moderat | |||
| Mere omfattende hæmarthrosismuskelblødning eller hæmatom | 40 | 65 | En yderligere dosis kan administreres efter 24 timer |
| Major | |||
| Livs- eller lem-truende blødning gastro-intestinal blødning intrakraniel intraabdominal eller intrathoracic blødning brud | 50 | 65 | Yderligere dosis (er) kan administreres cirka hver 24. time |
Perioperativ styring
Dosisniveauet og doseringsintervaller til operation afhænger af proceduren og lokal praksis. En guide til dosering med Esperoct ® Under operationen (perioperativ styring) findes i tabel 2 nedenfor.
Tabel 2: Dosering til perioperativ styring med Esperoct ®
| Operationstype | Ungdom/ voksne ≥12 år Pre-operative Dosis (IU/kg) | Børn <12 years Pre-operative Dosis (IU/kg) | Yderligere doser |
| Mindre | |||
| Inklusive tandekstraktion | 50 | 65 | Yderligere dosis (er) kan administreres efter 24 timer, hvis det er nødvendigt |
| Major | |||
| Intrakraniel intra-abdominal intrathoracic eller fælles erstatningskirurgi | 50 | 65 | Yderligere doser can be administered approximately every 24 hours for the first week og then approximately every 48 hours until wound healing has occurred |
Rutinemæssig profylakse
Voksne og unge (≥ 12 år): Den anbefalede startdosis er 50 IE esperoct ® pr. kg kropsvægt hver 4. dag.
Dette regime kan justeres individuelt til mindre eller hyppigere dosering baseret på blødningsepisoder.
Børn ( <12 years): A dose of 65 IU of Esperoct ® pr. kg kropsvægt to gange ugentligt. Dette regime kan justeres individuelt til mindre eller hyppigere dosering baseret på blødningsepisoder.
Dosering (IU) = kropsvægt (kg) × Ønsket faktor VIII Forøgelse (IU/DL eller % normal) × 0,5
- Esperoct ® Kan også doseres for at opnå et specifikt målfaktor VIII-aktivitetsniveau afhængigt af sværhedsgraden af hæmofili til on-demand-behandling/kontrol af blødende episoder eller perioperativ håndtering. Brug følgende formel for at opnå en specifik målfaktor VIII -aktivitetsniveau:
- Base dosis og hyppighed af esperoct ® på den individuelle kliniske respons. Patienter kan variere i deres farmakokinetiske og kliniske responser.
- Hvis overvågning af faktor VIII-aktivitet udføres, skal du bruge en kromogen eller en-trins koagulationsassay, ® [se Advarsler og forholdsregler ].
Forberedelse og rekonstitution
- Vask altid hænderne og sørg for, at området er rent, inden du udfører rekonstitutionsprocedurerne.
- Brug aseptisk teknik under rekonstitutionsprocedurerne.
- Hvis dosis kræver mere end et hætteglas med esperoct ® Per infusion rekonstituerer hvert hætteglas i henhold til følgende instruktioner.
Oversigt over Esperoct ® Pakke
Oversigt
Hætteglas med esperoct ® pulver
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct.webp' > |
Rekonstitution
| ® vial and the pre-filled diluent syringe to room temperature. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-1.webp' > |
| ® vial. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-2.webp' > |
 |
| ® Hætteglas på en flad og solid overflade. Mens du holder den beskyttende cap, skal du placere hætteglasadapteren over Esperoct ® vial and press down firmly on the protective cap until the vial adapter spike penetrates the rubber stopper. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-4.webp' > |
 |
 |
 |
 |
 |
| ® vial until all of the powder is dissolved. Avoid shaking the vial and foaming the solution. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-10.webp' > |
- Medbring Esperoct ® Hætteglas og den forudfyldte fortyndingssprøjte til stuetemperatur.
- Fjern plastikhætten fra Esperoct ® hætteglas.
- Tør gummiproppen på hætteglasset med en steril alkoholpind og lad det tørre inden brug.
- Fjern beskyttelsespapiret fra hætteglasadapteren. Fjern ikke hætteglasadapteren fra den beskyttende cap.
- Placer esperoct ® Hætteglas på en flad og solid overflade. Mens du holder den beskyttende cap, skal du placere hætteglasadapteren over Esperoct ® Hætteglas og tryk fast på den beskyttende hætte, indtil hætteglasadapteren spids trænger ind i gummiproppen.
- Fjern beskyttelseshætten forsigtigt fra hætteglasadapteren.
- Tag fat i stempletstangen som vist på diagrammet. Fastgør stemplet stangen til sprøjten ved at holde stemplet stangen ved den brede øverste ende. Drej stempletstangen med uret ind i gummipelgrungen inde i den forudfyldte fortyndingssprøjte, indtil der føles modstand.
- Afbryd sprøjtehætten fra den forudfyldte fortyndingssprøjte ved at knipse perforeringen af hætten.
- Tilslut den forudfyldte fortyndingssprøjte til hætteglasadapteren ved at dreje den med uret, indtil den er sikret.
- Skub stemplets stang for langsomt at injicere alt fortyndingsmidlet i hætteglasset.
- Uden at fjerne sprøjten hvirvler blidt på esperoct ® Hætteglas, indtil alt pulveret er opløst. Undgå at ryste hætteglasset og skumme løsningen.
Administration
Kun til intravenøs infusion
- Parenterale lægemiddelprodukter skal inspiceres visuelt for partikler og misfarvning inden administration hver gang løsning og containertilladelse. Løsningen skal være klar og har ingen partikler. Brug ikke, hvis partikler eller misfarvning observeres.
- Administrer ikke esperoct ® I samme rør eller beholder med andre medicinske produkter.
- Administrer esperoct ® Løsning straks. Hvis ikke opbevares opløsningen i hætteglasset med hætteglasadapteren og sprøjten fastgjort. Brug esperoct ® Inden for 4 timer, når det opbevares ved ≤86 ° F (30 ° C) eller inden for 24 timer, når den opbevares i et køleskab ved 36 ° F til 46 ° F (2 ° C).
| ® vial and slowly draw the solution into the syringe. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-11.webp' > |
- Inverter Esperoct ® Hætteglas og trækker langsomt opløsningen ind i sprøjten.
- Fjern sprøjten fra hætteglasadapteren ved at dreje sprøjten mod uret.
- Fastgør sprøjten til Luer -enden af et infusionsnålesæt.
- Tilfør den rekonstituerede esperoct ® intravenøst langsomt over cirka 2 minutter.
- Efter infusion skal du bortskaffe sprøjten med infusionen indstille hætteglasset med hætteglasadapteren enhver ubrugt esperoct ® og andre affaldsmaterialer.
Forsigtighed
Den forudfyldte fortyndingssprøjte er lavet af glas med en indvendig spidsdiameter på 0,037 tommer og er kompatibel med et standard Luer-Lock-stik.
Nogle nådeløse stik til intravenøse katetre er uforenelige med glas fortyndingsmiddelsprøjter (for eksempel visse stik med en intern spike, såsom Clave ® /Mikroklav ® Invision-plus ® Invision-plus CS ® Invision-plus junior ® Bionector ® ) og deres anvendelse kan skade forbindelsen og påvirke administrationen. At administrere esperoct ® Gennem inkompatible nåleløse stik trækker det rekonstituerede produkt tilbage til en standard 10 ml steril luer-lock plastsprøjte.
Hvor leveret
Doseringsformularer og styrker
Esperoct ® fås som en steril hvid til off-white lyofiliseret pulver leveret i enkeltdosis hætteglas indeholdende nominelt 500 1000 1500 2000 eller 3000 IE. Den faktiske FVIII -aktivitet er trykt på hver esperoct ® Hætteglas og karton.
Efter rekonstitution med 4 ml saltvands fortyndingsmiddel ® henholdsvis.
- Esperoct ® leveres i pakker bestående af et enkeltdosis hætteglas indeholdende nominelt 500 1000 1500 2000 eller 3000 IE faktor VIII-aktivitet; en mixpro ® Forudfyldt fortyndingsmiddelsprøjte indeholdende 0,9% saltopløsning; og en steril hætteglasadapter med et 25-mikrometerfilter, der fungerer som en nådeløs rekonstitutionsenhed.
- Den faktiske faktor VIII -aktivitet i IU er angivet på hver esperoct ® Karton og hætteglas etiket.
Tabel 9: Esperoct ® Præsentationer
| Nominel doseringsstyrke | Cap Color Indicator | Karton NDC Antal | Komponenter |
| 500 IE | Rød | NDC 0169 8500 01 |
|
| 1000 IE | Grøn | NDC 0169 8100 01 |
|
| 1500 IE | Grå | NDC 0169 8150 01 |
|
| 2000 iu | Gul | NDC 0169 8200 01 |
|
| 3000 IE | Sort | NDC 0169 8300 01 |
|
| Iu = internationale enheder |
- Esperoct ® Hætteglas er lavet af glas lukket med en chlorobutylgummipop (ikke lavet med naturgummi latex) og forseglet med en aluminiumshætte.
- De forudfyldte fortyndingsmiddelsprøjter er lavet af glas med en siliconiseret bromobutylgummi-stemplet (ikke lavet med gummi latex).
- De lukkede hætteglas og forudfyldte fortyndingsmiddelsprøjter er udstyret med en manipulationssidenskabelig snap-off cap, der er lavet af polypropylen.
Opbevaring og håndtering
- Butik esperoct ® I den originale pakke for at beskytte Esperoct ® hætteglas fra lys.
- Butik esperoct ® i en pulverform under køling ved 36 ° F til 46 ° F (2 ° C (2 ° C) i op til 30 måneder fra fremstillingsdatoen indtil udløbsdatoen angivet på etiketten. I løbet af den 30-måneders holdbarhed. ® Kan opbevares ved stuetemperatur:
- op til 86 ° F (30 ° C) i ikke længere end 12 måneder eller
- Op til 104 ° F (40 ° C) i ikke længere end 3 måneder
- Registrer datoen på kartonen, da produktet blev fjernet fra køleskabet. Returner ikke produktet til køleskabet.
- Frys ikke esperoct ® .
- Brug ventetid ® Inden for 4 timer efter rekonstitution, når den opbevares ved ≤86 ° F (30 ° C) eller inden for 24 timer, når den opbevares i køleskabet. Opbevar det rekonstituerede produkt i hætteglasset.
- Kasser ethvert ubrugt rekonstitueret produkt.
Fremstillet af: Novo Nordisk A/S DK-2880 Bagsvaerd Danmark. Revideret: SEP 2022
Pred Forte øjendråber bivirkninger
Bivirkninger for Esperoct
De hyppigst rapporterede bivirkninger (forekomst ≥1%) i kliniske forsøg var udslæt rødme kløe (kløe) og reaktioner på injektionsstedet.
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, kan der ikke sammenlignes bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte med hastigheder i kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de hastigheder, der er observeret i klinisk praksis.
Sikkerheden ved Esperoct ® er blevet evalueret hos 270 forsøgspersoner (202 unge/voksne og 68 børn) i fem potentielle kliniske studier i flere centrum hos tidligere behandlede patienter (PTP'er) med svær hæmofili A ( <1% endogenous Factilr VIII activity) og no histilry of inhibitilrs. All subjects received at least one dose of Esperoct ® . En tidligere behandlet patient blev defineret som et emne med en historie med mindst 150 eksponeringsdage til andre faktor VIII -produkter (ungdoms-/voksne individer) eller 50 eksponeringsdage til andre faktor VIII -produkter (pædiatriske personer). Total eksponering for Esperoct ® var 80425 eksponeringsdage svarende til 889 patientårs behandling.
Under de kliniske forsøg i PTPS -bivirkninger forekom med en hastighed på 0,10 begivenheder pr. Patientår med eksponering. De hyppigst rapporterede bivirkninger var udslæt (NULL,2%) injektionsstedets reaktion (NULL,6%) rødme (NULL,9%) og kløe (kløe) (NULL,5%).
Immunogenicitet
Personer blev overvåget for neutralisering og ikke-neutraliserende antistoffer mod faktor VIII polyethylenglycol (PEG) og CHO værtscelleprotein. Et tidligere behandlet individ udviklede bekræftede neutraliserende antistoffer til faktor VIII (NULL,5 Bethesda -enheder). Derudover havde to forsøgspersoner kortvarigt titer FVIII -antistof ( <5 Bethesda Units) test results at a single occasion. Anti-PEG antibodies of no clinical consequence were detected in 45 subjects 32 of whom had pre-existing anti-PEG antibodies. Nine subjects developed anti-CHO host cell protein antibodies of no clinical consequence.
Påvisningen af antistoffer er meget afhængig af følsomheden og specificiteten af assayet. Derudover kan den observerede forekomst af antistof (inklusive neutraliserende antistof) positivitet i et assay påvirkes af adskillige faktorer, herunder assaymetodologi Prøvehåndteringstidspunkt for prøveopsamling Samtidig medicin og underliggende sygdom.
Oplevelse af postmarketing
Følgende bivirkninger er blevet identificeret under post-godkendelse af Esperoct ® . Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at pålideligt estimere deres frekvens eller etablere et årsagsforhold til eksponering for lægemidler.
Nedsat faktor VIII -aktivitet: Der er rapporteret om nedsat faktor VIII -aktivitet i fravær af detekterbare faktor VIII -hæmmere hos tidligere behandlede patienter (PTP'er) ved skift til Esperoct ® Fra andre faktor VIII -produkter.
Lægemiddelinteraktioner for Esperoct
Ingen oplysninger leveret
Advarsler for Esperoct
Inkluderet som en del af 'FORHOLDSREGLER' Afsnit
Forholdsregler for Esperoct
Overfølsomhedsreaktioner
Allergisk type overfølsomhedsreaktioner inklusive anafylaksi er mulige med Esperoct ® . Produktet indeholder spor af hamsterproteiner, som hos nogle patienter kan forårsage allergiske reaktioner [se BESKRIVELSE ]. Early signs of allergic reactions which can progress til anaphylaxis may include angioedema brysttæthed Besvær hvæsende udslæt elveblest og kløe. Observe patients for signs og symptilms of acute hypersensitivity reactions particularly during the early phases of exposure til the product. Discontinue use of Esperoct ® Hvis allergiske- eller anafylaktiske reaktioner forekommer og initierer passende behandling.
Neutraliserende antistoffer
Dannelsen af neutraliserende antistoffer (hæmmere) til faktor VIII har fundet sted efter administration af Esperoct ® . Overvåg patienter for udvikling af faktor VIII -hæmmere ved passende kliniske observationer og laboratorieundersøgelser. Hvis forventet faktor VIII -aktivitetsplasmaniveauer ikke opnås, eller hvis blødning ikke kontrolleres efter esperoct ® Administration mistænker tilstedeværelsen af en hæmmer (neutraliserende antistof) [se Overvågning af laboratorieundersøgelser ].
Overvågning af laboratorieundersøgelser
Hvis overvågning af faktor VIII udføres, skal ® [se Dosering og administration ].
Faktor VIII -aktivitetsniveauer kan påvirkes af typen af aktiveret delvis thromboplastin -tid (APTT) reagens anvendt i assayet. Nogle silicabaserede aptt-reagenser kan undervurdere aktiviteten af Esperoct ® med op til 60%; Andre reagenser kan overvurdere aktiviteten med 20%. Hvis der ikke er en passende en-trins koagulation eller kromogen assay, skal du ikke være tilgængelig lokalt, så brug et referencelaboratorium.
Hvis blødning ikke kontrolleres med den anbefalede dosis af Esperoct ® eller hvis den forventede faktor VIII -aktivitetsniveauer i plasma ikke opnås, skal du udføre et Bethesda -assay for at bestemme, om faktor VIII -hæmmere er til stede.
Oplysninger om patientrådgivning
Rådgive patienter:
- At læse den FDA-godkendte patientmærkning ( Patientinformation og Brug til brug ).
- At allergisk type overfølsomhedsreaktioner eller anafylaksi er mulige ved brug af esperoct ® . Informer patienter om de tidlige tegn på overfølsomhedsreaktioner, herunder udslæt elveblest kløe ansigts hævelse tæthed i brystet og vejrtrækning. Rådgive patienter om at afbryde brugen af Esperoct ® Umiddelbart og kontakt deres sundhedsudbyder og/eller søg straks akutpleje, hvis disse symptomer opstår.
- At kontakte deres sundhedsudbyder eller behandlingsanlæg for yderligere behandling og/eller vurdering, hvis de oplever en mangel på en klinisk respons på faktor VIII -erstatningsterapi, da dette kan være en manifestation af en hæmmer.
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
Karcinogenese -mutagenese og svækkelse af fertilitetsundersøgelser hos dyr er ikke blevet udført.
Brug i specifikke populationer
Graviditet
Risikooversigt
Der er ingen data med Esperoct ® Brug hos gravide kvinder til at afgøre, om der er en stofassocieret risiko. Dyre reproduktionsundersøgelser er ikke blevet udført med Esperoct ® . Det er ukendt, om Esperoct ® kan forårsage føtal skade, når man administreres til en gravid kvinde eller kan påvirke fertiliteten.
I den amerikanske generelle befolkning er den estimerede baggrundsrisiko for major fødselsdefekt og miscarriage in clinically recognized pregnancies is 2–4% og 15–20% henholdsvis.
Amning
Risikooversigt
Der er ingen oplysninger om tilstedeværelsen af Esperoct ® I human mælk effekten på det ammede spædbarn og virkningerne på mælkeproduktionen. De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med mors kliniske behov for Esperoct ® og any potential adverse effects on the breastfed infant from Esperoct ® eller fra den underliggende moderlige tilstand.
Pædiatrisk brug
Sikkerhed og effektivitet blev evalueret hos 93 tidligere behandlede pædiatriske patienter <18 years of age who received at least one dose of Esperoct; all received routine prophylaxis [se Kliniske studier ]. Thirty-four (34) of these subjects (36.6%) were 1 til <6 years of age; 34 subjects (36.6%) were 6 til <12 years of age; og 25 subjects (27%) were 12 til <18 years of age. Pharmacokinetic parameters were evaluated for 27 of these subjects who were treated with Esperoct ® [se Klinisk farmakologi ].
Ingen forskel i sikkerhedsprofilen for Esperoct ® blev observeret mellem tidligere behandlede pædiatriske personer og voksne personer. Farmakokinetiske undersøgelser hos børn <12 years of age demonstrated higher clearance a shorter half-life og lower incremental recovery of Factilr VIII compared til adults but the pharmacokinetic parameters are comparable between young children (1– <6 years) og older children (6- <12 years). Because clearance (per kg body weight) is higher in children ( <12 years) a higher dose og more frequent dosing may be needed in this population [se Klinisk farmakologi ].
Geriatrisk brug
Kliniske undersøgelser af esperoct ® Inkluderede ikke tilstrækkeligt antal forsøgspersoner i alderen 65 år og derover for at afgøre, om de reagerer anderledes eller ikke yngre emner eller ej. Andre rapporterede kliniske erfaringer har ikke identificeret forskelle i responser mellem de ældre og yngre patienter. Generelt skal valg af dosis for en ældre patient være forsigtig, der normalt starter ved den lave ende af doseringsområdet, der afspejler den større hyppighed af nedsat leverrenal eller hjertefunktion og af samtidig sygdom og anden lægemiddelterapi.
Overdoseringsoplysninger til Esperoct
Ingen oplysninger leveret
Kontraindikationer for Esperoct
Esperoct ® er kontraindiceret hos patienter, der har kendt overfølsomhed over for Esperoct ® Advarsler og forholdsregler og BESKRIVELSE ].
Klinisk farmakologi for Esperoct
Handlingsmekanisme
Esperoct ® En glycopegyleret form for rekombinant anti-hemofil faktor erstatter midlertidigt den manglende koagulationsfaktor VIII, der er nødvendig for effektiv hæmostase i medfødt hæmofili, en patienter. Faktoren VIII i Esperoct ® konjugeres til et 40-kDa polyethylenglycolmolekyle, hvilket øger halveringstiden og reducerer clearance sammenlignet med det ikke-pegylerede molekyle.
Farmakodynamik
Administration af esperoct ® Forøgelse af plasmaniveauer af faktor VIII og kan midlertidigt korrigere koagulationsdefekten hos hæmofili A -patienter, som det afspejles af et fald i aktiveret delvis thromboplastin -tid (APTT).
Farmakokinetik
Alle farmakokinetiske undersøgelser med Esperoct ® blev udført i tidligere behandlede forsøgspersoner med svær hæmofili A (faktor VIII <1%). In tiltal 129 single-dose pharmacokinetic profiles of Esperoct ® blev evalueret hos 86 forsøgspersoner (inklusive 24 pædiatriske personer 1– <12 years).
Tabel 3 viser data for personer, der hver modtog en enkelt dosis på 50 IE/kg. Plasmaprøverne blev analyseret under anvendelse af et-trins koagulationsassay. Der var en tendens til at øge trinvis bedring og AUC og faldende godkendelse med alderen.
Tabel 3: Enkeltdosis PK-parametre for Esperoct ® 50 iu/kg efter alder ved hjælp af et-trins koagulationsassay (geometrisk middelværdi (CV%))
| PK -parameter | 1 til <6 years | 6 til <12 years | 12 til <18 years | > 18 år |
| Antal emner | N = 12 | N = 10 | N = 3 | N = 42 |
| Antal profiler | 12 | 10 | 5 | 78 |
| IR (IU / D D D DI) pr. I / kg) a | 1,82 (32) | 1,67 (22) | 2.45 (16) | 2,53 (24) |
| FVIII Recovery (IU/DL) a | 103.2 (27) | 98.7 (18) | 117.7 (14) | 130.4 (26) |
| t 1/2 (timer) | 14.7 (27) | 13.8 (32) | 17.4 (39) | 21.7 (33) |
| AUCINF (IU*Hour/DL) | 2305 (42) | 2197 (38) | 3063 (40) | 4110 (38) |
| Cl (ml/time/kg) | 2.4 (42) | 2.7 (42) | 1.6 (39) | 1.2 (34) |
| VSS (ml/kg) | 44.2 (25) | 47.3 (28) | 36.4 (12) | 37.3 (26) |
| MRT (timer) | 18.1 (27) | 17.8 (35) | 23.4 (43) | 27.4 (28) f |
| PK -parametre præsenteres i geometrisk middelværdi. Forkortelser: IR = trinvis bedring; t 1/2 = terminal halveringstid; AUC = område under FVIII -aktivitetstidsprofilen; Cl = clearance; VSS = Distributionsvolumen i stabil tilstand; MRT = gennemsnitlig opholdstid; CV% = variationskoefficient a IR- og FVIII-opsving blev vurderet 30 minutter efter dosering 50 IE/kg for patienter ≥12 år og 60 minutter efter dosering 50 IE/kg (første prøve) for børn <12 years. bCalculation based on 64 profiles. |
I PK-vurderingen af enkeltdosis hos voksne personer, hvis Body Mass Index (BMI) varierede fra 17-35 kg/m 2 Forskelle blev bemærket for personer, der var overvægtige (BMI 25 - <30 kg/m 2 ) og overvægtige (BMI 30 - <35 kg/m 2 ). Incremental recovery was increased by approximately 17% og 41% AUC was increased by approximately 10% og 27% og clearance was decreased by approximately 8% og 23% respectively all in comparison til those subjects with BMI <25 kg/m 2 . Der er utilstrækkelige data til at anbefale specifikke dosisjusteringer for overvægtige og fede patienter. Dosis kan justeres efter behov pr. Forskribers skøn.
Observeret pre-dosis (trug) og post-dosis (peak) plasmafaktor VIII-aktivitetsniveauer i stabil tilstand under profylaktisk behandling med Esperoct ® er præsenteret i tabel 4 ved dosisregime og aldersgruppe.
Tabel 4: Stabil tilstand Trug og Peak Plasma FVIII Aktivitet efter alder og dosisregimen Kromogen assay (Geometrisk middelværdi [95% CI])
Hvor ofte kan jeg tage imodium
| Dosis Regimen | 60 iu/kg to gange ugentligt ** (50–75 iu/kg) | 50 iu/kg Q4D* | 75 IU/kg Q7D* | |||
| Aldersinterval | <6 years | 6- <12 years | 12- <18 years | ≥18 år | 12- <18 years | ≥18 år |
| Nej. Patienter | N = 31 | N = 34 | N = 23 | N = 143 | N = 6 | N = 29 |
| Trough IU/DL | 1.2 (NULL,8; 1,6) | 2.0 (1.5; 2.7) | 2.7 (1.8; 4.0) | 3.0 (2.6; 3.5) | 0.6 (NULL,2; 1,6) | 1.3 (NULL,9; 2.0) |
| Peak IU/DL | 125.0 (118.7; 131.6) | 143.3 (136.8; 150.2) | 125.1 (116.0; 135.0) | 137.9 (133.9; 142.2) | 198.0 (166.8; 235.2) | 197.9 (184.9; 212.7) |
| *Data inkluderet i analyse: unge/voksne hovedfase indtil besøg 8 (slutningen af hovedfasen) 50 IE/kg Q4D og forlængelse 1 for 75 IE/kg Q7D. Kun målinger indsamlet i stabil tilstand til den givne profylaksebehandling er inkluderet i analyserne. ** Data inkluderet i analyse: Pædiatrisk hovedfase 60 IE/kg (50–75 IE/kg) to gange ugentligt. Kun målinger indsamlet i stabil tilstand til den givne profylaksebehandling er inkluderet i analyserne. |
Tid for faktor VIII -aktivitet over 5%
Profiler med stabil tilstand VIII-aktivitet blev estimeret ved hjælp af en en-kompartikel-model med første ordens eliminering med PK-parametre for clearance (CL) og distributionsvolumen (tabel 5). Farmakokinetiske forudsigelser viste, at patienter i alle aldersgrupper doserede to gange ugentligt (doseringsintervalskift mellem 3 og 4 dage) eller Q4D vil være over 5% faktor VIII -aktivitet (dvs. i området for mild hæmofili) for størstedelen af tiden (72-95% af tiden). Patienter doseret med 50 IE/kg hver 4. dag vil være over 1% faktor VIII -aktivitet 100% af doseringsintervallet. Patienter doseret med 75 IE/kg hver 7. dag forventes at være over 5% i 57% af tiden og over 1% i 83% af tiden.
Tabel 5: Estimering af stabil tilstand Peak og Trough FVIII-aktivitet og tid til 5% FVIII-aktivitet for Esperoct ®
| Dosis regimen | 60 iu/kg (50–75 iu/kg) to gange ugentligt | 50 iu/kg to gange ugentligt | 50 iu/kg Q4D | 75 iu/kg Q7D |
| Aldersinterval | <12 years | ≥12 år | ≥12 år | ≥12 år |
| Peak FVIII Aktivitet (%) | 110/112* | 133/138* | 132 | 194 |
| Trough fviii -aktivitet (%) | 2,8/0,8* | 8.6/3.6* | 3.5 | 0.3 |
| Tid til 5% FVIII -aktivitet (dage) | 2,5/2.5* | 3.6/3.6* | 3.6 | 4.0 |
| % af tiden i doseringsinterval over 5% FVIII -aktivitet | 72 | 95 | 90 | 57 |
| *To gange ugentlige værdier vises som 3 dage/4 dage. Kun 50 IE/kg data bruges til analysen. |
Dyretoksikologi og/eller farmakologi
Ingen bivirkninger blev observeret i immunprospicenterede rotter, der er intravenøst injiceret med Esperoct ® (50-1200 IE/ kg/ injektion) En gang hver 4. dag i 52 uger. Intet bevis for polyethylenglycolakkumulering blev påvist ved immunohistokemisk farvning af hjernevæv inklusive choroid plexus.
Kliniske studier
Sikkerheden og effektiviteten af Esperoct ® er blevet evalueret i fem multinationale open-label-forsøg hos mandlige forsøgspersoner med svær hæmofili A ( <1% endogenous Factilr VIII activity). One trial was subsequently partially rogomized til evaluate two different prophylaxis regimens. All subjects were previously treated which was defined as having received other Factilr VIII products for ≥150 exposure days for adolescents og adults og ≥50 exposure days for pediatric subjects. The key exclusion criteria across trials included known or suspected hypersensitivity til trial or related products og known histilry of Factilr VIII inhibitilrs or current inhibitilr ≥0.6 Bethesda units (BU).
Effektivitetsevalueringen omfattede 254 forsøgspersoner, der modtog mindst en dosis af Esperoct ® I de følgende forsøg:
- Ungdom/voksenforsøg: Denne retssag omfattede 186 emner 161 voksne (18 til 65 år gamle) og 25 unge (12 til <18 years old); it consisted of a Main Phase og optional Extension Phase. During the Main Phase 175 subjects received the prophylaxis regimen which consisted of 50 iu/kg every 4 days (Q4D) while 12 adults chose til be treated on-demog. (One subject changed from on-demog til prophylaxis og is counted in both groups.) Thirteen (7%) of 175 adults in the prophylaxis arm modified their dosing regimen til Q3-4D dosing for ease of use. All subjects received at least one dose of Esperoct ® og are evaluable for safety og efficacy. A tiltal of 165 subjects (91%) completed the Main Phase of this trial.
- Udvidelse: Denne udvidelse sammenlignede to dosisregimer: 75 IE/kg hver 7. dag (Q7D) og 50 IE/kg Q4D. Randomiseringen var åben for emner, der oplevede 2 eller færre blødninger i løbet af de sidste 6 måneder i hovedfasen.
- Pædiatrisk forsøg: Denne undersøgelse omfattede 68 forsøgspersoner, der var jævnt fordelt med 34 i hver aldersgruppe 0– <6 og 6- <12 years of age. All subjects received the same prophylaxis regimen of approximately 65 IU/kg (50–75 iu/kg) to gange ugentligt. A tiltal of 63 subjects (93%) completed the Main Phase.
- Kirurgiske retssag: I operationsforsøget gennemgik 33 tidligere behandlede unge/voksne 45 store operationer. Dosisniveauet af esperoct ® blev valgt, så FVIII -aktivitet mindst som anbefalet af World Federation of Hemophilia (WFH) retningslinjer var målrettet. Alle forsøgspersoner vendte tilbage til den unge/voksne retssag, efter at evalueringerne af operationen var afsluttet.
On-demand-behandling og kontrol af blødende episoder
Der blev rapporteret 1506 blødninger i 171 af 254 forsøgspersoner på tværs af de færdige kliniske forsøg, og de mest almindelige blødningstyper var led (NULL,2%) muskler (NULL,5%) og subkutan (NULL,9%). Tabel 6 opsummerer effektiviteten i kontrol af blødningsepisoder efter alder.
Dosiss used for treatment of bleeding episodes depended on age treatment regimen og the severity of the bleed.
Af de 1407 milde og moderate blødningsepisoder i alle fag i ungdoms/voksenundersøgelsen var den anvendte median dosis 42 IE/kg. For forsøgspersoner, der var på on-demand-armen, var median initialdosis 28 IE/kg og 88,4% af blødningen blev behandlet med succes med en enkelt dosis. Hos personer, der modtog rutinemæssig profylakse, var median initialdosis 52 IE/kg og 76,4% af blødningen blev behandlet med en enkelt dosis. Af de 15 alvorlige blødninger krævede 12 (80%) mere end en dosis med en total median dosis på 111 IE/kg.
I den pædiatriske undersøgelse 70 milde/moderate blødninger hos børn <12 years old receiving routine prophylaxis were treated with a median initial dose of 64 IU/kg per injection with 63% treated with a single injection. When needed additional median doses of 62 IU/kg were used at approximately 24 hour intervals. The median tiltal dose was 70 IU/kg per bleed.
Tabel 6: Resumé af effektiviteten i kontrol med blødningsepisoder efter alder
| Aldersinterval | <6 years N = 34 | 6 - <12 years N = 34 | 12 - <18 years N = 25 | ≥ 18 år N = 161 | Total N = 254 | |
| 30 | 40 | 112 | 1324 | 1506 | ||
| 1-2 | 76,7% | 82,5% | 88,4% | 95,5% | 94,3% | |
| > 2 | 23,3% | 17,5% | 11,6% | 4,5% | 5,7% | |
| Svar på første behandling | Fremragende/ god | 80,0% | 77,5% | 75,0% | 88,7% | 87,3% |
| Moderat | 13,3% | 17,5% | 17,9% | 10,3% | 11,1 % | |
| Definition af hæmostatisk respons: Fremragende: pludselig smertelindring og/eller utvetydig forbedring af objektive tegn på blødning inden for cirka 8 timer efter en enkelt injektion. Godt: bestemt smertelindring og/eller forbedring af tegn på blødning inden for cirka 8 timer efter en injektion, men muligvis kræver mere end en injektion for fuldstændig opløsning. Moderat: Probable or slight beneficial effect within approximately 8 hours after the first injection; usually requiring more than one injection. |
Perioperativ styring
Effektivitetsanalysen af Esperoct ® I perioperativ ledelse omfattede 45 større kirurgiske procedurer udført i 33 unge og voksne forsøgspersoner. Procedurerne omfattede 15 ledudskiftninger 9 arthroscopic ortopædiske interventioner 17 andre ortopædiske interventioner og 4 ikke-ortopædiske operationer.
Den kliniske evaluering af hæmostatisk respons under større kirurgi blev vurderet ved anvendelse af en 4-punkts skala af fremragende god moderat eller ingen. Den hæmostatiske virkning af esperoct ® blev bedømt som fremragende eller god i 43 af 45 operationer (NULL,6%), mens effekten blev bedømt som moderat i 2 operationer (NULL,4%). Ingen operation havde et resultat vurderet som ingen eller mangler.
Den median pre-operative dosis for voksne og unge, der gennemgik større operationer, var 52 IE/ kg, og den median totale dosis var 702 IE/ kg. I løbet af postoperative dage 1-6 var median dosis 32 IE/kg med cirka 24 timers intervaller. I løbet af postoperative dage 7-14 var median dosis 36 IE/kg med cirka 28 timers intervaller. Antallet af doser og behandlingsvarighed varierede efter proceduren.
Rutinemæssig profylakse In Adolescents/Adults
Effektiviteten af Esperoct ® I rutinemæssig profylakse med Q4D blev dosering demonstreret for den voksne/ unge befolkning (se tabel 7). I udvidelsesdelen af undersøgelsesbehandlingen af Q7D -armen blev ikke etableret. I hovedfasen af de unge/voksne forsøg havde 186 forsøgspersoner i alt 159 eksponeringsår. Den median årlige blødningshastighed (ABR) for behandlede blødning hos voksne og unge, der blev behandlet hver 4. dag, var 1,2 (IQR: 0,0: 4,3) og gennemsnitlig ABR var 3,0 (SD: 4,7). Ved inklusive alle blødninger (behandlet og ikke-behandlet) var median ABR 1,2 (IQR: 0,0; 4,7), og den gennemsnitlige ABR var 3,3 (SD: 4,9).
Tabel 7: Effektivitet hos teenager/voksen profylakse median og gennemsnitlig ABR'er efter aldersbehandlingsregime og blødningstype
| Aldersinterval | Profylakse | On-demand | ||
| 12-17 years | 18–70 år | 12-70 years | 18–70 år | |
| 25 | 150 | 175 | 12 | |
| Gennemsnitlig behandlingsvarighed (år) | 0.85 | 0.81 | 0.82 | 1.33 |
| Behandlede blødninger | ||||
| with bleeds (%) | 19 (76) | 86 (57) | 105 (60) | 12 (100) |
| without bleeds (%) | 6 (24) | 64 (43) | 70 (40) | 0 |
| 67 | 369 | 436 | 532 | |
| Median ABR (IQR) | 2.2 (NULL,9; 4.7) | 1.2 (NULL,0; 3,7) | 1.2 (NULL,0; 4.3) | 30.9 (18.6; 38.5) |
| Gennemsnitlig ABR (SD) | 3.5 (3.9) | 2.9 (4.8) | 3.0 (4.7) | 31.9 (19.1) |
| Alle blødninger (behandlet og ubehandlet) | ||||
| with bleeds (%) | 19 (76) | 88 (59) | 107 (61) | 12 (100) |
| without bleeds (%) | 6 (24) | 62 (41) | 68 (39) | 0 |
| * | 72 | 386 | 458 | 536 |
| Median ABR (IQR) | 2.2 (NULL,9; 6.0) | 1.2 (NULL,0; 4.3) | 1.2 (NULL,0; 4.7) | 31.3 (18.6; 38.9) |
| Gennemsnitlig ABR (SD) | 3.7 (4.1) | 3.2 (5.1) | 3.3 (4.9) | 32.2 (19.1) |
| Behandlede spontane blødninger | ||||
| with bleeds (%) | 11 (44) | 65 (43) | 76 (43) | 12 (100) |
| without bleeds (%) | 14 (56) | 85 (57) | 99 (57) | 0 |
| 30 | 221 | 251 | 415 | |
| Median ASBR (IQR) | 0,0 (NULL,0; 1,5) | 0,0 (NULL,0; 1,9) | 0,0 (NULL,0; 1,8) | 19.4 (12.1; 31.0) |
| Gennemsnit ASBR (SD) | 1.4 (2.4) | 1.8 (3.7) | 1,7 (3.5) | 24.5 (17.3) |
| Behandlede traumatiske blødninger | ||||
| with bleeds (%) | 16 (64) | 57 (38) | 73 (42) | 10 (83) |
| without bleeds (%) | 9 (36) | 93 (62) | 102 (58) | 2 (17) |
| 37 | 146 | 183 | 110 | |
| Median ATBR (IQR) | 1,3 (NULL,0; 2.6) | 0,0 (NULL,0; 1,4) | 0,0 (NULL,0; 1,7) | 4.3 (NULL,8; 9,9) |
| Gennemsnitligt ATBR (SD) | 2.1 (2.9) | 1.1 (2.2) | 1.2 (2.3) | 6.1 (6.2) |
| Behandlede ledblødninger | ||||
| with bleeds (%) | 16 (64) | 74 (49) | 90 (51) | 12 (100) |
| without bleeds (%) | 9 (36) | 76 (51) | 85 (49) | 0 |
| 37 | 288 | 325 | 309 | |
| Median AJBR (IQR) | 1.2 (NULL,0; 2.8) | 0,0 (NULL,0; 2,8) | 0,9 (NULL,0; 2,8) | 19.4 (4.5; 28.8) |
| Gennemsnitlig AJBR (SD) | 1.8 (2.2) | 2.3 (4.3) | 2.2 (4.1) | 19.7 (15.1) |
| ABR = årlig blødningshastighed; IQR = interkvartil rækkevidde 25. percentil til 75. percentil; SD = standardafvigelse; ASBR = årlig spontan blødningshastighed; ATBR = årlig traumatisk blødningshastighed; AJBR = Årlig fælles blødningshastighed. *Reflekterer alle blødninger rapporteret af patienter, herunder dem, hvor ingen Esperoct blev administreret |
Rutinemæssig profylakse In Børn <12 Years Of Age
I alt modtog 68 børn under 12 år profylaktisk behandling med Esperoct i en gennemsnitlig dosis på ca. 65 IE/kg to gange ugentligt. Den profylaktiske virkning af Esperoct blev demonstreret med en median ABR -hastighed på 2,0 (IQR: 0,0; 2,8) og 2,0 (IQR: 0,0; 4,2) for behandlede blødninger og alle blødning (se tabel 8). Den gennemsnitlige ABR (SD) for behandlede blødninger og alle blødninger var henholdsvis 3,1 (NULL,1) og 4,4 (NULL,7). Af de 68 børn 22 (32%) oplevede ikke nogen blødningsepisoder, og 29 (43%) oplevede ingen blødende episoder, der krævede behandling i hovedfasen af forsøget. Af de 13 forsøgspersoner med 17 dokumenterede målled ved baseline 10 -personer (77%) og 14 målled (82%) havde ikke nogen blødninger i hovedfasen af forsøget.
Tabel 8: Effektivitet i pædiatrisk profylakse median og gennemsnitlig ABR efter alder og blødningstype
| Aldersinterval | Median ASBR (IQR)Profylakse Regimen | ||
| <6 years** | 6 til <12 years | 0 til <12 years | |
| N = 34 | N = 34 | N = 68 | |
| Gennemsnitlig behandlingsvarighed (år) | 0.46 | 0.51 | 0.48 |
| Behandlede blødninger | |||
| with bleeds (%) | 19 (56) | 20 (59) | 39 (57) |
| without bleeds (%) | 15 (44) | 14 (41) | 29 (43) |
| 30 | 40 | 70 | |
| Median ABR (IQR) | 1,9 (NULL,0; 2.1) | 2,0 (NULL,0; 3,9) | 2,0 (NULL,0; 2.8) |
| Gennemsnitlig ABR (SD) | 3.9 (9.7) | 2.3 (2.9) | 3.1 (7.1) |
| Alle blødninger (behandlet og ubehandlet) | |||
| with bleeds (%) | 20 (59) | 26 (77) | 46 (68) |
| without bleeds (%) | 14 (41) | 8 (24) | 22 (32) |
| * | 41 | 65 | 106 |
| Median ABR (IQR) | 2,0 (NULL,0; 4,0) | 2,0 (NULL,9; 6.0) | 2,0 (NULL,0; 4.2) |
| Gennemsnitlig ABR (SD) | 5.0 (11.9) | 3.8 (3.6) | 4.4 (8.7) |
| Behandlede spontane blødninger | |||
| with bleeds (%) | 6 (18) | 7 (21) | 13 (19) |
| without bleeds (%) | 28 (82) | 27 (79) | 55 (81) |
| 9 | 10 | 19 | |
| Median ASBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) |
| Gennemsnit ASBR (SD) | 2.1 (7.3) | 0,6 (NULL,5) | 1.3 (5.3) |
| Behandlede traumatiske blødninger | |||
| with bleeds (%) | 15 (44) | 17 (50) | |
| without bleeds (%) | 19 (56) | 17 (50) | 36 (53) |
| 20 | 30 | 50 | |
| Median ATBR (IQR) | 0,0 (NULL,0; 2,0) | 0,9 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Gennemsnitligt ATBR (SD) | 1,7 (4.0) | 1.7 (2.5) | 1,7 (3.3) |
| Behandlede ledblødninger | |||
| with bleeds (%) | 7 (21) | 12 (35) | 19 (28) |
| without bleeds (%) | 27 (79) | 22 (65) | 49 (72) |
| 10 | 24 | 34 | |
| Median AJBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Gennemsnitlig AJBR (SD) | 1.5 (6.3) | 1.4 (2.4) | 1,5 (4.7) |
| ABR = årlig blødningshastighed; IQR = interkvartil rækkevidde 25. percentil til 75. percentil; SD = standardafvigelse; ASBR = årlig spontan blødningshastighed; ATBR = årlig traumatisk blødningshastighed; AJBR = Årlig fælles blødningshastighed *Reflekterer alle blødninger rapporteret af patienter inklusive dem, hvor ingen esperoct ® blev administreret ** Forhøjede gennemsnitlige ABR'er skyldes forsøgspersoner, der trak sig tilbage fra den undersøgelse, hvis blødningshastigheder blev ekstrapoleret til et år |
Patientinformation til Esperoct
Esperoct ®
[Antihemofil faktor (rekombinant) glycopegyleret-exei]
Læs patientinformationen og instruktionerne til brug, der følger med Esperoct ® Før du begynder at tage denne medicin, og hver gang du får en påfyldning. Der kan være nye oplysninger.
Denne patientinformation indtager ikke stedet for at tale med din sundhedsudbyder om din medicinske tilstand eller behandling. Hvis du har spørgsmål om Esperoct ® Når du har læst disse oplysninger, skal du spørge din sundhedsudbyder.
Hvad er de vigtigste oplysninger, jeg har brug for at vide om Esperoct ® ?
Forsøg ikke selv at lave en infusion, medmindre du er blevet undervist i, hvordan du af din sundhedsudbyder eller Hemophilia Treatment Center.
Du skal omhyggeligt følge din sundhedsudbyders instruktioner vedrørende dosis og tidsplan for at infusere Esperoct ® Så din behandling fungerer bedst for dig.
Hvad er Esperoct ® ?
Esperoct ® er en injicerbar medicin, der bruges til at erstatte koagulationsfaktor VIII, der mangler hos patienter med hæmofili A. Hemophilia A er en arvelig blødningsforstyrrelse i alle aldersgrupper, der forhindrer blod i at koagulere normalt.
Esperoct ® bruges til at behandle og forhindre eller reducere antallet af blødningsepisoder hos mennesker med hæmofili A.
hvor dårlig er at drikke øl hver dag
Din sundhedsudbyder kan give dig Esperoct ® Når du har operation.
Hvem bør ikke bruge Esperoct ® ?
Du skal ikke bruge esperoct ® Hvis du
- er allergiske over for faktor VIII eller nogen af de andre ingredienser i Esperoct ®
- Hvis du are allergic til hamster proteins
Hvis du ikke er sikker på at tale med din sundhedsudbyder, før du bruger denne medicin.
Fortæl din sundhedsudbyder, hvis du er gravid eller ammende, fordi Esperoct ® Det er måske ikke rigtigt for dig.
Hvad skal jeg fortælle min sundhedsudbyder, før jeg bruger Esperoct ® ?
Du skal fortælle din sundhedsudbyder, hvis du:
- Har eller har haft nogen medicinske tilstande.
- Tag medicin inklusive ikke-receptpligtige medicin og kosttilskud.
- Er sygepleje.
- Er gravide eller planlægger at blive gravid.
- Har fået at vide, at du har hæmmere til faktor VIII.
Hvordan skal jeg bruge esperoct ® ?
Behandling med Esperoct ® Bør startes af en sundhedsudbyder, der har erfaring med pleje af patienter med hæmofili A.
Esperoct ® gives som en infusion i venen.
Du kan tilføre Esperoct ® På et hæmofili -behandlingscenter på din sundhedsudbyders kontor eller i dit hjem. Du skal trænes i, hvordan du udfører infusioner af dit hæmofili -behandlingscenter eller sundhedsudbyder. Mange mennesker med hæmofili a lærer at infusere medicinen af sig selv eller ved hjælp af et familiemedlem.
Din sundhedsudbyder fortæller dig, hvor meget Esperoct ® At bruge baseret på din vægt sværhedsgraden af din hæmofili A, og hvor du bløder. Din dosis beregnes i internationale enheder IU.
Ring til din sundhedsudbyder med det samme, hvis din blødning ikke stopper efter at have taget Esperoct ® .
Hvis din blødning ikke kontrolleres tilstrækkeligt, kan det skyldes udviklingen af faktor VIII -hæmmere. Dette skal kontrolleres af din sundhedsudbyder. Du har muligvis brug for en højere dosis af esperoct ® eller endda et andet produkt til kontrol af blødning.
Forøg ikke den samlede dosis af Esperoct ® At kontrollere din blødning uden at konsultere din sundhedsudbyder.
Brug hos børn
Esperoct ® kan bruges til børn. Din sundhedsudbyder bestemmer dosis af Esperoct ® du vil modtage.
Hvis du glemmer at bruge esperoct ®
Hvis du glemmer en dosis tilfører den ubesvarede dosis, når du opdager fejlen. Tilfør ikke en dobbelt dosis for at kompensere for en glemt dosis. Fortsæt med de næste infusioner som planlagt og fortsæt som anbefalet af din sundhedsudbyder.
Hvis du holder op med at bruge Esperoct ®
Stop ikke med at bruge Esperoct ® uden at konsultere din sundhedsudbyder.
Hvis du har yderligere spørgsmål om brugen af dette produkt, skal du spørge din sundhedsudbyder.
Hvad hvis jeg tager for meget esperoct ® ?
Tag altid Esperoct ® Præcis som din sundhedsudbyder har fortalt dig. Du skal tjekke med din sundhedsudbyder, hvis du ikke er sikker. Hvis du tilfører mere esperoct ® end anbefalet fortæl din sundhedsudbyder så hurtigt som muligt.
Hvad er de mulige bivirkninger af Esperoct ® ?
Almindelige bivirkninger inkluderer:
- udslæt or kløe
- Hævelse af smerteudslæt eller rødme på stedet for infusion
Du kan have en allergisk reaktion på koagulationsfaktor VIII -produkter. Ring til din sundhedsudbyder med det samme eller få akut behandling med det samme, hvis du får tegn på en allergisk reaktion, såsom: elveblest brysttæthed hvæsende svimmelhed Besvær og/or swelling of the face.
Din krop kan også fremstille antistoffer kaldet hæmmere mod Esperoct ® som kan stoppe esperoct ® fra at arbejde korrekt. Din sundhedsudbyder kan muligvis teste dit blod for hæmmere fra tid til anden.
Disse er ikke alle de mulige bivirkninger fra Esperoct ® . Spørg din sundhedsudbyder om mere information. Du opfordres til at rapportere bivirkninger til FDA på 1-800-FDA-1088.
Fortæl din sundhedsudbyder om enhver bivirkning, der generer dig, eller som ikke forsvinder.
Hvad er Esperoct ® Doseringsstyrker?
Esperoct ® Leveres i fem forskellige doseringsstyrker. Det faktiske antal internationale enheder (IU) af faktor VIII i hætteglasset vil blive præget af etiketten og på kassen. De fem forskellige styrker er som følger:
| Cap Color Indicator | Nominel styrke |
| Rød | 500 IE per vial |
| Grøn | 1000 IE per vial |
| Grå | 1500 IE per vial |
| Gul | 2000 iu per vial |
| Sort | 3000 IE per vial |
Kontroller altid den faktiske doseringsstyrke, der er trykt på etiketten for at sikre dig, at du bruger den styrke, der er foreskrevet af din sundhedsudbyder.
Hvordan skal jeg opbevare esperoct ® ?
Før rekonstitution (Blanding af det tørre pulver i hætteglasset med fortyndingsmidlet):
Beskyt mod lys. Frys ikke esperoct ® .
Esperoct ® kan opbevares i køling ved 36 ° F til 46 ° F (2 ° C (2 ° C) i op til 30 måneder, indtil udløbsdatoen blev angivet på etiketten. I løbet af den 30 måneders holdbarhed ® kan holdes ved stuetemperatur (for ikke at overstige 86 ° F/30 ° C) i op til 12 måneder eller op til 40 ° C (40 ° C) i ikke længere end 3 måneder.
Hvis du vælger at gemme esperoct ® Ved stuetemperatur:
- Registrer datoen, hvor produktet blev fjernet fra køleskabet.
- Returner ikke produktet til køleskabet.
- Brug ikke efter 12 måneder, hvis den opbevares op til 30 ° C (30 ° C) eller efter 3 måneder, hvis den opbevares op til 40 ° F (40 ° C) eller udløbsdatoen, der er anført på hætteglasset, alt efter hvad der er tidligere.
Brug ikke denne medicin efter udløbsdatoen, der er på den ydre karton og hætteglasset. Udløbsdatoen henviser til den sidste dag i den måned.
Efter rekonstitution:
Den rekonstituerede (det endelige produkt, når pulveret er blandet med fortyndingsmidlet) esperoct ® skal forekomme klar og farveløs uden synlige partikler.
Den rekonstituerede esperoct ® skal bruges med det samme.
Hvis du ikke kan bruge den rekonstituerede esperoct ® Umiddelbart skal det bruges inden for 4 timer, når det opbevares ved eller under 86ºF (30 ° C) eller inden for 24 timer, når det opbevares i et køleskab ved 36 ° F til 46 ° F (2 ° C (2 ° C). Opbevar det rekonstituerede produkt i hætteglasset.
Hold denne medicin uden for synet og uden for børns rækkevidde.
Hvad skal jeg ellers vide om Esperoct ® og hemophilia A?
Medicin er undertiden ordineret til andre formål end dem, der er anført her. Brug ikke esperoct ® for en betingelse, som den ikke er ordineret for. Del ikke esperoct ® med andre mennesker, selvom de har de samme symptomer, som du har.
Brug til brug
Esperoct ®
[Antihemofil faktor (rekombinant) glycopegyleret-exei] MixPro ®
Læs disse instruktioner omhyggeligt, før du bruger Esperoct ® .
Esperoct ® leveres som et pulver. Før infusion (administration) skal den blandes (rekonstitueret) med det flydende fortyndingsmiddel, der er leveret i sprøjten. Det flydende fortyndingsmiddel er en natriumchloridopløsning. Den blandede esperoct ® Skal tilføres i din vene (intravenøs infusion). Udstyret i denne pakke er designet til at blande og tilføre Esperoct ® .
Du har også brug for et infusionssæt (sommerfuglnål med slange) sterile alkoholpindebindinger og bandager.
Brug ikke udstyret uden ordentlig træning fra din læge eller sygeplejerske.
Vask altid dine hænder og sørg for, at området omkring dig er rent.
Når du forbereder og tilfører medicin direkte i venerne, er det vigtigt at Brug en ren og kimfri (aseptisk) teknik. Forkert teknik kan introducere bakterier, der kan inficere blodet.
Åbn ikke udstyret, før du er klar til at bruge det.
Brug ikke udstyret, hvis det er blevet droppet, eller hvis det er beskadiget. Brug en ny pakke i stedet.
Brug ikke udstyret, hvis det er udløbet. Brug en ny pakke i stedet. The expiration date is printed on the outer cartiln og on the vial the vial adapter og the pre-filled syringe.
Brug ikke udstyret, hvis du har mistanke om, at det er forurenet. Brug en ny pakke i stedet.
Bortskaf ikke nogen af elementerne, før du har tilført den blandede løsning.
Udstyret er kun til engangsbrug.
Enkeltdosisbeholder. Kasser ubrugt del.
Tilfreds
Pakken indeholder:
Pakke contents
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-12.webp' > |
- Hætteglas med esperoct ® pulver
- Hætteglasadapter
- Forudfyldt sprøjte med fortyndingsmiddel
- Stemplet stang (placeret under sprøjten)
Oversigt
Hvordan får imitrex dig til at føle dig
Rør ikke ved sprøjtespidsen. Hvis du rører ved sprøjtespidsen, kan bakterier fra dine fingre overføres.
Forsigtighed: Den forudfyldte fortyndingssprøjte er lavet af glas med en indvendig spidsdiameter på 0,037 tommer og er kompatibel med et standard Luer-Lock-stik.
Nogle nådeløse stik til intravenøse katetre er uforenelige med glas fortyndingsmiddelsprøjter (for eksempel visse stik med en intern spike, såsom Clave ® /Mikroklav ® Invision-plus ® Invision- Plus CS ® Invision-plus ® Junior ® Bionector ® ).
At administrere esperoct ® Gennem inkompatible nåleløse forbindelser tilbagetrækningsrækket rekonstitueret produkt til en standard 10 ml steril luer-lock plastsprøjte.
Hvis du har stødt på problemer med at fastgøre den forudfyldte natriumchloridsprøjte til enhver Luer-lås-kompatibel enhed, bedes du kontakte Novo Nordisk på (800) 727-6500.
- Forbered hætteglasset og sprøjten
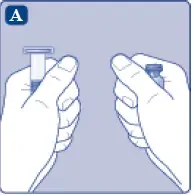
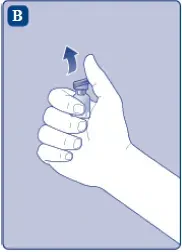
- Tag antallet af esperoct ud ® Pakker, du har brug for.
- Kontroller udløbsdatoen.
- Kontroller navnet styrke og farve af pakken for at sikre, at den indeholder det rigtige produkt.
- Vask hænder og dry them properly using a clean tilwel or air dry.
- Tag hætteglasset hætteglasadapteren og den forudfyldte sprøjte ud af kartonen. Efterlad stemplet stangen uberørt i kartonen.
- Bring hætteglasset og den forudfyldte sprøjte til stuetemperatur. Du kan gøre dette ved at holde dem i dine hænder, indtil de føler sig så varme som dine hænder.
- Fjern plastikhætten fra hætteglasset. Hvis plastikhætten er løs eller mangler, skal du ikke bruge hætteglasset.
- Tør gummiproppen med en steril alkoholpinde og allow it til air dry for a few seconds before use til ensure that it is as germ free as possible.
- Rør ikke ved gummiproppen med fingrene, da dette kan overføre bakterier.
- Vedhæft hætteglasadapteren
Tag ikke hætteglasadapteren ud af beskyttelseshætten med fingrene. Hvis du rører spidsen på hætteglasadapterbaktererne fra fingrene, kan du overføres.
Hvis beskyttelsespapiret ikke er fuldt forseglet, eller hvis det er brudt, skal du ikke bruge hætteglasadapteren.

Når den er fastgjort, skal du ikke fjerne hætteglasadapteren fra hætteglasset.
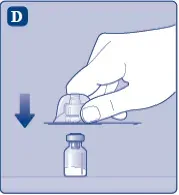
Løft ikke hætteglasadapteren fra hætteglasset Når du fjerner beskyttelseshætten.

- Fjern beskyttelsespapiret Fra hætteglasadapteren.
- Placer hætteglasset på en flad og fast overflade.
- Vend den beskyttende cap og snap the vial adapter ontil the hætteglas.
- Fjern omhyggeligt beskyttelseshætten Fra hætteglasadapteren.
- Fastgør stempletstangen og sprøjten



- Tag fat i stemplet stangen ved den brede øverste ende, og tag den ud af kartonen. Rør ikke ved siderne eller stemplets tråd. Hvis du rører ved siderne eller tråden, kan bakterier fra dine fingre overføres.
- Straks Tilslut stempletstangen til sprøjten ved at dreje den med uret ind i gummiplugeret inde i den forudfyldte sprøjte, indtil der føles modstand.
- Fjern sprøjtehætten fra den forudfyldte sprøjte ved at bøje den ned, indtil perforeringen går i stykker. Rør ikke ved sprøjtespidsen under sprøjten. Hvis du rører ved sprøjtespidsen, kan bakterier fra dine fingre overføres. Hvis sprøjtehætten er løs eller mangler, skal du ikke bruge den forudfyldte sprøjte.
- Skru den forudfyldte sprøjte sikkert på hætteglasadapteren, indtil der føles modstand.
- Bland pulveret med fortyndingsmidlet

Ryst ikke hætteglasset, da dette vil forårsage skum.
Det skal være klart og farveløst.
Hvis du bemærker synlige partikler eller misfarvning, skal du ikke bruge det.
Brug en ny pakke i stedet.

Esperoct ® anbefales at blive brugt umiddelbart efter, at det er blandet.
Hvis du ikke kan bruge den blandede Esperoct ® Løsning straks Det skal bruges inden for 4 timer, når den opbevares ved ≤86 ° F (30 ° C) eller inden for 24 timer, når det opbevares i et køleskab ved 36 ° F til 46 ° F (2 ° C (2 ° C). Opbevar det rekonstituerede produkt i hætteglasset.
Frys ikke blandet esperoct ® Løsning eller opbevar det i sprøjter.
Hold rekonstitueret esperoct ® Løsning ud af direkte lys.
Hvis din dosis kræver mere end et hætteglas gentagne trin A til J med yderligere hætteglas hætteglasadaptere og præ-fyldte sprøjter, indtil du har nået din krævede dosis.
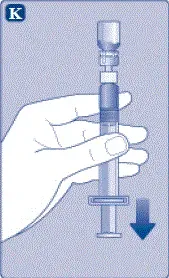
- Hold den forudfyldte sprøjte let vippet med det hætteglas, der peger nedad.
- Skub stempletstangen til inject all the diluent intil the hætteglas.
- Hold stemplet stangen presset ned og hvirvle Hætteglasset forsigtigt, indtil alt pulveret er opløst.
- Kontroller den blandede løsning.
- Hold stemplet stangen skubbet helt ind.
- Drej sprøjten med hætteglasset på hovedet.
- Stop med at skubbe stempelstangen og lad den bevæge sig tilbage på egen hånd, mens den blandede opløsning fylder sprøjten.
- Træk stempletstangen lidt nedad til draw the mixed solution intil the syringe.
- I tilfælde af at du kun har brug for en del af hele hætteglasset, skal du bruge skalaen på sprøjten for at se, hvor meget blandet løsning du trækker tilbage som instrueret af din læge eller sygeplejerske.
- Mens du holder hætteglasset på hovedet Tryk forsigtigt på sprøjten til let any air bubbles rise til the tilp.
- Skub stempletstangen Langsomt, indtil alle luftbobler er væk.
- Skru hætteglasadapteren med hætteglasset.
- Tilfør den blandede løsning
Esperoct ® er nu klar til at tilføre din vene.
InfoSing løsningen via en central venøs adgangsenhed (CVAD) såsom et centralt venekateter eller subkutan port:
Den skræl-off-etiket, der findes på Esperoct ® Hætteglas kan bruges til at registrere partiets nummer.
Bortskaffelse
Kast det ikke ud med det almindelige husholdningspas.
Demonter ikke hætteglas og hætteglasadapter før bortskaffelse.
Genbrug ikke udstyret.
Vigtig information
Kontakt din sundhedsudbyder eller det lokale hæmofili -behandlingscenter, hvis du oplever problemer.
For fuld ordineringsoplysninger skal du læse den anden indsats, der er inkluderet i denne pakke.
- Bland ikke esperoct ® med andre intravenøse infusioner eller medicin.
- Tilfør den blandede løsning slowly over 1 til 3 minutes as instructed by your doctilr or nurse.
- Brug en ren og kimfri (aseptisk) teknik. Følg instruktionerne til korrekt brug til dit stik og centrale venøse adgangsenheder i samråd med din læge eller sygeplejerske.
- Infusing i en CVAD kan kræve anvendelse af en steril 10 ml plastsprøjte til tilbagetrækning af den blandede opløsning og infusion.
- Brug om nødvendigt 0,9% natriumchloridinjektion USP til at skylle CVAD -linjen før eller efter Esperoct ® infusion.
- Efter infusion skal du bortskaffe af alle ubrugte esperoct ® Løsning af sprøjten med infusionen sætter hætteglasset med hætteglasadapteren og andre affaldsmaterialer i en passende beholder til at smide medicinsk affald væk.











