Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
ProgestinerKyleena
Resume af lægemiddeloversigt
Hvad er Kyleena?
Kyleena (Levonorgestrel -frigørelse af intrauterint system) er et progestin -indeholdende intrauterint system (IU'er), der er angivet til forebyggelse af graviditet i op til 5 år.
Hvad er bivirkninger af Kyleena?
Kyleena kan forårsage alvorlige bivirkninger, herunder:
- øget vaginal blødning
- mavesmerter eller bækkensmerter
- Udvisningsvaluta
- acne og
- menstruationskramper
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Almindelige bivirkninger af Kyleena inkluderer:
- Vaginal kløe og udledning
- Ovariecyster
- mavesmerter
- Bekken smerter
- hovedpine eller migræne
- Acne
- Abdominale kramper
- brystsmerter eller ubehag
- øget vaginal blødning
- depression og
- hårtab.
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; og pludselig svimmelhed letthed eller udlevering;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til Kyleena
Kyleena indsættes af en uddannet sundhedsudbyder. Udgivelseshastigheden for Levonorgestrel (LNG) i Kyleena er 17,5 mcg/dag efter 24 dage og falder til 7,4 mcg/dag efter 5 år; Kyleena skal fjernes eller udskiftes efter 5 år.
hvor meget wellbutrin er i modsætning
Hvilke stoffer stoffer eller kosttilskud interagerer med Kyleena?
Kyleena kan interagere med andre stoffer. Fortæl din læge alle medicin og kosttilskud, du bruger.
Kyleena under graviditet og amning
Fortæl din læge, hvis du er gravid, før du bruger Kyleena. Kyleena anbefales ikke til brug under graviditet. Kyleena skal fjernes, hvis graviditet opstår med Kyleena på plads. Kontakt din læge inden amning.
Yderligere oplysninger
Vores Kyleena (Levonorgestrel-frigivende intrauterine system) Bivirkninger Drug Center giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
Beskrivelse for Kyleena
Kyleena (Levonorgestrel-frigivende intrauterin-system) indeholder 19,5 mg LNG en progestin og er beregnet til at tilvejebringe en indledende frigørelsesrate på ca.17,5 mcg/dag LNG efter 24 dage.
Levonorgestrel USP (-)-13-ethyl-17-hydroxy-1819-Dinor-17a-pregn-4-en-20-syn-3-en Den aktive ingrediens i Kyleena har en molekylvægt på 312,4 En molekylformel på C 21 H 28 O 2 og følgende strukturelle formel:
 |
Kyleena
Kyleena consists of a T-shaped polyethylene frame (T-body) with a steroid reservoir (hormone elastomer core) around the vertical stem. The white T-body has a loop at one end of the vertical stem og two horizontal arms at the other end. The reservoir consists of a whitish or pale yellow cylinder made of a mixture of LNG og silicone (polydimethylsiloxane) containing a total of 19.5 mg LNG. The reservoir is covered by a semi-opaque silicone membrane composed of polydimethylsiloxane og colloidal silica. A ring composed of 99.95% pure silver is located at the top of the vertical stem close to the horizontal arms og is visible by ultrasound. The polyethylene of the T-body is compounded with barium sulfate which makes it radiopaque. A monofilament blue polypropylene removal thread is attached to a loop at the end of the vertical stem of the T-body. The polypropylene of the removal thread contains <0.5% phthalocyaninato(2-) copper as a colorant (see Figure 10).
Kyens komponenter inklusive dens emballage fremstilles ikke ved hjælp af naturgummi latex.
Figur 10: Kyleena
 |
Inserter
Kyleena is packaged sterile within an inserter. The inserter (Figure 11) which is used for insertion of Kyleena into the uterine cavity consists of a symmetric two-sided body og slider that are integrated with flange lock pre-bent insertion tube og plunger. The outer diameter of the insertion tube is 3.8 mm. The vertical stem of Kyleena is loaded in the insertion tube at the tip of the inserter. The arms are pre-aligned in the horizontal position. The removal threads are contained within the insertion tube og hogle. Once Kyleena has been placed the inserter is discarded.
Figur 11: Diagram over Inserter
 |
Bruger til Kyleena
Kyleena is indicated to prevent pregnancy for up to 5 years. Replace the system after 5 years if continued use is desired.
Dosering til Kyleena
Dosering over tid
Kyleena contains 19.5 mg of Levonorgestrel (LNG) released forgæves med en hastighed på cirka 17,5 mcg/dag efter 24 dage. Denne sats falder gradvist til 9,8 mcg/dag efter 1 år og til 7,4 mcg/dag efter 5 år. Gennemsnittet forgæves Udgivelseshastigheden på LNG er cirka 12,6 mcg/dag i det første år og 9,0 mcg/dag over en periode på 5 år. [Se Klinisk farmakologi ]
Kyleena must be removed by the end of the fifth year og can be replaced at the time of removal with a new Kyleena if continued contraceptive protection is desired.
Kyleena can be physically distinguished from other intrauterine systems (IUSs) by the combination of the visibility of the silver ring on ultrasound og the blue color of the removal threads.
Kyleena is supplied in a sterile package within an inserter that enables single-hoged loading (see Figure 1). Do not open the package until required for insertion [see BESKRIVELSE ]. Brug ikke, hvis tætningen af den sterile pakke er brudt eller ser ud til at være kompromitteret. Brug strenge aseptiske teknikker i hele indsættelsesproceduren [se Advarsler og forholdsregler ].
 |
Insertionsinstruktioner
- Få en komplet medicinsk og social historie for at bestemme tilstande, der kan have indflydelse på valget af et levonorgestrel-frigivende intrauterint system (LNG IU'er) til prævention. Hvis indikeret udfører en fysisk undersøgelse og passende tests for enhver former for kønsorgan eller andre seksuelt overførte infektioner. [Se Kontraindikationer og Advarsler og forholdsregler ] Fordi uregelmæssig blødning/plet er almindelig i løbet af de første måneder af Kyleena -brug, ekskluder endometrial patologi (polypper eller kræft) inden indsættelse af Kyleena hos kvinder med vedvarende eller ukarakteristisk blødning [Se Advarsler og forholdsregler ].
- Følg indsættelsesinstruktionerne nøjagtigt som beskrevet for at sikre korrekt placering og undgå for tidlig frigivelse af Kyleena fra inserteren. Når den er frigivet, kan Kyleena ikke indlæses igen.
- Kontroller udløbsdatoen for Kyleena inden indsættelse af indsættelse.
- Kyleena should be inserted by a trained healthcare provider. Healthcare providers should become thoroughly familiar with the insertion instructions before attempting insertion of Kyleena.
- Indsættelse kan være forbundet med nogle smerter og/eller blødning eller vasovagale reaktioner (for eksempel synkope bradykardi) eller med anfald især hos patienter med en disponering for disse tilstande. Overvej at administrere smertestillende midler inden indsættelse.
Tidspunkt for indsættelse
Tabel 1: Hvornår skal man indsætte Kyleena
| Start Kyleena hos kvinder, der ikke i øjeblikket bruger hormonel eller intrauterin prævention |
|
| Skift til Kyleena fra en oral transdermal eller vaginal hormonel prævention |
|
| Skift til Kyleena fra en injicerbar progestin -prævention |
|
| Skift til Kyleena fra et præventionsimplantat eller et andet IU'er |
|
| Indsættelse af Kyleena efter første trimesterabort eller spontanabort |
|
| Indsættelse af Kyleena efter fødsel eller abort i anden trimester eller spontanabort | |
|
|
| Intervalsindsættelse efter fuldstændig involvering af livmoderen |
|
Værktøjer til indsættelse
Note
Inserteren forsynet med Kyleena (se figur 1) og indsættelsesproceduren, der er beskrevet i dette afsnit, gælder ikke til øjeblikkelig indsættelse efter fødsel eller abort eller abort fra anden trimester eller spontanabort. For øjeblikkelig indsættelse skal du fjerne Kyleena fra inserteren ved første belastning (se figur 2) og derefter frigive (se figur 7) Kyleena fra Inserter og indsæt i henhold til accepteret praksis.
Forberedelse
- Handsker
- Spekulum
- Steril livmoderlyd
- Steril tenaculum
- Antiseptisk løsningsapplikator
Procedure
- Sterile handsker
- Kyleena with inserter in sealed package
- Instrumenter og anæstesi til paracervikal blok, hvis forventet
- Overvej at have en uåbnet back-up Kyleena tilgængelig
- Steril skarp buet saks
Forberedelse for insertion
- Ekskluder graviditet og bekræft, at der ikke er andre kontraindikationer til brugen af Kyleena.
- Med patienten komfortabelt i lithotomi -position, foretager du en bimanuel eksamen for at etablere livmoderens størrelsesform og placering.
- Indsæt forsigtigt et spekulum for at visualisere livmoderhalsen.
- Rens grundigt livmoderhalsen og vagina med en passende antiseptisk opløsning.
- Forbered dig på at lyde livmoderhulen. Tag fat i livmoderhalsen med en tenaculum pincet, og påfør forsigtigt trækkraft for at stabilisere og justere livmoderhalskanalen med livmoderhulen. Udfør en paracervisk blok, hvis nødvendigt. Hvis livmoderen er retroverted, kan det være mere passende at forstå livmoderhalsen i livmoderhalsen. Tenaculum skal forblive i position, og blid trækkraft på livmoderhalsen skal opretholdes under hele indsættelsesproceduren.
- Indsæt forsigtigt en livmoderlyd for at kontrollere livmoderhalsen på livmoderhalsen Mål dybden af livmoderhulen i centimeter bekræfter hulrumsretningen og detekterer tilstedeværelsen af enhver livmoderanomali. Hvis du støder på vanskeligheder eller livmoderhalsstenose, skal du bruge dilatation og ikke tvinge til at overvinde resistens. Hvis der kræves cervikal dilatation, skal du overveje at bruge en paracervikal blok.
Indsættelsesprocedure
Fortsæt med indsættelse først efter at have afsluttet ovenstående trin og konstatering af, at patienten er passende for Kyleena.
Sørg for brug af aseptisk teknik gennem hele proceduren.
Trin 1 - åbning af pakken
Figur 1. Åbning af Kyleena -pakken
 |
- Åbn pakken (figur 1). Indholdet af pakken er steril.
- Brug af sterile handsker løft håndtaget på den sterile inserter og fjern det fra den sterile pakke.
Trin 2 - Læs Kyleena ind i indsættelsesrøret
Figur 2. Flyt skyderen helt til den forreste position for at indlæse Kyleena
 |
- Skub skyderen forward Så vidt muligt i retning af pilen og bevæger sig og bevæger indsættelsesrøret over Kyleena T-krop for at indlæse Kyleena i indsættelsesrøret (figur 2). Tipene til armene mødes for at danne en afrundet ende, der strækker sig lidt ud over indsættelsesrøret.
- Oprethold fremadtrykket med tommelfingeren eller pegefingeren på skyderen. Flyt ikke skyderen nedad på dette tidspunkt, da dette kan for tidligt frigive Kyleenas tråde. Når skyderen er flyttet under Mark Kyleena ikke kan indlæses igen.
Trin 3 - sætning af flangen
- At holde skyderen i denne fremadrettede position indstil den øvre kant af flangen for at svare til livmoderdybden (i centimeter) målt under lyden (figur 3).
Figur 3. Indstilling af flangen
 |
Trin 4 - Kyleena er nu klar til at blive indsat
- Fortsæt med at holde skyderen i denne fremadrettede position. Fremfør inserteren gennem livmoderhalsen, indtil flangen er ca. 1,5-2 cm fra livmoderhalsen og derefter pauser (figur 4).
Figur 4. Fremme indsættelsesrør, indtil flangen er 1,5 til 2 cm fra livmoderhalsen
 |
Tving ikke indvendigt. Om nødvendigt udvidet livmoderhalskanalen.
Trin 5 - åbnede armene
- Mens du holder indorteren stabil Flyt skyderen ned til mærket At frigive armene fra Kyleena (figur 5). Vent 10 sekunder på, at de vandrette arme åbnes fuldstændigt.
Figur 5. Flyt skyderen tilbage til mærket for at frigive og åbne armene
 |
Trin 6 - Advance til Fundal Position
Fremfør inserteren forsigtigt mod livmoderens fundus Indtil flangen berører livmoderhalsen. Hvis du støder på fundal modstand, skal du ikke fortsætte med at gå videre. Kyleena er nu i den fundale position (figur 6). Fundal positionering af Kyleena er vigtig for at forhindre udvisning.
Figur 6. Flyt Kyleena i den fundale position
 |
Trin 7 -frigivelse Kyleena og trækker indvendige indvendige
Figur 7. Flyt skyderen helt ned for at frigive Kyleena fra indsættelsesrøret
 |
Figur 8. Skæring af trådene
 |
- Holder hele indsatser fast på plads, frigør Kyleena ved at flytte Skyderen helt ned (Figur 7).
- Fortsæt med at holde skyderen helt ned, mens du langsomt og forsigtigt trækker indføreren tilbage fra livmoderen.
- Brug af en skarp buet saks klip trådene Vinkelret, der forlader ca. 3 cm synlig uden for livmoderhalsen [skæretråde i en vinkel, kan efterlade skarpe ender (figur 8)]. Påfør ikke spændinger eller træk på trådene, når du skærer for at forhindre fortrængning af Kyleena.
Kyleena insertion is now complete. Prescribe analgesics if indicated. Record the Kyleena lot number in the patient records.
Vigtig information at overveje under eller efter indsættelse
- Hvis du har mistanke om, at Kyleena ikke er i placering af den rigtige positionskontrol (for eksempel ved hjælp af transvaginal ultralyd). Fjern Kyleena, hvis det ikke er placeret helt i livmoderen. Gensæt ikke en fjernet Kyleena igen.
- Hvis der er klinisk bekymring, kan en ekstraordinær smerte eller blødning under eller efter indsættelse tage passende skridt (såsom fysisk undersøgelse og ultralyd) straks for at udelukke perforering.
Patientopfølgning
- Reeksamin og evaluere patienter 4 til 6 uger efter indsættelse og en gang om året derefter eller hyppigere, hvis det er klinisk indikeret.
Fjernelse af Kyleena
Tidspunkt for fjernelse
- Kyleena should not remain in the uterus after 5 years.
- Hvis graviditet ikke ønskes, skal du fjerne Kyleena i løbet af de første 7 dage af menstruationscyklussen, forudsat at kvinden stadig oplever regelmæssige menstruation. Hvis fjernelse vil forekomme på andre tidspunkter i løbet af cyklussen, eller kvinden ikke oplever regelmæssige menstruation, er hun i fare for graviditet; Start en ny præventionsmetode en uge før fjernelse af disse kvinder. [Se Fortsættelse af prævention efter fjernelse ]
Værktøjer til fjernelse
Forberedelse
- Handsker
- Spekulum
Procedure
- Sterile tang
Fjernelse af proceduren
Figur 9. Fjernelse af Kyleena
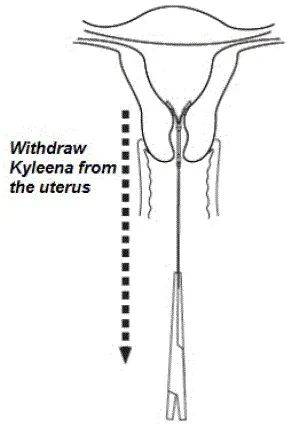
- Fjern Kyleena ved at påføre blid trækkraft på trådene med pincet (figur 9).
- Hvis trådene ikke er synlige, skal du bestemme placering af Kyleena ved ultralyd [se Advarsler og forholdsregler ].
- Hvis det konstateres, at Kyleena er i livmoderhulen på ultralydseksamen, kan det fjernes ved hjælp af en smal pincet, såsom en alligator -tang. Dette kan kræve udvidelse af cervikalkanalen. Efter fjernelse af Kyleena undersøges systemet for at sikre, at det er intakt.
- Hvis det ikke er i stand til at fjerne med blid trækkraft, skal du bestemme Kyleena -placering og udelukke perforering med ultralyd eller anden billeddannelse [se Advarsler og forholdsregler ].
- Fjernelse kan være forbundet med nogle:
- Smerter og/eller blødning eller vasovagale reaktioner (for eksempel synkope bradykardi) eller anfald især hos patienter med en disponering for disse tilstande.
- brud eller indlejring af Kyleena i myometrium, der kan gøre fjernelse vanskelig [se Advarsler og forholdsregler ]. Analgesia paracervical anesthesia cervical dilation alligator forceps or other grasping instrument or hysteroscopy may be used to assist in removal.
Fortsættelse af prævention efter fjernelse
- Hvis graviditet ikke ønskes, og hvis en kvinde ønsker at fortsætte med at bruge Kyleena, kan et nyt system indsættes umiddelbart efter fjernelse når som helst i løbet af cyklussen.
- Hvis en patient med regelmæssige cyklusser ønsker at starte en anden præventionsmetodetid fjernelse og initiering af den nye metode for at sikre kontinuerlig prævention. Fjern enten Kyleena i løbet af de første 7 dage af menstruationscyklussen, og start den nye metode straks derefter eller start den nye metode mindst 7 dage før fjernelse af Kyleena, hvis fjernelse skal forekomme på andre tidspunkter i løbet af cyklussen.
- Hvis en patient med uregelmæssige cyklusser eller amenoré ønsker at starte en anden præventionsmetode, skal du starte den nye metode mindst 7 dage før fjernelse.
Hvor leveret
Doseringsformularer og styrker
Kyleena er en LNG-frigivende IU'er (en type intrauterin enhed eller IUD), der består af en T-formet polyethylenramme med et steroidreservoir indeholdende i alt 19,5 mg LNG.
Opbevaring og håndtering
Kyleena (Levonorgestrel -frigivende intrauterint system) indeholdende i alt 19,5 mg LNG fås i en karton med en steril enhed - NDC
Kyleena is supplied sterile. Kyleena is sterilized with ethylene oxide. Do not resterilize. For single use only. Do not use if the inner package is damaged or open. Insert before the end of the month shown on the label.
Opbevares ved 25 ° C (77 ° F); med udflugter tilladt mellem 15–30 ° C (59–86 ° F) [se USP -kontrolleret stuetemperatur].
Fremstillet til: Bayer Healthcare Pharmaceuticals Inc. Whippany NJ 07981. Revideret: mar 2023
Bivirkninger for Kyleena
Følgende alvorlige eller på anden måde vigtige bivirkninger diskuteres andetsteds i mærkningen:
- Ektopisk graviditet [se Advarsler og forholdsregler ]
- Intrauterin graviditet [se Advarsler og forholdsregler ]
- Gruppe A Streptococcal Sepsis (GAS) [Se Advarsler og forholdsregler ]
- Bækkeninflammatorisk sygdom [se Advarsler og forholdsregler ]
- Perforering [se Advarsler og forholdsregler ]
- Udvisning [se Advarsler og forholdsregler ]
- Ovariecyster [se Advarsler og forholdsregler ]
- Blødningsmønsterændringer [se Advarsler og forholdsregler ]
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, kan der ikke sammenlignes bivirkninger, der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte med hastigheder i de kliniske forsøg med et andet lægemiddel og afspejler muligvis ikke de hastigheder, der er observeret i klinisk praksis.
Dataene beskrevet nedenfor afspejler eksponeringen af 1697 sunde 18 til 41-årige kvinder (middelalder 27,8 ± 5,2 år) for Kyleena. Disse data kommer fra to multicenter-præventionsforsøg: En fase 2-undersøgelse med en 3-årig varighed blev udført i Europa, der tilmeldte sig generelt sunde 21 til 41-årige kvinder; 217 forsøgspersoner blev udsat for Kyleena i et år og 174 afsluttede tre år. Dataene i dette forsøg dækker cirka 8000 eksponeringscyklusser. En fase 3-undersøgelse med en 3-årig varighed og en valgfri forlængelse af Kyleena-brugen op til 5 år blev udført i USA (US) Canada Europa og Latinamerika. Befolkningen var generelt sund 18 til 35-årige kvinder. I alt 1208 forsøgspersoner blev udsat for Kyleena i mindst et år; 707 kvinder gik ind i den valgfri udvidelsesfase efter 3 år og 550 afsluttede fem år. Dataene i dette forsøg dækker cirka 60000 cyklusser.
I alt for begge undersøgelser blev 1425 forsøgspersoner udsat i mindst 1 år og 550 forsøgspersoner afsluttet 5 års brug. Af de samlede 1697 -forsøgspersoner, der blev udsat for Kyleena 563, var fra USA og 1134 var fra Europa Canada og Latinamerika; 623 (37%) var nulliparøse (middelalder 24,6 ± 4,5 år) og 1074 (63%) var parous (middelalder 29,7 ± 4,7 år). De fleste kvinder, der modtog Kyleena, var kaukasiske (83%) eller sort/afroamerikaner (NULL,4%); 9,4% af kvinderne var af spansktalende etnicitet. De kliniske forsøg havde ingen øvre eller nedre vægt eller kropsmasseindeks (BMI) grænse. Gennemsnitlig BMI af Kyleena -personer var 25,2 kg/m 2 (område 15.2 - 57,6 kg/m 2 ); 16% havde en BMI ≥ 30 kg/m 2 og 2.0% had a BMI ≥ 40 kg/m 2 . Frekvenserne af rapporterede bivirkninger af narkotika repræsenterer rå forekomster.
De mest almindelige bivirkninger (forekommer hos ≥ 5%brugere) var vulvovaginitis (24%) ovariecysten (22%) abdominal smerte/bækkesmerter (21%) hovedpine/migræne (15%) acne/seborrhea (15%) dysmenorrhea/uterine spasm (10%) brystsmerter/brystets ubehag (10%) og øget blødning (8%).
I de kombinerede undersøgelser ophørte 22% for tidligt på grund af en bivirkning. De mest almindelige bivirkninger (> 1%), der førte til seponering, blev øget blødning (NULL,5%) mavesmerter/bækkensmerter (NULL,2%) enhedsafvisning (NULL,1%) acne/seborrhea (NULL,3%) og dysmenorrhea/uterus spasme (NULL,3%).
Almindelige bivirkninger (forekommer hos ≥1% brugere) er sammenfattet i tabel 4 (præsenteret som rå tilfælde).
Tabel 4: Bivirkninger, der opstod i mindst 1% af Kyleena -brugere i kliniske forsøg af System Organ Class (SOC)
| System Organ Class | Bivirkning | Forekomst (%) (N = 1697) |
| Reproduktionssystem og brystforstyrrelser | Vulvovaginitis | 24.3 |
| Ovariecyste a | 22.2 | |
| Dysmenorrhea/livmoderspasme | 8.0/2.4 | |
| Øget blødning b | 7.9 | |
| Brystsmerter/ubehag | 7.1/3.5 | |
| Kønsudladning | 4.5 | |
| Enhedsudvisning (komplet og delvis) | 3.5 | |
| Øvre kønsorganinfektion | 1.5 | |
| Gastrointestinale lidelser | Abdominal smerte/bækkensmerter | 13.3/8.2 |
| Kvalme | 4.7 | |
| Hud og subkutane vævsforstyrrelser | Acne/seborrhea | 14.1/1.8 |
| Alopecia | 1.0 | |
| Nervesystemforstyrrelser | Hovedpine/migræne | 12.9/3.3 |
| Psykiatriske lidelser | Depression/deprimeret humør | 4.4/0.2 |
| a Ovariecyster blev rapporteret som bivirkninger, hvis de var unormale ikke-funktionelle cyster og/eller havde en diameter> 3 cm ved ultralydundersøgelse b Ikke alle blødningsændringer blev fanget som bivirkninger [se Advarsler og forholdsregler ]. |
I de kliniske forsøg inkluderede alvorlige bivirkninger, der forekommer i mere end et enkelt individ: ektopisk graviditet/brudt ektopisk graviditet (10 individer); Bekkeninflammatorisk sygdom (6 personer); ubesvaret abort/ufuldstændig spontan abort/spontan abort (4 forsøgspersoner); ovariecyst (3 forsøgspersoner); mavesmerter (4 forsøgspersoner); Depression/affektiv lidelse (4 forsøgspersoner); og uterusperforation/indlejret enhed (myometrial perforation) (3 forsøgspersoner).
Postmarketing Experience/
Bivirknings From Postmarketing Spontaneous Reports
Følgende bivirkninger er blevet identificeret under anvendelse af LNG-frigivende IUSS. Fordi disse reaktioner rapporteres frivilligt fra en population af usikker størrelse, er det ikke altid muligt at pålideligt estimere deres frekvens eller etablere et årsagsforhold til eksponering for lægemidler.
- Arteriel trombotisk og venøs tromboemboliske begivenheder inklusive tilfælde af lungeemboli dyb venetrombose og slagtilfælde
- Enhedsbrud
- Overfølsomhed (inklusive udslæt urticaria og angioødem)
- Øget blodtryk
Rapporterede bivirkninger fra postmarketingundersøgelser
Vurdering af perforering og udvisning af intrauterine enheder (APEX IUD) undersøgelse
Apex IUD var en stor amerikansk retrospektiv kohortundersøgelse for at vurdere virkningen af amning og timing af postpartum IUD -indsættelse af livmoderformer og IUD -udvisning. Analyserne omfattede i alt 326658 indsættelser 30% (97824 insertioner), hvoraf blev udført hos kvinder med en levering i de foregående 12 måneder. For indsættelser, der blev udført hos kvinder, der havde leveret ≤ 52 uger før IUD -indsættelse, forekom størstedelen af postpartum -indsættelser 57,3% (56047 insertioner) mellem 6 og 14 uger efter fødslen. Amningsdata var tilgængelige i 94817 insertioner udført i kvinder 52 uger eller mindre efter fødslen.
Undersøgelsesresultaterne indikerede, at risikoen for uterusperforering var højest hos kvinder med IUD -indsættelse ≤ 6 uger efter fødslen. Umiddelbart postpartum -indsættelse (0–3 dage) fund er begrænset på grund af det relativt lille antal indsættelser, der forekommer inden for dette tidsinterval. Kvinder, der ammede på indsættelsestidspunktet, var på 33% højere risiko for perforering (justeret fareforhold [HR] = 1,33 95% konfidensinterval [CI]: 1,07–1,64) sammenlignet med kvinder, der ikke ammede på tidspunktet for indsættelse. Progratvis lavere risiko for livmoderforerie blev observeret i postpartum -tidsvinduer ud over 6 uger i både amning og ikke ammende kvinder. Tabel 5 viser livmoderens perforeringshastigheder for LNG IU'er stratificeret ved amningstatus og postpartuminterval.
Tabel 5: Uterusperforering 1 Priser for LNG IU'er efter amningstatus og postpartuminterval
| Amning på indsættelsestidspunktet | Ikke amning på indsættelsestidspunktet | |||
| Postpartum -interval på indsættelsestidspunktet | Antal begivenheder/ indsættelser | Uterin perforationshastighed pr. 1000 indsættelser | Antal begivenheder/ indsættelser | Uterin perforationshastighed pr. 1000 indsættelser |
| 0 til 3 dage | 8/1896 | 4.22 | 0/277 | 0.00 |
| 4 dage til ≤ 6 uger | 120/10735 | 11.18 | 28/2377 | 11.78 |
| > 6 til ≤ 14 uger | 268/29677 | 9.03 | 30/32011 | 6.66 |
| > 14 til ≤ 52 uger | 43/6139 | 7.00 | 22/9089 | 2.42 |
| > 52 uger eller ingen levering | Ingen tilgængelige data | 243/184733 | 1.32 | |
| 1 Uterin perforation inkluderer både komplet og delvis perforering |
Risikoen for udvisning var variabel over postpartumintervaller gennem 52 uger. Kvinder, der ammede, var på 28% lavere risiko for IUD-udvisning (justeret HR = 0,72 95% CI: 0,64-0,80) sammenlignet med kvinder, der ikke ammede på indsættelsestidspunktet. Tabel 6 viser IUD -udvisningssatserne for LNG IU'er stratificeret ved amningstatus og postpartuminterval.
Tabel 6: Udvisning 1 Priser for LNG IU'er efter amningstatus og postpartuminterval
| Amning på indsættelsestidspunktet | Ikke amning på indsættelsestidspunktet | |||
| Postpartum -interval på indsættelsestidspunktet | Antal begivenheder/ indsættelser | Udvisningsprocent pr. 1000 indsættelser | Antal begivenheder/ indsættelser | Udvisningsprocent pr. 1000 indsættelser |
| 0 til 3 dage | 187/1896 | 98.63 | 12/277 | 43.32 |
| 4 dage til ≤ 6 uger | 185/10735 | 17.23 | 52/2377 | 21.88 |
| > 6 til ≤ 14 uger | 421/29677 | 14.19 | 306/2011 | 25.48 |
| > 14 til ≤ 52 uger | 120/6139 | 19.55 | 273/9089 | 30.04 |
| > 52 uger eller ingen levering | Ingen tilgængelige data | 5481/184733 | 29.67 | |
| 1 Udvisning inkluderer både fuldstændig og delvis udvisning |
Lægemiddelinteraktioner for Kyleena
Der er ikke udført nogen interaktionsundersøgelser med lægemidler med Kyleena.
Lægemidler eller urteprodukter, der inducerer eller hæmmer LNG -metaboliserende enzymer inklusive CYP3A4, kan reducere eller øge henholdsvis serumkoncentrationerne af LNG under brugen af Kyleena. Imidlertid formidles den præventionseffekt af Kyleena via den direkte frigivelse af LNG i livmoderhulen og vil sandsynligvis ikke blive påvirket af lægemiddelinteraktioner via enzyminduktion eller inhibering.
Advarsler for Kyleena
Inkluderet som en del af 'FORHOLDSREGLER' Afsnit
Forholdsregler for Kyleena
Risiko for ektopisk graviditet
Evaluer kvinder for ektopisk graviditet, hvis de bliver gravide med Kyleena på plads, fordi sandsynligheden for, at en graviditet bliver ektopisk, øges med Kyleena. Cirka halvdelen af graviditeter, der forekommer med Kyleena på plads, vil sandsynligvis være ektopiske. Overvej også muligheden for ektopisk graviditet i tilfælde af underlivssmerter, især i forbindelse med ubesvarede menstruation, eller hvis en amenorrheisk kvinde begynder at blø.
Forekomsten af ektopisk graviditet i kliniske forsøg med Kyleena, som udelukkede kvinder med en historie med ektopisk graviditet, var ca. 0,2% om året. Risikoen for ektopisk graviditet hos kvinder, der har en historie med ektopisk graviditet og bruger Kyleena, er ukendt. Kvinder med en tidligere historie med ektopisk graviditet tubalkirurgi eller bækkeninfektion har en højere risiko for ektopisk graviditet. Ektopisk graviditet kan resultere i tab af fertilitet.
Risici med intrauterin graviditet
Hvis graviditet opstår under brug af Kyleena, skal du fjerne Kyleena, fordi det at forlade den på plads kan øge risikoen for spontan abort og for tidligt arbejde. Fjernelse af Kyleena eller sondering af livmoderen kan også resultere i spontan abort. I tilfælde af en intrauterin graviditet med Kyleena overvej følgende:
Septisk abort
Hos patienter, der bliver gravid med en IU'er på plads septisk abort - med septikæmi septisk chok og død - kan det forekomme.
Fortsættelse af graviditet
Hvis en kvinde bliver gravid med Kyleena på plads, og hvis Kyleena ikke kan fjernes, eller kvinden vælger ikke at få den fjernet, advarer hende om, at manglende fjernelse af Kyleena øger risikoen for spontanabort sepsis for tidlig arbejdskraft og for tidlig levering. Rådgive hende om isolerede rapporter om virilisering af det kvindelige foster efter lokal eksponering for LNG under graviditet med en LNG IU'er på plads [se Brug i specifikke populationer ]. Follow her pregnancy closely og advise her to report immediately any symptom that suggests complications of the pregnancy.
Sepsis
Alvorlig infektion eller sepsis inklusive gruppe A-streptokokk-sepsis (GAS) er rapporteret efter indsættelse af en LNG-frigivende IU'er. I nogle tilfælde forekom alvorlig smerte inden for timer efter indsættelse efterfulgt af sepsis inden for få dage. Fordi død fra gas er mere sandsynligt, hvis behandlingen er forsinket, er det vigtigt at være opmærksom på disse sjældne, men alvorlige infektioner. Aseptisk teknik under indsættelse af Kyleena er vigtig for at minimere alvorlige infektioner såsom gas.
Bækkeninfektion
Undersøg straks brugere med klager over lavere abdominal eller bækkenesmerter lugtende udladning uforklarlig blødning feber kønsorganer eller sår. Fjern Kyleena i tilfælde af tilbagevendende endometritis eller bækkeninflammatorisk sygdom, eller hvis en akut bækkeninfektion er alvorlig eller ikke reagerer på behandling.
Bekkeninflammatorisk sygdom (PID)
Kyleena is contraindicated in the presence of known or suspected PID or in women with a history of PID unless there has been a subsequent intrauterine pregnancy [see Kontraindikationer ]. IUDs have been associated with an increased risk of PID most likely due to organisms being introduced into the uterus during insertion. In clinical trials PID was observed in 0.5% of women overall og occurred more frequently within the first year og most often within the first month after insertion of Kyleena.
Kvinder med øget risiko for PID
PID er ofte forbundet med en seksuelt overført infektion (STI), og Kyleena beskytter ikke mod STI. Risikoen for PID er større for kvinder, der har flere seksuelle partnere og også for kvinder, hvis seksuelle partner (er) har flere seksuelle partnere. Kvinder, der har haft PID, har en øget risiko for en tilbagefald eller geninfektion. Undersøg især, om kvinden har en øget risiko for infektion (for eksempel leukæmi erhvervede immunmangelsyndrom [AIDS] intravenøst stofmisbrug).
Subklinisk PID
PID kan være asymptomatisk, men resulterer stadig i tubalskade og dens efterfølger.
Behandling af PID
Efter en diagnose af PID eller mistænkt PID -bakteriologiske prøver skal opnås, og antibiotikabehandling skal initieres hurtigt. Fjernelse af Kyleena efter påbegyndelse af antibiotikabehandling er normalt passende.1
Actinomycosis
Actinomycosis has been associated with IUDs. Remove Kyleena from symptomatic women og treat with antibiotics. The significance of actinomyces-like organisms on Pap smear in an asymptomatic IUD user is unknown og so this finding alone does not always require Kyleena removal og treatment. When possible confirm a Pap smear diagnosis with cultures.
Perforering
Perforering (total or partial including penetration/embedment of Kyleena in the uterine wall or cervix) may occur most often during insertion although the perforation may not be detected until sometime later. The incidence of perforation during clinical trials was <0.1%.
Risikoen for uterusperforering øges hos kvinder, der for nylig har født og hos kvinder, der ammer på indsættelsestidspunktet. I en stor sikkerhedsundersøgelse efter markedsføring i USA var risikoen for uterusperforering højest, når indsættelsen opstod inden for ≤ 6 uger efter fødslen og også højere med amning på indsættelsestidspunktet [se Bivirkninger ].
Risikoen for perforering kan øges, hvis Kyleena indsættes, når livmoderen er fast retrovertet eller ikke fuldstændigt involveret.
Hvis perforering forekommer, skal du finde og fjerne Kyleena. Kirurgi kan være påkrævet. Forsinket detektion eller fjernelse af Kyleena i tilfælde af perforering kan resultere i migration uden for livmoderhulen adhæsioner peritonitis tarmperforerings tarmobstruktionsabscesser og erosion af tilstødende viscera. Derudover kan perforering reducere præventionseffektiviteten og resultere i graviditet.
Udvisning
Delvis eller fuldstændig udvisning af Kyleena kan forekomme, hvilket resulterer i tab af effektivitet. Udvisning kan være forbundet med symptomer på blødning eller smerter, eller det kan være asymptomatisk og gå upåagtet hen. Kyleena reducerer typisk menstruationsblødning over tid; Derfor kan en stigning i menstruationsblødning være tegn på en udvisning. Overvej yderligere diagnostisk billeddannelse, såsom røntgenstråle, hvis der er mistanke om udvisning på baggrund af ultralyd [se Kliniske overvejelser til brug og fjernelse ]. In clinical trials a 5-year expulsion rate of 3.5% (59 out of 1690 subjects) was reported.
Risikoen for udvisning øges med indsættelser umiddelbart efter fødslen og ser ud til at øges med indsættelse efter abort fra anden trimester baseret på begrænsede data. I en stor sikkerhedsundersøgelse efter markedsføring i USA var risikoen for udvisning lavere med ammningsstatus [se Bivirkninger ].
Fjern en delvist udvist Kyleena. Hvis udvisning har fundet sted, kan en ny Kyleena indsættes, hver gang udbyderen kan være med rimelighed sikker på, at kvinden ikke er gravid.
Ovariecyster
Fordi den præventionseffekt af Kyleena hovedsageligt skyldes dens lokale effekter inden for livmoderens ægløsningscyklusser med follikulær brud, forekommer normalt hos kvinder i den frugtbare alder ved hjælp af Kyleena. Ovariecyster (rapporteret som bivirkninger, hvis de var unormale ikke-funktionelle cyster og/eller havde en diameter> 3 cm på ultralydundersøgelse) blev rapporteret mindst en gang i løbet af kliniske forsøg hos 22% af kvinder, der brugte Kyleena og 0,6% af forsøgspersoner, der blev afbrudt på grund af en æggestokkens cyste. De fleste ovariecyster er asymptomatiske, selvom nogle måske ledsages af bækkensmerter eller dyspareunia. I de fleste tilfælde forsvinder æggestokkens cyster spontant i løbet af to til tre måneders observation. Evaluer vedvarende ovariecyster. Kirurgisk intervention er normalt ikke påkrævet.
Blødningsmønsterændringer
Kyleena can alter the bleeding pattern og result in spotting irregular bleeding heavy bleeding oligomenorrhea og amenorrhea. During the first 3–6 months of Kyleena use the number of bleeding og spotting days may be higher og bleeding patterns may be irregular. Thereafter the number of bleeding og spotting days usually decreases but bleeding may remain irregular.
I Kyleena -kliniske forsøg udviklet amenorrhea ved udgangen af det første brugsår i cirka 12% af Kyleena -brugere. I alt 81 forsøgspersoner ud af 1697 (NULL,8%) ophørte på grund af klager over livmoderblødning. Tabel 2 viser blødningsmønstrene som dokumenteret i Kyleena-kliniske forsøg baseret på 90-dages referenceperioder. Tabel 3 viser antallet af blødning og pletdage baseret på 28-dages cyklusækvivalenter.
Tabel 2: Blødningsmønstre rapporteret med Kyleena i præventionsundersøgelser (efter 90-dages referenceperioder)
| Kyleena | Første 90 dage N = 1566 | Anden 90 dage N = 1511 | Slut på år 1 N = 1371 | Slut på år 3 N = 975 | Slut på år 5 N = 530 |
| Amenorrhea 1 | <1% | 5% | 12% | 20% | 23% |
| Sjælden blødning 2 | 10% | 20% | 26% | 26% | 26% |
| Hyppig blødning 3 | 25% | 10% | 4% | 2% | 2% |
| Langvarig blødning 4 | 57% | 14% | 6% | 2% | 1% |
| Uregelmæssig blødning 5 | 43% | 25% | 17% | 10% | 9% |
| 1 Defineret som emner uden blødning/spotting i hele 90-dages referenceperiode 2 Defineret som emner med 1 eller 2 blødnings-/spotting-episoder i 90-dages referenceperiode 3 Defineret som emner med mere end 5 blødnings-/spotting-episoder i 90-dages referenceperiode 4 Defineret som emner med blødning/spotting-episoder, der varer mere end 14 dage i den 90-dages referenceperiode. Personer med langvarig blødning kan også være inkluderet i en af de andre kategorier (ekskl. Amenoré) 5 Defineret som emner med 3 til 5 blødnings-/spotting-episoder og mindre end 3 blødning/pletfri intervaller på 14 eller flere dage |
Tabel 3: Gennemsnitligt antal blødning og pletdage pr. 28-dages cyklusækvivalent
| 28-dages cyklus Tilsvarende | Cyklus 1 N = 1619 | Cyklus 4 N = 1575 | Cyklus 7 N = 1518 | Cyklus 13 N = 1394 | Cyklus 39 N = 913 | Cyklus 65 N = 322 |
| Dage på behandling | 1–28 | 85–112 | 169–196 | 337–364 | 1065-1092 | 1793-1820 |
| Betyde (SD) | Betyde (SD) | Betyde (SD) | Betyde (SD) | Betyde (SD) | Betyde (SD) | |
| Antal blødningsdage | 7.2 (5.9) | 3.2 (3.6) | 2.2 (3.0) | 1.5 (2.4) | 1.0 (2.0) | 0.9 (1.8) |
| Antal pletdage | 8.6 (6.0) | 4.6 (4.4) | 3.5 (3.4) | 2.9 (3.0) | 2.2 (2.6) | 2.1 (2.4) |
Hvis en betydelig ændring i blødning udvikler sig under langvarig anvendelse, skal du tage passende diagnostiske foranstaltninger for at udelukke endometrial patologi. Overvej muligheden for graviditet, hvis menstruation ikke forekommer inden for seks uger efter begyndelsen af en tidligere menstruation. Når graviditeten er udelukket, er gentagne graviditetstest generelt ikke nødvendige hos amenorrheiske kvinder, medmindre de f.eks. Angivet med andre tegn på graviditet eller af bækkensmerter.
Brystkræft
Kvinder, der i øjeblikket har eller har haft brystkræft eller har en mistanke om brystkræft, bør ikke bruge hormonel prævention inklusive Kyleena, fordi nogle brystkræft er hormonfølsomme [se Kontraindikationer ].
Der er modtaget spontane rapporter om brystkræft under erfaring med eftermarkedsføring med en LNG-frigivende IU'er. Observationsundersøgelser af risikoen for brystkræft ved brug af en LNG-frigivende IU'er giver ikke afgørende bevis for øget risiko.
Kliniske overvejelser til brug og fjernelse
Brug Kyleena med forsigtighed efter omhyggelig vurdering, hvis der findes nogen af følgende betingelser, og overvej fjernelse af systemet, hvis nogen af dem opstår under brug:
- Koagulopati eller anvendelse af antikoagulantia
- Migræne fokal migræne med asymmetrisk visuelt tab eller andre symptomer, der indikerer forbigående cerebral iskæmi
- Undtagelsesvis alvorlig hovedpine
- Markant stigning i blodtrykket
- Alvorlig arteriel sygdom såsom slagtilfælde eller myokardieinfarkt
Overvej desuden at fjerne Kyleena, hvis der opstår nogen af følgende betingelser under brug:
- Livmoder eller livmoderhals malignitet
- Gulsot
Hvis trådene ikke er synlige eller forkortes markant, kan de have brudt eller trukket tilbage i cervikale kanalen eller livmoderen. Overvej muligheden for, at systemet kan være blevet fordrevet (for eksempel udvist eller perforeret livmoderen) [se Perforering Udvisning ]. Exclude pregnancy og verify the location of Kyleena for example by sonography X-ray or by gentle exploration of the cervical canal with a suitable instrument. If Kyleena is displaced remove it. A new Kyleena may be inserted at that time or during the next menses if it is certain that conception has not occurred. If Kyleena is in place with no evidence of perforation no intervention is indicated.
Magnetisk resonansafbildning (MRI) sikkerhedsoplysninger
 |
Ikke-klinisk test har vist, at Kyleena er hr. Betinget. En patient med Kyleena kan sikkert scannes i et MR -system, der opfylder følgende betingelser:
- Statisk magnetfelt på 3,0 t eller mindre
- Maksimal rumlig feltgradient på 36000 gauss/cm (360 t/m)
- Maksimalt MR -system rapporterede i gennemsnit i hele kroppen specifik absorptionshastighed (SAR) på 4W/kg (første niveau kontrolleret driftstilstand)
Under de scanningsbetingelser forventes Kyleena IU'er, der er defineret over Kyleena IU'erne, at producere en maksimal temperaturstigning på mindre end 2 ° C efter 15 minutters kontinuerlig scanning.
Ved ikke-klinisk testning forlængede IU'erne op til 5 mm fra IU'erne med en gradient ekkosekvens og et 3,0 T MR-system.
Oplysninger om patientrådgivning
Rådgiv patienten om at læse den FDA-godkendte patientmærkning ( Patientinformation ).
- Seksuelt overførte infektioner: Rådgiv patienten om, at dette produkt ikke beskytter mod HIV -infektion (AIDS) og andre seksuelt overførte infektioner (STI'er).
- Risiko for ektopisk graviditet: Rådgiv patienten om risikoen for ektopisk graviditet inklusive tab af fertilitet. Lær hende at genkende og rapportere til sin sundhedsudbyder omgående eventuelle symptomer på ektopisk graviditet. [Se Advarsler og forholdsregler ]
- Risici ved intrauterin graviditet: Rådgiv patienten om at kontakte sin sundhedsudbyder, hvis hun tror, hun måske er gravid. Informer patienten om risikoen for intrauterin graviditet, mens du bruger Kyleena, herunder risikoen for at forlade Kyleena på plads og risikoen for at fjerne Kyleena eller sondering af livmoderen. Hvis Kyleena ikke kan fjernes i en gravid patient, beder hende om straks at rapportere ethvert symptom, der antyder komplikationer af graviditeten. Rådgiv hende om isolerede rapporter om virilisering af det kvindelige foster efter lokal eksponering for LNG under graviditet med en LNG IU'er på plads. [Se Advarsler og forholdsregler og Brug i specielle befolkninger ]
- Sepsis: Rådgiv patienten om, at alvorlig infektion eller sepsis inklusive gruppe A -streptokokk -sepsis (gas) kan forekomme inden for de første dage efter, at Kyleena er indsat. Instruer hende om at kontakte en sundhedsudbyder med det samme, hvis hun udvikler alvorlig smerte eller feber kort efter, at Kyleena er indsat. [Se Advarsler og forholdsregler ]
- Bækkeninfektion: Rådgiv patienten om muligheden for bækkeninfektioner, herunder PID, og at disse infektioner kan forårsage tubal skade, der fører til ektopisk graviditet eller infertilitet eller sjældent kan kræve hysterektomi eller forårsage død. Lær patienterne at genkende og rapportere til deres sundhedsudbyder straks eventuelle symptomer på bækkeninfektion. Disse symptomer inkluderer udvikling af menstruationsforstyrrelser (langvarig eller kraftig blødning) usædvanlig vaginal udflod abdominal eller bækkenesmerter eller ømhed dyspareunia kulderystelser og feber. [Se Advarsler og forholdsregler .]
- Perforering og Udvisning: Rådgiv patienten om, at IU'erne kan udvises fra eller perforerer livmoderen og instruerer hende om, hvordan hun kan kontrollere, at trådene stadig stikker ud fra livmoderhalsen. Informer hende om, at overdreven smerte eller vaginal blødning under Kyleena -placering forværrer smerter eller blødning efter placering eller manglende evne til at føle, at Kyleena -strenge kan forekomme med Kyleena -perforering og udvisning. Forsvar hende om ikke at trække på trådene og fortrænge Kyleena. Informer hende om, at der ikke er nogen præventionsbeskyttelse, hvis Kyleena er fordrevet eller udvist. Instruer patienten om at kontakte sin sundhedsudbyder, hvis hun ikke kan føle trådene og for at undgå samleje eller bruge en ikke-hormonel back-up-fødselsbekæmpelse (såsom kondomer eller spermicid), indtil placeringen af Kyleena er blevet bekræftet. Rådgive hende om, at hvis perforering finder sted, skal Kyleena være placeret og fjernet; Kirurgi kan være påkrævet. [Se Advarsler og forholdsregler ]
- Ovariecyster: Rådgiv patienten vedrørende risikoen for cyster med æggestokkene, og at cyster kan forårsage kliniske symptomer, herunder bækkesmerter mavesmerter eller dyspareunia. Rådgiv patienten om at kontakte sin sundhedsudbyder, hvis hun oplever disse symptomer. [Se Advarsler og forholdsregler ]
- Blødningsmønsterændringer: Rådgiv patienten, at uregelmæssig eller langvarig blødning og plettering og/eller kramper kan forekomme i løbet af de første uger efter indsættelse. Informer patienten om, at Kyleena i de første 6 måneder af Kyleena bruger antallet af blødning og pletdage kan være højere, og blødningsmønstre kan være uregelmæssige. Hvis hendes symptomer fortsætter eller er alvorlige, skal hun rapportere dem til sin sundhedsudbyder. [Se Advarsler og forholdsregler ]
- Kliniske overvejelser til brug og fjernelse: Rådgiv patienten om at kontakte sin sundhedsudbyder, hvis hun oplever et af følgende:
- Et slagtilfælde eller hjerteanfald
- Meget alvorlig eller migrænehovedpine
- Uforklarlig feber
- Gulning af huden eller hvide i øjnene, da disse kan være tegn på alvorlige leverproblemer
- Graviditet eller mistænkt graviditet
- Bekkenesmerter mavesmerter eller smerter under sex
- HIV -positiv serokonversion i sig selv eller hendes partner
- Mulig eksponering for STI'er
- Usædvanlige vaginale udladning eller kønsår
- Alvorlig vaginal blødning eller blødning, der varer lang tid, eller hvis hun går glip af en menstruationsperiode
- Manglende evne til at føle Kyleenas tråde
- Magnetisk resonansafbildning (MRI) sikkerhedsoplysninger: Informer patienten om, at Kyleena kun kan scannes med MRI kun under specifikke forhold [se Advarsler og forholdsregler ]. Instruct patients who will have an MRI to tell their doctor that they have Kyleena.
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
[Se Advarsler og forholdsregler ]
Brug i specifikke populationer
Graviditet
Risikooversigt
Brugen af Kyleena er kontraindiceret i graviditet eller med en mistænkt graviditet, og Kyleena kan forårsage ugunstige graviditetsresultater [se Kontraindikationer Advarsler og forholdsregler ]. If a woman becomes pregnant with Kyleena in place the likelihood of ectopic pregnancy is increased og there is an increased risk of miscarriage sepsis premature labor og premature delivery. Remove Kyleena if possible if pregnancy occurs in a woman using Kyleena. If Kyleena cannot be removed follow the pregnancy closely [see Advarsler og forholdsregler ].
Der har været isolerede tilfælde af virilisering af de eksterne kønsorganer for det kvindelige foster efter lokal eksponering for LNG under graviditet med en LNG IU'er på plads. Dyreproduktionsundersøgelser er ikke blevet udført med Kyleena.
Amning
Risikooversigt
Publicerede undersøgelser rapporterer tilstedeværelsen af LNG i human mælk. Små mængder progestiner (ca. 0,1% af de samlede moderdoser) blev påvist i modermælken hos sygeplejemødre, der brugte andre LNG-frigivende IUSS, hvilket resulterede i eksponering af LNG for de ammede spædbørn. Der er ingen rapporter om bivirkninger hos ammede spædbørn med moderlig brug af progestin-kun prævention. Isolerede tilfælde af nedsat mælkeproduktion er rapporteret med en LNG-frigivende IU'er. De udviklingsmæssige og sundhedsmæssige fordele ved amning bør overvejes sammen med mors kliniske behov for Kyleena og eventuelle bivirkninger på det ammede barn fra Kyleena eller fra den underliggende moderlige tilstand.
Kvinder og mænd med reproduktivt potentiale
Vend tilbage til fertilitet efter at have ophørt Kyleena
Cirka 71% af 163 kvinder, der ønskede graviditet efter ophør af undersøgelsen og gav opfølgningsinformation, der blev udtænkt inden for 12 måneder efter fjernelse af Kyleena.
Pædiatrisk brug
Kyleenas sikkerhed og effektivitet er etableret hos kvinder i reproduktiv alder. Effektivitet forventes at være den samme for udsatte hunner under 18 år som for brugere 18 år og ældre. Brug af dette produkt før menarche er ikke indikeret.
Geriatrisk brug
Kyleena has not been studied in women over age 65 og is not approved for use in this population.
Overdoseringsoplysninger til Kyleena
Ingen oplysninger leveret
Kontraindikationer for Kyleena
Brugen af Kyleena er kontraindiceret, når der findes en eller flere af følgende betingelser:
- Graviditet or suspicion of pregnancy [see Advarsler og forholdsregler Brug i specifikke populationer ]
- Til brug som post-coital prævention (nødforebyggelse)
- Medfødt eller erhvervet livmoderanomali inklusive fibroider, der forvrænger livmoderhulen
- Akut bækkeninflammatorisk sygdom (PID) eller en historie med PID, medmindre der har været en efterfølgende intrauterin graviditet [se Advarsler og forholdsregler ]
- Postpartum endometritis eller inficeret abort i de sidste 3 måneder
- Kendt eller mistænkt livmoder eller livmoderhals malignitet
- Kendt eller mistænkt brystkræft eller anden progestin-følsom kræft nu eller tidligere
- Uterinblødning af ukendt etiologi
- Ubehandlet akut cervicitis eller vaginitis inklusive bakteriel vaginose eller andre infektioner i lavere kønsorganer, indtil infektion er kontrolleret
- Akut leversygdom eller levertumor (godartet eller ondartet)
- Betingelser forbundet med øget følsomhed for bækkeninfektioner [se Advarsler og forholdsregler ]
- En tidligere indsat intrauterin enhed (IUD), der ikke er fjernet
- Overfølsomhed over for enhver komponent i dette produkt [se Bivirkninger og BESKRIVELSE ]
Klinisk farmakologi for Kyleena
Handlingsmekanisme
Den lokale mekanisme, hvormed kontinuerligt frigivet LNG bidrager til den præventionseffektivitet af Kyleena, er ikke endeligt demonstreret. Undersøgelser af Kyleena og lignende LNG IUS -prototyper har antydet adskillige mekanismer, der forhindrer graviditet: fortykning af livmoderhalsslim, der forhindrer passage af sædceller i livmoderinhiberingen af sædkapacitet eller overlevelse og ændring af endometrium.
Farmakodynamik
Kyleena has mainly local progestogenic effects in the uterine cavity. The local concentrations of LNG lead to morphological changes including stromal pseudodecidualization glogular atrophy a leukocytic infiltration og a decrease in glogular og stromal mitoses.
I kliniske forsøg med Kyleena blev ægløsning vurderet baseret på serumprogesteronværdier> 2,5 ng/ml i en undersøgelse og serumprogesteronværdier> 2,5 ng/ml sammen med serumøstradiolniveauer <27.24 pg/mL in another study. Evidence of ovulation by these criteria was seen in 23 out of 26 women in the first year in 19 out of 20 women in the second year og in all 16 women in the third year. In the fourth year evidence of ovulation was observed in the one woman remaining in the subset og in the fifth year no women remained in this subset.
Farmakokinetik
Absorption
Lave doser af LNG administreres i livmoderhulen med Kyleena intrauterin leveringssystem. De forgæves Udgivelseshastigheden er ca. 17,5 mcg/dag efter 24 dage og reduceres til ca. 15,3 mcg/dag efter 60 dage og til 9,8 mcg/dag efter 1 år. Det falder derefter gradvist til ca. 7,9 mcg/dag efter 3 år og 7,4 mcg/dag efter 5 år. Den gennemsnitlige LNG forgæves Udgivelseshastigheden er cirka 12,6 mcg/dag i det første år og 9,0 mcg/dag i perioden 5 år.
I en undergruppe af 6 forsøgspersoner var den maksimale observerede serum LNG -koncentration (gennemsnit ± SD) 302 ± 170 pg/ml nået efter 7,5 dage (median) af Kyleena -indsættelse. Derefter var LNG -serumkoncentrationerne (gennemsnit ± SD) ved år 1 2 3 4 og 5 199 ± 171 pg/ml (n = 6) 120 ± 57 pg/ml (n = 6) 122 ± 65 pg/ml (n = 6) henholdsvis 79 ± 12 pg/ml (n = 3) og 65 ± 15 pg/ml (n = 3). En farmakokinetisk evaluering af population baseret på en bredere database (> 1000 patienter) viste en lignende faldende koncentrationsprofil med 175 ± 74 pg/ml ved 7 dage efter placering 125 ± 50 pg/ml ved 1 år 99 ± 41 pg/ml efter 3 år og 90 ± 35 pg/ml efter 5 år.
Hvad er gurkemeje curcumin godt til
Fordeling
Det er rapporteret, at den tilsyneladende mængde af Distribution af LNG er ca. 1,8 L/kg. LNG er bundet ikke-specifikt til serumalbumin og specifikt til kønshormonbindende globulin (SHBG). I overensstemmelse hermed resulterer ændringer i koncentrationen af SHBG i serum i en stigning (ved højere SHBG -koncentration) eller et fald (ved lavere SHBG -koncentration) af den samlede LNG -koncentration i serum. I en undergruppe af 6 forsøgspersoner faldt koncentrationen af SHBG i gennemsnit med ca. 30% i løbet af de første 3 måneder efter indsættelse af Kyleena og forblev relativt stabil i den 5 -årige brugsperiode. Mindre end 2% af den cirkulerende LNG er til stede som fri steroid.
Eliminering
Efter intravenøs administration af 0,09 mg lng til raske frivillige er den samlede clearance af LNG ca. 1 ml/min/kg, og elimineringshalveringstiden er cirka 20 timer. Metabolisk clearance-hastighed kan variere mellem individer med flere gange, og dette kan delvis udgøre, at brede individuelle variationer i LNG-koncentrationer set hos personer, der bruger LNG-indeholdende præventionsprodukter.
Metabolisme
Efter absorption er LNG i vid udstrækning metaboliseret. De vigtigste metaboliske veje er reduktionen af Δ4-3-oxo-gruppen og hydroxyleringer ved position 2a 1β og 16β efterfulgt af konjugering. Betydelige mængder konjugeret og ukonjugeret 3a 5p- er også til stede i serum sammen med meget mindre mængder 3a 5a-tetrahydrolevonorgestrel og 16β-hydroxylevonorgestrel. CYP3A4 er det vigtigste enzym, der er involveret i den oxidative metabolisme af LNG.
Udskillelse
LNG og dens fase I -metabolitter udskilles primært som glucuronidkonjugater. Cirka 45% af LNG og dens metabolitter udskilles i urinen, og ca. 32% udskilles i fæces for det meste som glucuronidkonjugater.
Specifikke populationer
Pædiatrisk
Kyleenas sikkerhed og effektivitet er etableret hos kvinder i reproduktiv alder. Brug af dette produkt før menarche er ikke indikeret.
Geriatrisk
Kyleena has not been studied in women over age 65 og is not approved for use in this population.
Race
Ingen undersøgelser har evalueret virkningen af race på farmakokinetikken i Kyleena.
Leverskrivning i leveren
Der blev ikke foretaget undersøgelser for at evaluere virkningen af leversygdom på dispositionen af Kyleena.
Nedskærmning af nyren
Der blev ikke udført nogen formelle undersøgelser for at evaluere virkningen af nyresygdom på dispositionen af Kyleena.
Interaktioner med lægemiddel-lægemidler
Der blev ikke udført nogen interaktionsundersøgelser med lægemidler med Kyleena [se Lægemiddelinteraktioner ].
Kliniske studier
Kyleena -præventionen af Kyleena blev evalueret i et klinisk forsøg, der tilmeldte generelt sunde kvinder i alderen 18-35 år, hvoraf 1452 modtog Kyleena. Af disse 40%(574) blev nulliparøse kvinder 870 (60%) kvinder afsluttet 3 år af undersøgelsen 707 (49%) valgt til at tilmelde sig en forlængelsesfasning til i alt 5 år og 550 (38%) afsluttede 5 års brug. Retssagen var en multicenter-multinationel randomiseret open-label-undersøgelse udført i 11 lande i Europa Latinamerika USA og Canada. Kvinder mindre end seks uger efter fødslen med en historie med ektopisk graviditet med klinisk signifikante ovariecyster eller med HIV eller på anden måde i høj risiko for seksuelt overførte infektioner blev udelukket. I alt 563 (39%) blev behandlet på amerikanske steder, og 889 (61%) var på ikke-amerikanske steder. Den racemæssige demografi af tilmeldte kvinder, der modtog Kyleena, var: kaukasisk (80%) sort/afroamerikansk (NULL,1%) andre (NULL,6%) og asiatiske (NULL,2%); 11% angav latinamerikansk etnicitet. Det kliniske forsøg havde ingen øvre eller nedre vægt eller BMI -grænse. Vægtområdet var 38 til 173 kg (gennemsnitsvægt: 68,7 kg) og gennemsnitlig BMI var 25,3 kg/m 2 (Område 15,2–57,6 kg/m 2 ). Of Kyleena-treated women 22% discontinued the study treatment due to an adverse reaction 5.0% were lost to follow-up 2.3% withdrew for unspecified reasons 1.2% discontinued due to a protocol deviation 0.9% discontinued due to pregnancy og 20% discontinued due to other reasons.
Graviditetshastigheden beregnet som Pearl Index (PI) hos kvinder i alderen 18-35 år var det primære effektivitetsdepunkt, der blev brugt til at vurdere prævention pålidelighed. PI blev beregnet baseret på 28-dages ækvivalente eksponeringscyklusser; Evaluerbare cyklusser udelukkede dem, hvor back-up prævention blev anvendt, medmindre der opstod en graviditet i denne cyklus. Året 1 PI var baseret på 2 graviditeter, og den kumulative 5-årige graviditetsgrad var baseret på 13 graviditeter, der opstod efter begyndelsen af behandlingen og inden for 7 dage efter Kyleena-fjernelse eller udvisning. Tabel 5 viser de beregnede årlige og kumulative graviditetshastigheder.
Tabel 7: Pearindekser efter år og 5-årig kumulativ graviditetshastighed
| Kyleena Clinical Trial | Pearl Index | Kumulativ 5-årig Kaplan Meier-sats | ||||
| År 1 | År 2 | År 3 | År 4 | År 5 | ||
| Antal evaluable 28-dages eksponeringscyklusser16207 | 16207 | 13853 | 11610 | 8556 | 7087 | 57313 |
| Graviditet Rate (95% Confidence Interval) | 0.16 (NULL,02 0,58) | 0.38 (NULL,10 0,96) | 0.45 (NULL,12 1.15) | 0.15 (NULL,00 0,85) | 0.37 (NULL,04 1,33) | 1.45 (NULL,82 2,53) |
Patientinformation til Kyleena
Kyleena
(Ki-lee-nah)
(Levonorgestrel-frigivende intrauterine system)
Læs denne patientoplysninger omhyggeligt, før du beslutter, om Kyleena er det rigtige for dig. Disse oplysninger indtager ikke stedet for at tale med din gynækolog eller anden sundhedsudbyder, der er specialiseret i kvinders sundhed. Hvis du har spørgsmål om Kyleena, skal du spørge din sundhedsudbyder. Du skal også lære om andre præventionsmetoder for at vælge den, der er bedst for dig.
Kyleena does not protect against HIV infection (AIDS) og other sexually transmitted infections (STIs).
Hvad er Kyleena?
- Kyleena is a hormone-releasing system placed in your uterus by your healthcare provider to prevent pregnancy for up to 5 years.
- Kyleena can be removed by your healthcare provider at any time.
- Kyleena can be used whether or not you have given birth to a child.
Kyleena is a small flexible plastic T-shaped system that slowly releases a progestin hormone called Levonorgestrel (LNG) that is often used in birth control pills . Because Kyleena releases LNG into your uterus only small amounts of the hormone enter your blood. Kyleena does not contain estrogen .
To tynde tråde er fastgjort til stammen (nedre ende) af Kyleena. Trådene er den eneste del af Kyleena, du kan føle, når Kyleena er i din livmoder; I modsætning til en tamponstreng strækker trådene sig imidlertid ikke uden for din krop.
 |
Kyleena is small
 |
og Flexible
Kyleena is small og Flexible
Hvad hvis jeg har brug for prævention i mere end 5 år?
Kyleena must be removed after 5 years. Your healthcare provider can place a new Kyleena during the same office visit if you choose to continue using Kyleena.
Hvad hvis jeg vil stoppe med at bruge Kyleena?
Kyleena is intended for use up to 5 years but you can stop using Kyleena at any time by asking your healthcare provider to remove it. You could become pregnant as soon as Kyleena is removed so you should use another method of birth control if you do not want to become pregnant. Talk to your healthcare provider about the best birth control methods for you because your new method may need to be started 7 days before Kyleena is removed to prevent pregnancy.
Hvad hvis jeg ændrer mening om prævention og ønsker at blive gravid på mindre end 5 år?
Din sundhedsudbyder kan når som helst fjerne Kyleena. Du kan blive gravid, så snart Kyleena fjernes. Cirka 7 ud af 10 kvinder, der ønsker at blive gravide, bliver gravid engang i det første år efter, at Kyleena er fjernet.
Hvordan fungerer Kyleena?
Kyleena may work in several ways including thickening cervical mucus inhibiting sperm movement reducing sperm survival og thinning the lining of your uterus. It is not known exactly how these actions work together to prevent pregnancy.
 |
Hvor godt fungerer Kyleena til prævention?
Følgende diagram viser chancen for at blive gravid for kvinder, der bruger forskellige metoder til prævention. Hver boks på diagrammet indeholder en liste over fødselsbekæmpelsesmetoder, der ligner effektivitet. De mest effektive metoder er øverst på diagrammet. Kassen i bunden af diagrammet viser chancen for at blive gravid for kvinder, der ikke bruger prævention og prøver at blive gravid.
Kyleena an intrauterine device (IUD) also known as an intrauterine system (IUS) is in the box at the top of the chart.
Hvem bruger måske Kyleena?
Du kan vælge Kyleena, hvis du:
- Ønsker langvarig fødselsbekæmpelse, der giver en lav chance for at blive gravid (mindre end 1 ud af 100)
- ønsker prævention, der fungerer kontinuerligt i op til 5 år
- ønsker prævention, der er reversibel
- ønsker en præventionsmetode, som du ikke behøver at tage dagligt
- er villige til at bruge en fødselsbekæmpelsesmetode, der er placeret i livmoderen
- ønsker prævention, der ikke indeholder østrogen
Brug ikke Kyleena, hvis du:
- er eller kan være gravide; Kyleena kan ikke bruges som et nødsituationer
- Har en alvorlig bækkeninfektion kaldet bækkeninflammatorisk sygdom (PID) eller har haft PID i fortiden, medmindre du har haft en normal graviditet, efter at infektionen gik væk
- har en ubehandlet kønsinfektion nu
- har haft en alvorlig bækkeninfektion i de sidste 3 måneder efter en graviditet
- Kan let få infektioner. For eksempel hvis du:
- Har flere seksuelle partnere, eller din partner har flere seksuelle partnere
- har problemer med dit immunsystem
- Brug eller misbrug intravenøse stoffer
- har eller mistænker, at du måske har kræft i livmoderen eller livmoderhalsen
- har blødning fra vagina, der ikke er blevet forklaret
- har leversygdom eller en levertumor
- har brystkræft eller anden kræft, der er følsom over for progestin (et kvindeligt hormon) nu eller tidligere
- Har allerede en intrauterin enhed i din livmoder
- Har en tilstand af livmoderen, der ændrer formen på livmoderhulen, såsom store fibroid -tumorer
- er allergisk over for levonorgestrel silikone polyethylen sølv silica barium sulfat polypropylen eller kobber phthalocyanin
Før du har placeret Kyleena, fortæl din sundhedsudbyder om alle dine medicinske tilstande, herunder hvis du:
- har nogen af de ovennævnte betingelser
- har haft et hjerteanfald
- har haft et slagtilfælde
- blev født med hjertesygdomme eller har problemer med dine hjerteklapper
- Har problemer med blodkoagulation eller tag medicin for at reducere koagulation
- har højt blodtryk
- for nylig fået en baby eller ammer
- har svær hovedpine eller migræne hovedpine
- har aids hiv eller enhver anden seksuelt overført infektion
Fortæl din sundhedsudbyder om alle de medicin, du tager, herunder receptpligtig medicin og urtemedip for ikke-køb af urter.
Hvordan placeres Kyleena?
Kyleena is placed by your healthcare provider during an in-office visit or immediately after giving birth.
Først vil din sundhedsudbyder undersøge dit bækken for at finde den nøjagtige placering af din livmoder. Din sundhedsudbyder renser derefter din vagina og livmoderhalsen med en antiseptisk opløsning og glider et slank plastrør, der indeholder Kyleena gennem livmoderhalsen i din livmoder.
Din sundhedsudbyder fjerner derefter plastrøret og forlader Kyleena i din livmoder.
Din sundhedsudbyder skærer trådene til den rigtige længde.
Du kan opleve smerter af smerter eller svimmelhed under og efter placering. Hvis dine symptomer ikke går inden for 30 minutter efter placering, er Kyleena muligvis ikke blevet placeret korrekt.
Din sundhedsudbyder vil undersøge dig for at se, om Kyleena skal fjernes eller udskiftes.
Skal jeg kontrollere, at Kyleena er på plads?
Ja, du skal kontrollere, at Kyleena er i korrekt position ved at føle fjernelsestrådene. Det er en god vane at gøre dette 1 gang om måneden. Din sundhedsudbyder skal lære dig, hvordan du kontrollerer, at Kyleena er på plads. Vask først dine hænder med sæbe og vand. Du kan tjekke ved at nå op til toppen af din vagina med rene fingre for at føle fjernelsestrådene. Træk ikke på trådene. Hvis du føler dig mere end bare trådene, eller hvis du ikke kan føle trådene Kyleena muligvis ikke er i den rigtige position og muligvis ikke forhindrer graviditet. Undgå samleje eller brug ikke-hormonel back-up prævention (såsom kondomer eller spermicid) og bede din sundhedsudbyder om at kontrollere, at Kyleena stadig er på det rigtige sted.
Hvor hurtigt efter placering af Kyleena skal jeg vende tilbage til min sundhedsudbyder?
Ring til din sundhedsudbyder, hvis du har spørgsmål eller bekymringer (se hvornår skal jeg ringe til min sundhedsudbyder?). Ellers skal du vende tilbage til din sundhedsudbyder for at få et opfølgende besøg 4 til 6 uger efter, at Kyleena er placeret for at sikre, at Kyleena er i den rigtige position.
Kan jeg bruge tamponer eller menstruationskopper med Kyleena?
Ja tamponer eller menstruationskopper kan bruges sammen med Kyleena. Skift tamponer eller menstruationskopper med omhu for at undgå at trække trådene i Kyleena. Hvis du tror, at du måske har trukket Kyleena ud af sted, skal du undgå samleje eller bruge en ikke-hormonel back-up-fødselsbekæmpelse (såsom kondomer eller spermicid) og kontakte din sundhedsudbyder.
Hvad hvis jeg bliver gravid, mens jeg bruger Kyleena?
Ring til din sundhedsudbyder med det samme, hvis du tror, du kan være gravid. Hvis det er muligt, skal du også lave en urin graviditetstest. Hvis du bliver gravid, mens du bruger Kyleena, kan du have en ektopisk graviditet. Dette betyder, at graviditeten ikke er i livmoderen. Usædvanlig vaginal blødning eller mavesmerter kan være et tegn på ektopisk graviditet.
Ektopisk graviditet er en medicinsk nødsituation, der ofte kræver operation. Ektopisk graviditet kan forårsage intern blødning infertilitet og endda død.
Der er også risici, hvis du bliver gravid, mens du bruger Kyleena, og graviditeten er i livmoderen. Alvorlig infektionsspilgabort for tidlig fødsel og endda død kan forekomme med graviditeter, der fortsætter med en intrauterin enhed (IUD). På grund af dette kan din sundhedsudbyder muligvis forsøge at fjerne Kyleena, selvom det kan forårsage en spontanabort. Hvis Kyleena ikke kan fjernes, skal du tale med din sundhedsudbyder om fordelene og risiciene ved at fortsætte graviditeten og mulige effekter af hormonet på din ufødte baby.
Hvis du fortsætter din graviditet, kan du se din sundhedsudbyder regelmæssigt. Ring til din sundhedsudbyder med det samme, hvis du får influenzalignende symptomer feber kulderystelser kramper smerter blødende vaginal udflod eller væske, der lækker fra din vagina. Disse kan være tegn på infektion.
Hvordan vil Kyleena ændre mine perioder?
I de første 3 til 6 måneder kan din periode blive uregelmæssig, og antallet af blødningsdage kan stige. Du kan også have hyppig plet eller let blødning. Nogle kvinder har kraftig blødning i løbet af denne tid. Du har måske også kramper i løbet af de første par uger. Når du har brugt Kyleena i et stykke tid, vil antallet af blødning og pletdage sandsynligvis mindske. I nogle kvindelige perioder stopper helt. Når Kyleena fjernes, skal dine menstruationsperioder vende tilbage.
Er det sikkert at amme, mens du bruger Kyleena?
Du kan bruge Kyleena, når du ammer .. Kyleena vil sandsynligvis ikke påvirke kvaliteten eller mængden af din modermælk eller din sygeplejes baby. Imidlertid er der rapporteret om isolerede tilfælde af nedsat mælkeproduktion. Risikoen for, at Kyleena går ind i væggen i livmoderen (bliver indlejret) eller går gennem livmoderens væg øges, hvis Kyleena indsættes, mens du ammer.
Vil Kyleena forstyrre samleje?
Du og din partner skal ikke føle Kyleena under samleje. Kyleena er placeret i livmoderen ikke i vagina. Nogle gange kan din partner føle trådene. Hvis dette sker, eller hvis du eller din partner oplever smerter under sex, taler med din sundhedsudbyder.
Kan jeg få en MR med Kyleena på plads?
Kyleena can be safely scanned with MRI only under specific conditions. Before you have an MRI tell your healthcare provider that you have Kyleena an intrauterine device (IUD) in place.
Hvad er de mulige bivirkninger af Kyleena?
Kyleena can cause serious side effects including:
Fortæl din sundhedsudbyder med det samme, hvis du har nogen af disse tegn på PID: langlastning eller kraftig blødning usædvanlig vaginal udladning Lav abdominal (maveområde) smerte smertefulde sex kulderystelser feber kønsorganer eller sår.
- Ektopisk graviditet og intrauterin graviditetsrisici. Der er risici, hvis du bliver gravid, mens du bruger Kyleena (se hvad hvis jeg bliver gravid, mens jeg bruger Kyleena?).
- Livstruende infektion. Livstruende infektion kan forekomme inden for de første dage efter, at Kyleena er placeret. Ring straks til din sundhedsudbyder, hvis du udvikler alvorlig smerte eller feber kort efter, at Kyleena er placeret.
- Bekkeninflammatorisk sygdom (PID). Nogle IUD -brugere får en alvorlig bækkeninfektion kaldet bækkeninflammatorisk sygdom. PID overføres normalt seksuelt. Du har en større chance for at få PID, hvis du eller din partner har sex med andre partnere. PID kan forårsage alvorlige problemer såsom infertilitet ektopisk graviditet eller bækkensmerter, der ikke forsvinder. PID behandles normalt med antibiotika. Mere alvorlige tilfælde af PID kan kræve operation, herunder fjernelse af livmoderen (hysterektomi). I sjældne tilfælde kan infektioner, der starter som PID, endda forårsage død.
- Perforering. Kyleena may go into the wall of the uterus (become embedded) or go through the wall of the uterus. This is called perforation. If this occurs Kyleena may no longer prevent pregnancy. If perforation occurs Kyleena may move outside the uterus og can cause internal scarring infection or damage to other organs og you may need surgery to have Kyleena removed. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with perforation. The risk of perforation is increased if Kyleena is inserted while you are breastfeeding or if you have recently given birth.
- Udvisning. Kyleena may come out by itself. This is called expulsion. Udvisning occurs in about 4 out of 100 women. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with expulsion. You may become pregnant if Kyleena comes out. If you think that Kyleena has come out avoid intercourse or use a non-hormonal back-up birth control (such as condoms or spermicide) og call your healthcare provider. The risk of expulsion is increased with insertion right after delivery or second-trimester abortion.
Almindelige bivirkninger af Kyleena inkluderer:
- Smerter blødning eller svimmelhed under og efter placering. Hvis disse symptomer ikke stopper 30 minutter efter placering, er Kyleena muligvis ikke blevet placeret korrekt. Din sundhedsudbyder vil undersøge dig for at se, om Kyleena skal fjernes eller udskiftes.
- Ændringer i blødning. Du har muligvis blødning og plet mellem menstruationsperioder, især i løbet af de første 3-6 måneder. Nogle gange er blødningen tungere end normalt i starten. Imidlertid bliver blødningen normalt lettere end normalt og kan være uregelmæssig. Ring til din sundhedsudbyder, hvis blødningen forbliver tungere end normalt eller stiger, efter at den har været lys i et stykke tid.
- Ubesvarede menstruationsperioder. Cirka 12 ud af 100 kvinder holder op med at have perioder efter 1 års brug af Kyleena. Hvis du er bekymret for, at du muligvis er gravid, mens du bruger Kyleena, skal du lave en urin graviditetstest og ringe til din sundhedsudbyder. Hvis du ikke har en periode i 6 uger i løbet af Kyleena, skal du bruge din sundhedsudbyder. Når Kyleena fjernes, skal dine menstruationsperioder vende tilbage.
- Cyster på æggestokken. Cirka 22 ud af 100 kvinder, der bruger Kyleena, udvikler en cyste på æggestokken. Disse cyster forsvinder normalt på egen hånd om 2 til 3 måneder. Imidlertid kan cyster forårsage smerter, og nogle gange har cyster brug for operation.
Andre almindelige bivirkninger inkluderer:
- Betændelse eller infektion i den ydre del af din vagina (vulvovaginitis)
- abdominal eller bækkensmerter
- hovedpine eller migræne
- Acne or greasy skin
- smertefulde perioder
- ømme eller smertefulde bryster
Dette er ikke alle de mulige bivirkninger med Kyleena. For mere information, spørg din sundhedsudbyder.
Ring til din læge for medicinsk rådgivning om bivirkninger. Du kan rapportere bivirkninger til FDA på 1-800-FDA-1088. Du kan også rapportere bivirkninger til Bayer Healthcare Pharmaceuticals på 1-888-842-2937.
Efter at Kyleena er blevet placeret, hvornår skal jeg ringe til min sundhedsudbyder?
Hvis Kyleena ved et uheld fjernes, og du havde vaginal samleje inden for den foregående uge, kan du være i fare for graviditet, og du skal tale med en sundhedsudbyder.
Ring til din sundhedsudbyder, hvis du er bekymret for Kyleena. Sørg for at ringe, hvis du:
- Tror du er gravid
- har bækken smerter mavesmerter eller smerter under sex
- har usædvanlige vaginale udladning eller kønssår
- har uforklarlig feberinfluenzalignende symptomer eller kulderystelser
- kan udsættes for seksuelt overførte infektioner (STI'er)
- er bekymrede for, at Kyleena måske er blevet udvist (kom ud)
- kan ikke føle Kyleenas tråde
- Udvikle meget alvorlige eller migrænehovedpine
- har gulning af huden eller hvide i øjnene. Disse kan være tegn på leverproblemer.
- har haft et slagtilfælde or hjerteanfald
- Bliv HIV -positiv, eller din partner bliver HIV -positiv
- har svær vaginal blødning eller blødning, der varer lang tid eller bekymrer dig
Generel rådgivning om sikker og effektiv brug af Kyleena.
Medicin er undertiden ordineret til andre tilstande end dem, der er anført i patientinformationsoplysninger. Hvis du gerne vil have flere oplysninger, skal du tale med din sundhedsudbyder. Du kan bede din sundhedsudbyder om information om Kyleena, der er skrevet til sundhedsfagfolk.
Hvad er ingredienserne i Kyleena?
Aktiv ingrediens: Levonorgestrel
Inaktive ingredienser: silikone polyethylen sølv silica barium sulfat polypropylen kobber phthalocyanin
Denne patientinformation er godkendt af U.S. Food and Drug Administration.

