Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
DecarboxylaseinhibitorerStalevo
Resume af lægemiddeloversigt
Hvad er Stalevo?
Stalevo (Carbidopa Levodopa og Entacapone) er en kombination af flere medicin, der bruges til behandling af Parkinson -symptomer, såsom muskelstivhedsrum spasmer og dårlig muskelkontrol. Levodopa konverteres til et kemikalie kaldet dopamin i hjernen. Symptomer på Parkinsons sygdom Kan være forårsaget af lave niveauer dopamin i hjernen. Carbidopa hjælper med at forhindre nedbrydning af levodopa, før den kan nå hjernen og træde i kraft. Når det bruges sammen med carbidopa og levodopa, øger entacapone niveauer af levodopa i kroppen.
Hvad er bivirkninger af Stalevo?
Stalevo
- elveblest
- Besvær
- Hævelse af dine ansigtslæber tunge eller hals
- Ny eller forværring af muskelspasme
- øget øget øje blinkende eller rykker
- besvimende
- diarre
- Vision ændres
- sløret vision
- Øjesmerter
- Alvorlig mavesmerter
- sort eller tarry afføring
- opkast, der ligner kaffegrunde
- muskelsmerter ømhed eller svaghed
- Ændring i mængden af urin
- humør ændres
- forvirring
- Hallucinationer
- Tanker om selvmord
- vedvarende ondt i halsen
- let blødning eller blå mærker
- usædvanlig træthed
- prikken af hænder eller fødder
- Usædvanlige stærke trang (øget spil for seksuelle trang)
- brystsmerter
- feber
- Usædvanlig muskelstivhed
- Alvorlig forvirring
- sved
- Hurtig eller uregelmæssig hjerteslag
- hurtig vejrtrækning og
- Alvorlig svimmelhed
Få medicinsk hjælp med det samme, hvis du har nogen af de symptomer, der er anført ovenfor.
Almindelige bivirkninger af Stalevo inkluderer:
- diarre
- kvalme
- opkast
- hovedpine
- svimmelhed
- døsighed
- sløret vision
- mavesmerter eller ked af det
- Tab af appetit
- forstoppelse
- tør mund
- Ændringer i din smagsfølelse
- hududslæt eller kløe
- Usædvanlige hudændringer
- Muskelkramper
- Rygsmerter
- Agitation
- angst
- vanskeligheder med at sove (søvnløshed) eller
- mærkelig drømme .
Fortæl din læge, hvis du har alvorlige bivirkninger af Stalevo inklusive:
- ufrivillig Bevægelser (især rykning af øjenlåget)
- besvimende or falling
- Sværheds vanskeligheder
- mave/mavesmerter
- vedvarende diarre
- Vision ændres (including sløret vision)
- Sort/tarry afføring
- Muskelsmerter
- Ændringer i mængden af urin
- Mental/humørændringer (såsom forvirring Hallucinationer Tanker om selvmord)
- tegn på infektion (f.eks. Vedvarende ondt i halsen) eller
- Usædvanlige stærke trang (såsom øget spil øgede seksuelle trang).
Søg medicinsk behandling eller ring 911 på én gang, hvis du har følgende alvorlige bivirkninger:
- Alvorlige øjensymptomer såsom pludseligt synstab sløret synet tunnel vision øje smerter eller hævelse eller at se haloer omkring lys;
- Alvorlige hjertesymptomer såsom hurtig uregelmæssige eller bankende hjerteslag; flagrende i brystet; åndenød; Og pludselig svimmelhed Lightheadedness eller gå ud;
- Alvorlig hovedpine forvirring sløret talearm eller ben svaghed problemer med at gå tab af koordination føles ustabil meget stive muskler høj feber voldsom sved eller rysten.
Dette dokument indeholder ikke alle mulige bivirkninger, og andre kan forekomme. Kontakt din læge for yderligere oplysninger om bivirkninger.
Dosering til Stalevo
Den optimale daglige dosering af Stalevo skal bestemmes for hver patient. Terapi skal individualiseres og justeres i henhold til den ønskede terapeutiske respons.
Hvilke stoffer stoffer eller kosttilskud interagerer med Stalevo?
Stalevo kan interagere med apomorphin -kolestyramin dobutamin Epinephrin Isoniazid isoproterenol Methyldopa Metoclopramid papaverin phenytoin probenecid antibiotika blodtryk medicin antidepressiva medicin til behandling af psykiatriske lidelser koldt eller allergi Medicin narkotika sovepiller muskelafslappende medicin til anfald eller anti-angst medicin. Fortæl din læge alle medicin, du tager.
Stalevo under graviditet og amning
Stalevo skal kun bruges, når det er ordineret under graviditet. Levodopa passerer ind i modermælk. Det er ukendt, om Carbidopa eller Entacapone passerer til modermælk. Kontakt din læge inden amning.
Yderligere oplysninger
Vores Stalevo (Carbidopa Levodopa og Entacapone) bivirkninger Drug Center giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Lægemiddelinteraktioner
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
Beskrivelse for Stalevo
Stalevo er en kombination af carbidopa levodopa og entacapone til behandling af Parkinsons sygdom.
Carbidopa En hæmmer af aromatisk aminosyre -dekarboxylering er en hvid krystallinsk forbindelse, der er lidt opløselig i vand med en molekylvægt på 244,3. Det betegnes kemisk som (-)-l- (a- hydrazino- (α-methyl-ß- (34-dihydroxybenzen) propansyre monohydrat. Dens empiriske formel er c 10 H 14 N 2 O 4 · H. 2 O og dens strukturelle formel er:
 |
Tabletindhold udtrykkes i form af vandfri carbidopa, der har en molekylvægt på 226,3.
Levodopa En aromatisk aminosyre er en hvid krystallinsk forbindelse, der er lidt opløselig i vand med en molekylvægt på 197,2. Det betegnes kemisk som (-)-L-a-amino-ß- (34-dihydroxybenzen) propansyre. Dens empiriske formel er C 9 H 11 INGEN 4 Og dens strukturelle formel er:
 |
Entacapone En COMT-hæmmer er en nitro-catechol-struktureret forbindelse med en molekylvægt på 305,3. Det kemiske navn på Entacapone er (E) -2-cyano-3- (34-dihydroxy-5-nitrophenyl) -nn-diethyl-2-propenamid. Dens empiriske formel er C 14 H 15 N 3 O 5 Og dens strukturelle formel er:
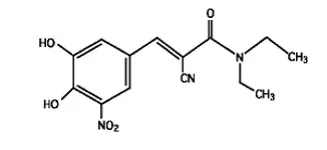 |
Stalevo leveres som tabletter i 6 styrker:
Stalevo 50: 12,5 mg carbidopa 50 mg levodopa og 200 mg entacapone
Stalevo 75: 18,75 mg carbidopa 75 mg levodopa og 200 mg entacapone
Stalevo 100: 25 mg Carbidopa 100 mg levodopa og 200 mg entacapone
Stalevo125: 31,25 mg carbidopa 125 mg levodopa og 200 mg entacapone
Stalevo 150: 37,5 mg carbidopa 150 mg levodopa og 200 mg entacapone
Stalevo 200: 50 mg Carbidopa 200 mg levodopa og 200 mg entacapone
Inaktive ingredienser: Corn Starch Croscarmellose Sodium Glycerol 85% Hypromellose Magnesium Stearate Mannitol Polysorbate 80 Povidon Sucrose Rødjernoxid og titandioxid. Stalevo 50 Stalevo 100 og Stalevo 150 indeholder også gult jernoxid.
Anvendelser til Stalevo
Stalevo er indikeret til behandling af Parkinsons sygdom.
Stalevo kan bruges:
- At erstatte (med ækvivalente styrker for hver af de tre komponenter) Carbidopa/Levodopa og Entacapone, der tidligere blev administreret som individuelle produkter.
- At erstatte carbidopa/levodopa-terapi (uden entacapone), når patienter oplever tegn og symptomer på endof-dosis i slidning, og når de har taget en total daglig dosis af levodopa på 600 mg eller mindre og har ikke oplevet dyskinesier.
Dosering til Stalevo
Stalevo bør bruges som erstatning for patienter, der allerede er stabiliseret på ækvivalente doser af Carbidopa/Levodopa og Entacapone. Imidlertid kan nogle patienter, der er blevet stabiliseret på en given dosis Carbidopa/Levodopa, behandles med Stalevo, hvis der er truffet en beslutning om at tilføje entacapone (se under ). Terapi skal individualiseres og justeres i henhold til den ønskede terapeutiske respons.
Doseringsoplysninger
Den optimale daglige dosering af Stalevo skal bestemmes ved omhyggelig titrering hos hver patient.
Klinisk erfaring med daglige doser over 1600 mg entacapone er begrænset. Den maksimale anbefalede daglige dosis af Stalevo afhænger af den anvendte styrke. Det maksimale antal tabletter, der skal bruges i en 24-timers periode, er mindre med den højeste styrke (Stalevo 200) end med lavere styrker (se tabel 1). Undersøgelser viser, at perifer Dopa -dekarboxylase er mættet af carbidopa med ca. 70 mg pr. Dag til 100 mg pr. Dag. Patienter, der får mindre end denne mængde carbidopa, er mere tilbøjelige til at opleve kvalme og opkast.
Tabel 1: Maksimal anbefalet dosis af Stalevo i en 24-timers periode
| Stalevo doseringsstyrke | Maksimalt antal tabletter i en 24-timers periode |
| Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 | 8 |
| Stalevo 200 | 6 |
Konvertering af patienter fra Carbidopa Levodopa og Entacapone til Stalevo
Patienter, der i øjeblikket behandles med Entacapone 200 mg med hver dosis af ikke-udvidet frigivelse Carbidopa/Levodopa-tablet, kan skifte til den tilsvarende styrke af Stalevo, der indeholder de samme mængder levodopa og carbidopa. For eksempel kan patienter, der modtager en tablet Carbidopa/Levodopa 25 mg/100 mg og en tablet entacapone 200 mg ved hver administration, skifte til en enkelt Stalevo 100 -tablet (indeholdende 25 mg Carbidopa 100 mg levodopa og 200 mg entacapone).
Konvertering af patienter fra Carbidopa og Levodopa -produkter til Stalevo
Der er ingen erfaring med at overføre patienter, der i øjeblikket behandles med udvidede frigivelsesformuleringer af Carbidopa/Levodopa eller Carbidopa/Levodopa -produkter, der ikke kombineres i et forhold på 1: 4 mellem Carbidopa og Levodopa.
Patienter med en historie med moderat eller svær dyskinesier eller tager mere end 600 mg af levodopa -komponenten pr. Dag kræver sandsynligvis en reduktion i deres daglige levodopa -dosis, når entacapone tilføjes. Fordi dosisjustering af den individuelle carbidopa- eller levodopa-komponent ikke er mulig med faste dosisprodukter oprindeligt titrerer patienter til en dosis, der tolereres, og som opfylder deres individuelle terapeutiske behov ved hjælp af en separat carbidopa/levodopa-tablet (1: 4-forhold) plus en Entacapone-tablet. Når patientens individuelle dosis carbidopa/levodopa plus entacapone -dosis er blevet etableret ved hjælp af to separate tabletter; Skift patienten til en tilsvarende enkelt tablet af Stalevo.
Når der kræves mindre levodopa, reducerer den samlede daglige dosering af carbidopa/levodopa enten ved at reducere styrken af Stalevo ved hver administration eller ved at reducere administrationsfrekvensen ved at udvide tiden mellem doser.
Samtidig brug med andre anti-Parkinsons sygdomsmedicin
Antikolinergiske midler dopamin Agonister Monoamine oxidase (MAO) - B -hæmmere amantadin og andre standardlægemidler til Parkinsons sygdom kan anvendes samtidigt, mens Stalevo administreres; Dog kan doseringsjusteringer af den samtidige medicin eller Stalevo være påkrævet.
Fald eller afbrydelse af dosering
Undgå afbrydelse af Stalevo -dosering, fordi der er rapporteret om hyperpyrexia hos patienter, der pludselig afbryder eller reducerer deres brug af levodopa [se Advarsler og forholdsregler ].
Vigtige administrationsinstruktioner
Opdel ikke knus eller tygg Stalevo -tabletter. Administrer kun en tablet i hvert doseringsinterval. Alle styrker af Stalevo indeholder 200 mg entacapone. Kombination af flere tabletter eller dele af tabletter for at opnå en højere levodopa -dosis kan føre til en overdosis af entacapone.
Administrer Stalevo med eller uden mad. Imidlertid kan et højtfedt måltid med højt kalorieindhold forsinke absorptionen af levodopa med ca. 2 timer [se Klinisk farmakologi ].
Hvor leveret
Doseringsformularer og styrker
Hver Stalevo-tablet, der er leveret i 6 enkeltdosisstyrker, indeholder carbidopa og levodopa i et forhold på 1: 4 og en 200 mg dosis entacapone. Stalevo (Carbidopa Levodopa og Entacapone) leveres som filmbelagte tabletter til oral administration i følgende 6 styrker:
Stalevo 50 Filmbelagte tabletter indeholdende 12,5 mg carbidopa 50 mg levodopa og 200 mg entacapone. De runde bi-konvekse formede tabletter er brunlige eller grårøde uskadte og prægede LCE 50 på den ene side.
Stalevo 75 Filmbelagte tabletter indeholdende 18,75 mg carbidopa 75 mg levodopa og 200 mg entacapone. De ovalformede tabletter er lysebrunlige røde, der er ukornet og præget med kode LCE 75 på den ene side.
Stalevo 100 Filmbelagte tabletter indeholdende 25 mg carbidopa 100 mg levodopa og 200 mg entacapone. De ovalformede tabletter er brunlige- eller grå-røde ubehagelige og prægede LCE 100 på den ene side.
Stalevo 125 Filmbelagte tabletter indeholdende 31,25 mg carbidopa 125 mg levodopa og 200 mg entacapone. De ovale formede tabletter er lysebrune røde, der er ukorrekt og præget med kode LCE 125 på den ene side.
Stalevo 150 Filmbelagte tabletter indeholdende 37,5 mg carbidopa 150 mg levodopa og 200 mg entacapone. De langstrakte ellipseformede tabletter er brunlige eller grårøde uskadte og prægede LCE 150 på den ene side.
Stalevo 200 Filmbelagte tabletter indeholdende 50 mg carbidopa 200 mg levodopa og 200 mg entacapone. De ovale formede tabletter er mørkebrune røde, der er ucentreret og præget LCE 200 på den ene side.
Opbevaring og håndtering
Stalevo (Carbidopa Levodopa og Entacapone) leveres som filmbelagte tabletter til oral administration i følgende seks styrker:
Stalevo 50 film-coated tablets indeholdende 12,5 mg carbidopa 50 mg levodopa og 200 mg entacapone.
De runde bi-konvekse formede tabletter er brunlige eller grårøde uskadte og prægede LCE 50 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-805-01
Stalevo 75 film-coated tablets indeholdende 18,75 mg carbidopa 75 mg levodopa og 200 mg entacapone.
De ovale formede tabletter er lysebrunlige røde, der er ukornet og præget med kode LCE 75 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-809-01
Stalevo 100 film-coated tablets indeholdende 25 mg carbidopa 100 mg levodopa og 200 mg entacapone.
De ovale formede tabletter er brunlige- eller grå-røde ubehagelige og prægede LCE 100 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-816-01
Stalevo 125 film-coated tablets indeholdende 31,25 mg carbidopa 125 mg levodopa og 200 mg entacapone.
De ovale formede tabletter er lysebrune røde, der er ukorrekt og præget med kode LCE 125 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-827-01
Stalevo 150 film-coated tablets indeholdende 37,5 mg carbidopa 150 mg levodopa og 200 mg entacapone.
De langstrakte ellipseformede tabletter er brunlige eller grårøde uskadte og prægede LCE 150 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-834-01
Stalevo 200 film-coated tablets indeholdende 50 mg carbidopa 200 mg levodopa og 200 mg entacapone.
De ovale formede tabletter er mørkebrune røde, der er ucentreret og præget LCE 200 på den ene side.
HDPE -flaske på 100 tabletter NDC 52427-842-01
Opbevares ved 25 ° C (77 ° F); Udflugter tilladt til 15 ° C til 30 ° C (59 ° F til 86 ° F).
[Se USP -kontrolleret stuetemperatur .]
Dispens i tæt beholder (USP).
Fremstillet af: Orion Corporation Orion Pharma Orionintie 1 FI-02200 Espoo Finland. Distribueret af: Almatica Pharma LLC Morristown NJ 07960 USA. Revideret: maj 2020
Bivirkninger for Stalevo
Følgende bivirkninger diskuteres mere detaljeret i afsnittet Advarsler og forholdsregler: Mærkning:
- Falder i søvn under aktiviteter i dagligdagen og somnolens [se Advarsler og forholdsregler ]
- Hypotension /Ortostatisk hypotension og synkope [se Advarsler og forholdsregler ]
- Dyskinesi [se Advarsler og forholdsregler ]
- Depression og selvmord [se Advarsler og forholdsregler ]
- Hallucinationer/psykotisk lignende opførsel [se Advarsler og forholdsregler ]
- Impulskontrol og/eller tvangsmæssig adfærd [se Advarsler og forholdsregler ]
- Tilbagetrækning-fremkommende hyperpyrexia og forvirring [se Advarsler og forholdsregler ]
- Diarré og colitis [se Advarsler og forholdsregler ]
- Rhabdomyolyse [se Advarsler og forholdsregler ]
- Peptisk mavesår [se Advarsler og forholdsregler ]
Kliniske forsøg oplever
Fordi kliniske forsøg udføres under vidt forskellige tilstande, forekommer forekomsten af bivirkninger (antal unikke patienter, der oplever en bivirkning, der er forbundet med behandling/samlet antal patienter, der er behandlet), der er observeret i de kliniske forsøg med et lægemiddel, ikke direkte sammenlignet med forekomsten af bivirkninger i de kliniske forsøg med et andet lægemiddel og muligvis ikke afspejler forekomsten af bivirkninger, der er observeret i klinisk praksis.
Entacapone
De mest almindeligt observerede bivirkninger (forekomst mindst 3% større end placebo-forekomst) i den dobbeltblinde carbidopa-levodopa-placebo-kontrollerede forsøg med entacapone (n = 1003 patienter) forbundet med brugen af carbidopalevodopa-entacapone alene og ikke set ved en ækvivalent frekvens blandt placebo-behandlede patienter var: dyskinesia diaeRhea naUsaea og ikke ses ved en ækvivalent frekvens blandt placeringsboks-behandlede patienter: dyskinesiia diaeRhea naUsaeaeaeaeaehopeKines Hyperkines Hyperkines Hyperkines Hyperkines Hyperkines Hyperkines Abdominal smerte opkast tør mund og misfarvning af urin.
Forekomsten af behandlingsforskellen for for tidlig undersøgelse af undersøgelsen for entacapone med levodopa og dopa decarboxylaseinhibitor i de dobbeltblinde placebokontrollerede forsøg var 5%. Forekomsten af behandlingsforskellen for de hyppigste årsager til ophør med undersøgelsen var 2% for diarré og 1% for andre specifikke bivirkninger, herunder psykiatriske grunde dyskinesi/ hyperkinesias kvalme eller mavesmerter.
Forekomst af bivirkninger i kontrollerede kliniske undersøgelser af entacapone
Tabel 2 viser behandling af behandlingsoptagende bivirkninger, der forekom hos mindst 1% af patienterne behandlet med Carbidopa/Levodopa og 200 mg entacapone, der deltog i den dobbeltblinde placebokontrollerede studier, og det var numerisk mere almindelige i denne gruppe end i Carbidopa/Levodopa Plus Placebogruppe. I disse undersøgelser blev enten entacapone eller placebo tilsat til carbidopa/levodopa (eller benserazid/levodopa).
Tabel 2: Resumé af patienter med bivirkninger efter start af forsøgsmedicinsk administration mindst 1% i entacapone -gruppen og større end placebo
| System Organ Class Bivirkning | Carbidopa/Levodopa plus entacapone (n = 603) % af patienterne | Carbidopa/Levodopa plus placebo (n = 400) % af patienterne |
| Hud- og vedhængsforstyrrelser | ||
| Sveden steg | 2 | 1 |
| Muskuloskeletalsystemforstyrrelser | ||
| Rygsmerter | 5 | 3 |
| Central og perifere nervesystemforstyrrelser | ||
| Dyskinesi | 25 | 15 |
| Hyperkinesi | 10 | 5 |
| Hypokinesi | 9 | 8 |
| Svimmelhed | 8 | 6 |
| Særlige sanser Andre lidelser | ||
| Smag perversion | 1 | 0 |
| Psykiatriske lidelser | ||
| Angst | 2 | 1 |
| Somnolence | 2 | 0 |
| Agitation | 1 | 0 |
| Gastrointestinal systemforstyrrelser | ||
| Kvalme | 14 | 8 |
| Diarre | 10 | 4 |
| Mavesmerter | 8 | 4 |
| Forstoppelse | 6 | 4 |
| Opkast | 4 | 1 |
| Mund tør | 3 | 0 |
| Dyspepsi | 2 | 1 |
| Flatulens | 2 | 0 |
| Gastritis | 1 | 0 |
| Gastrointestinale lidelser nr | 1 | 0 |
| Forstyrrelser i respirationssystemer | ||
| Dyspnø | 3 | 1 |
| Blodpladeblødning og koagulation Lidelser | ||
| Purpura | 2 | 1 |
| Urinsystemforstyrrelser | ||
| Misfarvning af urin | 10 | 0 |
| Krop som helgeneralforstyrrelser | ||
| Træthed | 6 | 4 |
| Asthenia | 2 | 1 |
| Forstyrrelser i modstandsmekanismer | ||
| Infektionsbakteriel | 1 | 0 |
Oplevelse af postmarketing
Følgende spontane rapporter om bivirkninger, der midlertidigt er forbundet med entacapone eller Stalevo, er blevet identificeret siden markedsindførelsen og ikke er anført i tabel 2., fordi disse reaktioner rapporteres frivilligt fra en population af ukendt størrelse, er det ikke altid muligt at pålideligt estimere deres frekvens eller etablere årsagsforhold til entacapone eller Stalevo -eksponering.
Hepatitis med hovedsageligt kolestatiske træk er rapporteret.
Effekter af køn og alder på bivirkninger
Der blev ikke observeret nogen forskelle i hastigheden af bivirkninger, der kan henføres til entacapone alene efter alder eller køn.
Lægemiddelinteraktioner for Stalevo
MAO -hæmmere
Patienter, der får ikke -selektive MAO -hæmmere og carbidopa levodopa og entacapone, kan være i fare for øget adrenerg tone. Derfor er brugen af Stalevo kontraindiceret til patienter, der får ikke -selektive MAO -hæmmere [se Kontraindikationer ].
Lægemidler metaboliseret af Catechol-O-Methyltransferase (COMT)
Lægemidler, der er kendt for at være metaboliseret af COMT, såsom isoproterenol epinephrin norepinephrin dopamin dobutamin alpha-methyldopa apomorfin isoetherin og bitolterol bør administreres med forsigtighed hos patienter, der får entakapone uanset indgivelsesruten (herunder inhalation), da deres interaktion kan resultere i, at hjertetilvågning muligvis er gennemgå [Se Advarsler og forholdsregler ].
Antihypertensive agenter
Symptomatisk Postural hypotension er forekommet, når carbidopa/levodopa blev føjet til behandlingen af patienter, der fik antihypertensive lægemidler. Ved startterapi med Stalevo -doseringsjustering af antihypertensivt lægemiddel kan være påkrævet.
Tricykliske antidepressiva
Der har været rapporter om bivirkninger, herunder hypertension og dyskinesi, der er resultatet af den samtidige anvendelse af tricyklisk Antidepressiva og Carbidopa/Levodopa.
Dopamin D2 -receptorantagonister
Dopamin D2 -receptorantagonister (f.eks. Metoclopramid -phenothiaziner butyrophenoner risperidon) kan reducere de terapeutiske virkninger af levodopa.
Isoniazid
Isoniazid may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Phable
Det er rapporteret, at de gavnlige virkninger af levodopa i Parkinsons sygdom er vendt af phenytoin. Patienter, der tager phenytoin med carbidopa/levodopa, skal observeres omhyggeligt for tab af terapeutisk respons. Stalevo -dosering bør øges som klinisk nødvendigt hos patienter, der modtager phenytoin.
Papaverin
Det er rapporteret, at de fordelagtige virkninger af levodopa i Parkinsons sygdom er vendt af papaverin. Patienter, der tager papaverin med carbidopa/levodopa, skal observeres omhyggeligt for tab af terapeutisk respons. Stalevo -dosering bør øges som klinisk nødvendigt hos patienter, der får papaverin.
Jernsalte
Jernsalte eller multi -vitaminer, der indeholder jernsalte, skal administreres med forsigtighed. Jernsalte kan danne chelater med levodopa carbidopa og entacapone og følgelig reducere biotilgængeligheden af levodopa carbidopa og entacapone.
Lægemidler, der er kendt for at forstyrre galden udskillelse af glukuronidering og tarm beta-glucuronidase
Da de fleste entacapone -udskillelse er via endog Der skal udvises forsigtighed, når medikamenter, der er kendt for at forstyrre galdeudskillelsesglucuronidering og tarmbeta-glucuronidase, gives samtidigt med entacapone. Disse inkluderer probenecid -cholestyramin og nogle antibiotika (f.eks. Erythromycin rifampicin ampicillin og chloramphenicol).
Lægemidler metaboliseret via CYP2C9 (f.eks. Coumadin)
Doseringen af Stalevo skal justeres som klinisk nødvendigt hos patienter, der bruger andre lægemidler, der metaboliseres via CYP2C9. En interaktionsundersøgelse hos raske frivillige entacapone øgede AUC for R-Warfarin i gennemsnit med 18% og INR-værdierne i gennemsnit med 13%. Tilfælde af øget INR hos patienter, der samtidig ved hjælp af warfarin er rapporteret under den post-godkendelse af entacapone. Således anbefales overvågning af INR, når Stalevo -behandling initieres til patienter, der modtager warfarin.
Advarsler for Stalevo
Inkluderet som en del af FORHOLDSREGLER afsnit.
Forholdsregler for Stalevo
Følgende bivirkninger, der er beskrevet i dette afsnit, er relateret til mindst en af komponenterne i Stalevo (dvs. levodopa carbidopa og/eller entacapone) baseret på sikkerhedserfaringen i kliniske forsøg (især pivotale forsøg) eller i postmarkedsrapporter.
Falder i søvn under aktiviteter i dagligdagen og somnolens
Patienter med Parkinsons sygdom behandlet med Stalevo eller andre Carbidopa/Levodopa -produkter har pludselig rapporteret, at de falder i søvn uden forudgående advarsel om søvnighed, mens de deltog i aktiviteter i dagligdagen (inklusive drift af motorkøretøjer). Nogle af disse episoder resulterede i ulykker. Selvom mange af disse patienter rapporterede om somnolens, mens de tog entacapone, opfattede nogle ikke advarselsskilte, såsom overdreven døsighed og troede, at de var opmærksomme umiddelbart før begivenheden. Nogle af disse begivenheder er rapporteret at forekomme op til et år efter påbegyndelse af behandlingen.
Somnolence was reported in 2% of patients taking entacapone og 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for døsighed or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge døsighed or sleepiness until directly questioned about døsighed or sleepiness during specific activities. Patients who have already experienced somnolence og/or an episode of sudden sleep onset should not participate in these activities during treatment with Stalevo.
Før han indledte behandling med Stalevo rådgiver patienter om potentialet til at udvikle døsighed og specifikt spørge om faktorer, der kan øge denne risiko, såsom brug af samtidig sedating medicin og tilstedeværelsen af søvnforstyrrelser. Hvis en patient udvikler søvnighed om dagen eller episoder med at falde i søvn under aktiviteter, der kræver aktiv deltagelse (f.eks. Samtaler, der spiser osv.), Skal Stalevo normalt afbrydes [se Dosering og administration og Advarsler og forholdsregler ]. If the decision is made to continue Stalevo patients should be advised not to drive og to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Hypotension Orthostatic Hypotension And Syncope
Rapporter om synkope var generelt hyppigere hos patienter i begge behandlingsgrupper, der havde haft en forudgående episode af dokumenteret hypotension (selvom episoderne af synkope opnået ved historien selv ikke var dokumenteret med vital tegnmåling). Hypotension ortostatisk hypotension og synkope observeres hos patienter behandlet med lægemidler, der øger den centrale dopaminergiske tone inklusive Stalevo.
Dyskinesi
Dyskinesi (ufrivillig movements) may occur or be exacerbated at lower dosages og sooner with Stalevo than with preparations containing only carbidopa og levodopa. The occurrence of dyskinesias may require dosage reduction.
I pivotale forsøg var behandlingsforskellens forekomst af dyskinesi 10% og for carbidopa-levodopa plus 200 mg entacapone. Selvom det at reducere dosis af levodopa kan forbedre denne bivirkning, fortsatte mange patienter i kontrollerede forsøg med at opleve hyppige dyskinesier på trods af en reduktion i deres dosis levodopa. Behandlingsforskellens forekomst af undersøgelse af undersøgelsen for dyskinesi var 1% for carbidopa-levodopa-entacapone.
Depression og selvmord
Alle patienter skal observeres omhyggeligt for udvikling af depression med samtidig selvmordstendenser. Patienter med tidligere eller nuværende psykoser skal behandles med forsigtighed.
Hallucinationer og/eller psykotisk lignende opførsel
Dopaminergisk terapi hos patienter med Parkinsons sygdom har været forbundet med hallucinationer. Hallucinationer førte til ophør af medikamentet og for tidlig tilbagetrækning fra kliniske forsøg hos henholdsvis 0,8% og 0% af patienterne behandlet med henholdsvis Carbidopa Levodopa entacapone og Carbidopa Levodopa. Hallucinationer førte til hospitalisering hos 1,0% og 0,3% af patienterne i henholdsvis Carbidopa Levodopa Entacapone og Carbidopa Levodopa. Agitation forekom hos 1% af patienterne behandlet med carbidopa levodopa entacapone og 0% behandlet med carbidopa levodopa.
Impulskontrol og/eller tvangsmæssig adfærd
Rapporter efter markedsføring antyder, at patienter, der er behandlet med anti-Parkinson-medicin, kan opleve intense trang til at gamble øgede seksuelle trang til intense trang til at bruge penge ukontrolleret og andre intense trang. Patienter kan ikke være i stand til at kontrollere disse trang, mens de tager en eller flere af de medicin, der generelt anvendes til behandling af Parkinsons sygdom, og som øger den centrale dopaminergiske tone inklusive entacapone taget med levodopa og carbidopa. I nogle tilfælde blev det rapporteret, at ikke alle disse trang var stoppet, når dosis af anti-Parkinson-medicin blev reduceret eller ophørt. Fordi patienter muligvis ikke genkender denne adfærd som unormal, er det vigtigt for ordinerende at specifikt spørge patienter eller deres plejere om udviklingen af nye eller øgede spil opfordrer trakes seksuelle trang ukontrollerede udgifter eller andre trang, mens de behandles med entacapone. Læger skal overveje dosisreduktion eller stoppe Stalevo, hvis en patient udvikler sådanne trang, mens de tager Stalevo [se Dosering og administration Advarsler og forholdsregler ].
Tilbagetrækning-fremkommende hyperpyrexi og forvirring
Tilfælde af hyperpyrexi og forvirring, der ligner neuroleptisk malignt syndrom (NMS), er rapporteret i forbindelse med dosisreduktion eller tilbagetrækning af terapi med Carbidopa Levodopa og Entacapone. I nogle tilfælde blev der imidlertid rapporteret om hyperpyrexi og forvirring efter påbegyndelse af behandling med entacapone. Hyperpyrexi og forvirring er ualmindelige, men de kan være livstruende med en række forskellige funktioner, herunder hyperpyrexia/feber/hypertermi muskelstivhed ufrivillig bevægelser ændret bevidsthed/mental status ændrer delirium autonome dysfunktion Leukocytose myoglobinuri og øget serum myoglobin).
Hvis en patient skal afbryde eller reducere deres daglige dosis af Stalevo, skal dosis langsomt reduceres med tilsyn fra en sundhedsudbyder [se Dosering og administration ]. Specific methods for tapering entacapone have not been systematically evaluated.
Diarre And Colitis
I kliniske forsøg med entacapone -diarré udviklede sig i 60 af 603 (NULL,0%) og 16 af 400 (NULL,0%) af patienterne behandlet med 200 mg entacapone eller placebo i kombination med levodopa og DOPA decarboxylaseinhibitor. Hos patienter, der blev behandlet med entacapon -diarré, var generelt mild til moderat i sværhedsgrad (NULL,6%), men blev betragtet som alvorlig i 1,3%. Diarré resulterede i tilbagetrækning hos 10 af 603 (NULL,7%) patienter 7 (NULL,2%) med mild og moderat diarré og 3 (NULL,5%) med svær diarré. Diarré løftes generelt efter seponering af entacapone. To patienter med diarré blev indlagt på hospitalet. Typisk præsenterer diarré inden for 4 til 12 uger efter, at Entacapone er startet, men det kan vises så tidligt som den første uge og så sent som mange måneder efter påbegyndelsen af behandlingen. Diarré kan være forbundet med vægttab dehydrering og hypokalæmi.
Oplevelse af postmarked har vist, at diarré kan være et tegn på medikamentinduceret mikroskopisk colitis primært lymfocytisk colitis. I disse tilfælde har diarré normalt været moderat til svær vandig og ikke-blodig til tider forbundet med dehydrering af abdominal smertestab og hypokalæmi. I de fleste tilfælde løste diarré og andre colitis-relaterede symptomer eller forbedrede signifikant, når entacapone-behandling blev stoppet. Hos nogle patienter med biopsi bekræftede colitis -diarré løst eller signifikant forbedret efter seponering af entacapone, men gentaget efter tilbagetrækning med entacapone.
Hvis der mistænkes for langvarig diarré, skal lægemidlet afbrydes, og passende medicinsk terapi overvejes. Hvis årsagen til langvarig diarré forbliver uklar eller fortsætter efter at have stoppet entacapone, skal der overvejes yderligere diagnostiske undersøgelser, herunder koloskopi og biopsier.
Rhabdomyolyse
Tilfælde af svær rhabdomyolyse er rapporteret med entacapone, når de bruges i kombination med carbidopa og levodopa. Alvorlig langvarig motorisk aktivitet inklusive dyskinesi kan muligvis redegøre for rhabdomyolyse. De fleste af tilfældene blev manifesteret af myalgi og øgede værdier af kreatinphosphokinase (CPK) og myoglobin. Nogle af reaktionerne omfattede også feber og/eller ændring af bevidstheden. Det er også muligt, at rhabdomyolyse kan være et resultat af det syndrom, der er beskrevet i tilbagetrækning-fremkommende hyperpyrexi og forvirring [se Advarsler og forholdsregler ].
Interaktion med lægemidler, der er metaboliseret af COMT
Lægemidler, der er kendt for at være metaboliseret af COMT, såsom isoproterenol epinephrin norepinephrin dopamin dobutamin alpha-methyldopa apomorfin isoetherin og bitolterol bør administreres med forsigtighed hos patienter, der får entakapon uanset indførelsesruten (herunder inhalation), da deres interaktion kan resultere i, at hjerteriets rate rate rate og/or eller øget blodtryk.
Fibrotiske komplikationer
Tilfælde af retroperitoneal fibrose lungeinfiltrater pleural effusion og pleural fortykning er rapporteret hos nogle patienter behandlet med ergot -afledte dopaminergiske midler. Disse komplikationer kan løse, når lægemidlet ophører, men fuldstændig opløsning forekommer ikke altid. Selvom disse bivirkninger kan være relateret til ergolinstrukturen af disse forbindelser, er en mulig årsagsrolle af ikke -ergot -afledte lægemidler (f.eks. Entacapone levodopa), som øger dopaminergisk aktivitet, også blevet overvejet. Den forventede forekomst af fibrotiske komplikationer er så lav, at selvom entacapone forårsagede disse komplikationer i hastigheder, der ligner dem, der kan henføres til andre dopaminergiske terapier, er det usandsynligt, at det ville have været påvist i en kohort af størrelsen udsat for entacapone under dens kliniske udvikling. Der er rapporteret om fire tilfælde af lungefibrose under klinisk udvikling af entacapone; 3 af disse patienter blev også behandlet med pergolid og 1 med bromocriptin. Varigheden af behandlingen med Entacapone varierede fra 7 måneder til 17 måneder.
Peptisk mavesår
Som med levodopa -behandling med Stalevo kan øge muligheden for øvre gastrointestinal blødning hos patienter med en historie med mavesår.
Leverskrivning i leveren
Patienter med nedsat leverfunktion skal behandles med forsigtighed [se Klinisk farmakologi ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Laboratorieundersøgelser
Abnormaliteter i laboratorieundersøgelser kan omfatte forhøjninger af leverfunktionstest, såsom alkalisk phosphatase SGOT (AST) SGPT (ALT) mælketdehydrogenase og bilirubin. Abnormiteter i blod Urea Nitrogen- og positiv Coombs -test er også rapporteret. Almindelige niveauer af blodurinstofnitrogenkreatinin og urinsyre er lavere under administration af Stalevo end med levodopa.
Stalevo may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
Der skal udvises forsigtighed ved fortolkning af plasma- og urinniveauerne af catecholamines og deres metabolitter hos patienter på Carbidopa/Levodopa -terapi.
Oplysninger om patientrådgivning
Falder i søvn under aktiviteter i dagligdagen og somnolens
Rådgiv patienter om potentialet for beroligende effekter forbundet med Stalevo inklusive somnolens og muligheden for at falde i søvn, mens de deltager i aktiviteter i dagligdagen. Fordi somnolens kan være en hyppig bivirkning med potentielt alvorlige konsekvenser, bør patienter ikke drive et motorkøretøjs drift af tunge maskiner eller deltage i andre potentielt farlige aktiviteter, indtil de har fået tilstrækkelig erfaring med Stalevo til at afgøre, om det påvirker deres mentale og/eller motoriske præstation negativt [se Advarsler og forholdsregler ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Rådgiver patienter til at tale med deres receptpligtige sundhedsydelser, før de tager alkohol -beroligende medicin eller andre CNS -depressiva (f.eks. Benzodiazepiner antipsykotika antidepressiva osv.) På grund af de mulige additive effekter i kombination med Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Rådgiv patienter om, at de kan udvikle symptomatiske (eller asymptomatiske) posturale (ortostatiske) hypotension eller ikke -ortostatisk hypotension, mens de tager Stalevo. Hypotension/ortostatisk hypotension kan forekomme hyppigere under den indledende terapi. Patienter bør ikke stige hurtigt efter at have siddet eller liggende, især hvis de har gjort det i langvarige perioder og især ved påbegyndelse af behandling med Stalevo.
Rådgiv patienter om potentialet for synkope hos patienter, der bruger dopaminagonister. Af denne grund informerer patienter om muligheden for at synkope, mens de tager Stalevo [se Advarsler og forholdsregler ].
Dyskinesis
Informer patienter om, at Stalevo kan forårsage og/eller forværre allerede eksisterende dyskinesier [se Advarsler og forholdsregler ].
Hallucinationer og/eller psykotisk lignende opførsel
Informer patienter om, at hallucinationer og anden psykotisk lignende opførsel kan forekomme, mens Stalevo [se Advarsler og forholdsregler ].
Impulskontrol og/eller tvangsmæssig adfærd
Rådgiv patienter om, at de kan opleve impulskontrol og/eller tvangsmæssig adfærd, mens de tager en eller flere af de medicin, der bruges til behandling af Parkinsons sygdom, herunder Stalevo. Spørg patienter om udviklingen af nye eller øgede spiludtrængninger opfordrer trakes seksuelle trang til opfordringer til ukontrollerede udgifter eller andre intense trang, mens de behandles med Stalevo. Rådgiv patienter om at informere deres læge eller sundhedsudbyder, hvis de oplever nye eller øgede spiludtrækninger øgede seksuelle trang eller andre intense trang, mens de tager Stalevo. Læger skal overveje dosisreduktion eller stoppe medicinen, hvis en patient udvikler sådanne trang, mens de tager Stalevo [se Advarsler og forholdsregler ].
Tilbagetrækning-fremkommende hyperpyrexi og forvirring
Rådgiv patienter om, at de kan udvikle feber og forvirring som en del af et syndrom, der ligner NMS og muligvis med andre kliniske træk (f.eks. Muskelstivhed autonom dysfunktion hyper- eller hypotension osv.). Dette feber- og forvirringssyndrom kan især forekomme med dosisreduktion eller tilbagetrækning af Stalevo, men kan også udvikle sig efter påbegyndelse af behandlingen. Rådgive patienter om at kontakte deres sundhedsudbyder, hvis de ønsker at afbryde eller mindske dosis af Stalevo og til at kontakte en sundhedsudbyder, hvis de udvikler feber og forvirring [se Advarsler og forholdsregler ].
Diarre And Colitis
Informer patienterne om, at diarré kan forekomme med Stalevo, og det kan have en forsinket begyndelse. Undertiden kan langvarig diarré være forårsaget af colitis (betændelse i tarmtarmen). Patienter med diarré skal drikke væsker for at opretholde tilstrækkelig hydrering og overvåge for vægttab. Hvis diarré forbundet med Stalevo forlænges, forventes det at afbryde lægemidlet at føre til opløsning. Hvis diarré fortsætter efter at have stoppet Stalevo, kan det være nødvendigt med yderligere diagnostiske undersøgelser. I nogle tilfælde kan diarré være forbundet med colitis [se Advarsler og forholdsregler ].
Rhabdomyolyse
Rådgiv patienter om, at de kan udvikle rhabdomyolyse og myalgi, hvis de oplever langvarig motorisk aktivitet inklusive dyskinesi. Denne begivenhed kan også være forbundet med feber og forvirring [se Advarsler og forholdsregler ].
Kvalme And Opkast
Informer patienter om, at Stalevo kan forårsage kvalme og opkast kan forekomme hyppigere under den første terapi og kan kræve dosisjustering.
Brug til brug
Instruer patienter om kun at tage Stalevo som foreskrevet. Instruer patienter om kun at tage en enkelt tablet af Stalevo i hvert doseringsinterval. Instruer patienter om ikke at tage flere tabletter eller yderligere dele af tabletter for at opnå en højere dosis levodopa. Rådgiv patienter om ikke at splitte knus eller tygge Stalevo.
Informer patienten om, at Stalevo er en formulering af carbidopa/levodopa kombineret med entacapone, der er designet til at begynde frigivelse af ingredienser inden for 30 minutter efter indtagelse. Det er vigtigt, at Stalevo tages med regelmæssige intervaller i henhold til den tidsplan, der er beskrevet af lægen. FORSIGTIG Patienten om ikke at ændre det foreskrevne doseringsregime og ikke at tilføje yderligere Antiparkinson -medicin, herunder andre Carbidopa/Levodopa -præparater uden først at konsultere lægen.
Rådgive patienter om, at episoder (iført lægemiddeleffekt) forekommer i slutningen af doseringsintervallet, men uforudsigelige episoder kan forekomme når som helst. Rådgive patienten om at underrette en sundhedsudbyder om mulige behandlingsjusteringer, hvis en sådan respons udgør et problem for patientens hverdag.
Rådgive patienter om, at mørk farve (rødbrun eller sort) kan optræde i spyt urin eller sved efter at have taget Stalevo. Selvom farven ser ud til at være klinisk ubetydelige beklædningsgenstande kan blive misfarvet.
Rådgive patienter om, at en ændring i diæt til fødevarer, der er høje i protein, kan forsinke absorptionen af levodopa. Overdreven surhed forsinker også mavetømning og dermed forsinker absorptionen af levodopa. Jernsalte (såsom i tabletter med flere vitamin) kan også reducere effektiviteten af Stalevo.
Graviditet
Instruer patienter om at underrette deres sundhedsudbyder, hvis de bliver gravide eller har til hensigt at blive gravide under terapi [se Brug i specifikke populationer ].
Amning
Instruer patienter om at underrette deres sundhedsudbyder, hvis de har til hensigt at amme eller amme et spædbarn [se Brug i specifikke populationer ].
Ikke -klinisk toksikologi
Karcinogenese mutagenese nedskrivning af fertilitet
Carcinogenese
Hos rotter resulterede oral administration af carbidopa-levodopa i 2 år ikke i bevis for kræftfremkaldende stoff ved doser på cirka 2 gange (carbidopa) -4 gange (levodopa) den maksimale anbefalede humane dosis (MRHD).
To-årige carcinogenicitetsundersøgelser af entacapone blev udført hos mus og rotter. Hos mus blev der ikke observeret nogen stigning i tumorer ved orale doser på 100 200 og 400 mg/kg/dag. Ved den højeste dosis testede plasmaeksponeringer (AUC) var 4 gange højere end hos mennesker ved den maksimale anbefalede daglige dosis (MRDD) på 1600 mg. Hos rotter, der blev administreret orale doser på 20 90 eller 400 mg/kg/dag, blev der observeret en øget forekomst af nyretørulære adenomer og carcinomer hos mænd i den højeste testede dosis. Plasma -AUC'er i den højere dosis, der ikke var forbundet med forøgede nyretumorer (90 mg/kg/dag), var cirka 5 gange det hos mennesker ved mRDD af entacapone.
Det kræftfremkaldende potentiale for entacapone, der administreres i kombination med carbidopa-levodopa, er ikke blevet evalueret.
Mutagenese
Carbidopa var mutagen i in vitro -bakteriel omvendt mutation (AMES) -assay i nærvær og fravær af metabolisk aktivering og i in vitro muselymfom thymidinkinase (TK) assay i fravær af metabolisk aktivering. Carbidopa var negativ i in vivo -musemikronukleus -assayet.
Entacapone was mutagenic og clastogenic in the in vitro mouse lymphoma tk assay in the presence og absence of metabolic activation og was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapone either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus og in the Ames assays.
Værdiforringelse af fertiliteten
I reproduktionsundersøgelser blev der ikke fundet nogen effekter på fertiliteten hos rotter, der modtog carbidopa-levodopa i doser på cirka 2 gange (carbidopa) -4 gange (levodopa) MRHD.
Hos rotter behandlet oralt med entacapone (op til 700 mg/kg/dag) blev der ikke observeret nogen effekter på fertilitet eller generel reproduktionsydelse. Plasmaeksponeringer (AUC) ved den højeste testede dosis var cirka 30 gange, at hos mennesker ved MRHD af entacapone. Forsinket parring var tydeligt hos kvinder i den højeste testede dosis.
Brug i specifikke populationer
Graviditet
Risikooversigt
Der er ingen tilstrækkelige data om udviklingsrisikoen forbundet med brugen af Stalevo hos gravide kvinder. I dyrs administration af carbidopa-levodopa eller entacapone under graviditet var der forbundet med udviklingstoksicitet, herunder øgede forekomster af føtal misdannelser (se Data ). Den estimerede baggrundsrisiko for store fødselsdefekter og spontanabort i den angivne befolkning er ukendt. I den amerikanske generelle befolkning er de estimerede baggrundsrisici for vigtige fødselsdefekter og spontanabort i klinisk anerkendte graviditeter henholdsvis 2 til 4% og 15 til 20%.
Data
Dyredata
I ikke-kliniske undersøgelser, hvor carbidopa-levodopa blev administreret til gravide dyr, blev øgede forekomster af viscerale og skeletmisdannelser observeret i kaniner i alle doser og forhold mellem carbidopa-levodopa testet, der varierede fra 10 gange (carbidopa) -5 gange (levodopa) til 20 gange (carbidopa) -10 gange (Levodopa) den maksimale hæmmede dosel (MRHD) på 1600 mg/dag. Hos rotter var der et fald i antallet af levende hvalpe leveret af dæmninger, der modtog cirka to gange (carbidopa) -five gange (levodopa) MRHD i hele organogenese. Der blev ikke observeret nogen effekter på misdannelsesfrekvenser hos mus, der modtog op til 20 gange MRHD for carbidopa-levodopa.
I embryo-føtaludviklingsundersøgelser af entacapone-gravide dyr modtog doser på op til 1000 mg/kg/dag (rotter) eller 300 mg/kg/dag (kaniner) i hele organogenese. Forøgede forekomster af føtalvariationer var tydelige i kuld fra rotter behandlet med den højeste dosis i fravær af åbenlyse tegn på moders toksicitet. Mødreplasma -entacapone -eksponeringen (AUC), der var forbundet med denne dosis, var cirka 34 gange, at hos mennesker ved MRHD. Forøgede frekvenser af aborter og sene/samlede resorptioner og nedsatte føtalvægte blev observeret i kulderne af kaniner behandlet med mødre giftige doser på 100 mg/kg/dag (plasma -AUC'er mindre end hos mennesker ved MRHD) eller større. Der var ingen stigninger i misdannelsesgraden i disse undersøgelser.
Når entacapone blev administreret til kvindelige rotter før parring, og under tidlig drægtighed blev der observeret en øget forekomst af føtal øje -anomalier (makrophthalmia -mikrophthalmia -anophthalmia) i dæmperne behandlet med doser af 160 mg/kg/dag (plasma aucs syv gange, der i humans ved MRHD) eller større i fraværmen af maternalstoksitet. Administration af op til 700 mg/kg/dag (plasma AUCS 28 gange, at hos mennesker ved MRHD) til rotter under den sidste del af drægtigheden og i hele laktation frembragte ingen bevis for udviklingsvirkning i afkom.
Amning
Risikooversigt
Levodopa er påvist i human mælk efter administration af carbidopa-levodopa. Der er ingen data om tilstedeværelsen af entacapone eller carbidopa i human mælk Effekten af levodopa carbidopa eller entacapone på det ammede spædbarn eller virkningerne på mælkeproduktionen. Imidlertid kan inhibering af amning forekomme, fordi levodopa reducerer sekretionen af prolactin [se Klinisk farmakologi ]. Carbidopa og entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone og/or metabolites in milk up to 2 to 3 times that in plasma. The developmental og health benefits of breastfeeding should be considered along with the mother's clinical need for Stalevo og any potential adverse effects on the breastfed infant from Stalevo or from the underlying maternal condition.
Pædiatrisk brug
Sikkerhed og effektivitet hos pædiatriske patienter er ikke etableret.
Geriatrisk brug
Af det samlede antal forsøgspersoner i kliniske undersøgelser af Stalevo var 43,8% 65 år gamle og derover, mens 7,2% var 75 år gamle og derover. Der blev ikke observeret nogen samlede forskelle i sikkerhed eller effektivitet mellem disse forsøgspersoner og yngre forsøgspersoner og andre rapporterede kliniske erfaringer har ikke identificeret forskelle i svar mellem de ældre og yngre patienter; Imidlertid kan større følsomhed for nogle ældre personer ikke udelukkes.
Stalevo tablets have not been studied in Parkinsons sygdom patients or in healthy volunteers older than 75 years [see Klinisk farmakologi ].
Nedskærmning af nyren
Nedskrivning i nyren påvirker ikke farmakokinetik af entacapone. Der er ingen undersøgelser af farmakokinetikken i levodopa og carbidopa hos patienter med nedsat nyrefunktion [se Klinisk farmakologi ].
Leverskrivning i leveren Or Biliary Obstruction
Der er ingen undersøgelser af farmakokinetikken af Carbidopa og Levodopa hos patienter med leverfunktion. Stalevo bør administreres forsigtigt til patienter med galdeobstruktion eller leversygdom, da udskillelse af galdefag ser ud til at være den vigtigste rute for udskillelse af entacapone og leverhæmning havde en signifikant effekt på farmakokinetikken for entacapone, når 200 mg entacapone blev administreret alene [se [se Klinisk farmakologi ].
Overdoseringsoplysninger til Stalevo
Tegn og symptomer på overdosering
Der er meget få tilfælde af overdosis med levodopa rapporteret i den offentliggjorte litteratur. Baseret på de tilgængelige oplysninger kan de akutte symptomer på levodopa og dopa decarboxylaseinhibitor overdosis forventes at opstå fra dopaminerg overstimulering. Doser af nogle få gram kan resultere i CNS -forstyrrelser med en stigende sandsynlighed for hjerte -kar -forstyrrelse (f.eks. Hypotension takykardi) og mere alvorlige psykiatriske problemer ved højere doser. En isoleret rapport om rhabdomyolyse og en anden af kortvarig nyreinsufficiens antyder, at levodopa overdosis kan give anledning til systemiske komplikationer sekundært til dopaminerg overstimulering.
COMT-hæmning ved entacapone-behandling er dosisafhængig. En massiv overdosis af entacapone kan teoretisk producere en 100% inhibering af COMT-enzymet hos mennesker og derved forhindre O-methylering af endogene og eksogene katekoler.
I kliniske forsøg var den højeste enkelt dosis af entacapone administreret til mennesker 800 mg, hvilket resulterede i en plasmakoncentration på 14,1 mcg pr. Ml. Den højeste daglige dosis, der blev givet til mennesker, blev 2400 mg administreret i en undersøgelse som 400 mg seks gange dagligt med Carbidopa/Levodopa i 14 dage i 15 Parkinsons sygdomspatienter og i en anden undersøgelse som 800 mg tre gange dagligt i 7 dage i 8 raske frivillige. Ved denne daglige dosis var de maksimale plasmakoncentrationer af entacapone i gennemsnit 2,0 mcg pr. Ml (ved 45 minutter sammenlignet med 1,0 mcg pr. Ml og 1,2 mcg pr. Ml med 200 mg entacapon ved 45 minutter.). Mavesmerter og løs afføring var de mest almindeligt observerede bivirkninger under denne undersøgelse. Daglige doser så høje som 2000 mg entacapone er blevet administreret som 200 mg 10 gange dagligt med carbidopa/levodopa eller benserazid/levodopa i mindst 1 år hos 10 patienter i mindst 2 år hos 8 patienter og i mindst 3 år hos 7 patienter. Generelt er imidlertid klinisk erfaring med daglige doser over 1600 mg begrænset.
Håndtering af overdosering
Hospitalisering anbefales, og generelle støttende foranstaltninger bør anvendes sammen med øjeblikkelig gastrisk skylning og gentagne doser af kul over tid. Dette kan fremskynde eliminering af entacapon især ved at reducere dens absorption og reabsorption fra GI -kanalen. Intravenøse væsker skal administreres fornuftigt, og en passende luftvej opretholdes.
Respiratorisk kredsløb og nyrefunktion skal overvåges og passende understøttende foranstaltninger anvendes. Elektrokardiografisk overvågning bør indføres, og patienten observeres omhyggeligt for udviklingen af arytmier; Om nødvendigt bør der gives passende antiarytmisk terapi. Muligheden for, at patienten kan have taget andre lægemidler, der øger risikoen for medikamentinteraktioner (især katekolstrukturerede lægemidler), bør tages i betragtning. Indtil videre er der ikke rapporteret om nogen erfaring med dialyse; Derfor er dens værdi i overdosering ikke kendt. Hæmodialyse eller hæmoperfusion vil sandsynligvis ikke reducere entacapon -niveauer på grund af dets høje binding til plasmaproteiner. Pyridoxin er ikke effektiv til at vende Stalevos handlinger.
Kontraindikationer for Stalevo
Stalevo is contraindicated in patients:
- Tager ikke -selektiv monoaminoxidase (MAO) hæmmere (f.eks. Phenelzin og tranylcypromin). Disse ikke -selektive MAO -hæmmere skal afbrydes mindst to uger før påbegyndelse af terapi med Stalevo.
- Med smalvinklet glaukom .
Klinisk farmakologi for Stalevo
Handlingsmekanisme
Levodopa
Aktuelle beviser tyder på, at symptomer på Parkinsons sygdom er relateret til udtømning af dopamin i corpus striatum. Administration af dopamin er ineffektiv i behandlingen af Parkinsons sygdom, fordi den ikke krydser blod-hjerne-barrieren. Imidlertid krydser Levodopa den metaboliske forløber for dopamin blod-hjerne-barrieren og konverteres formodentlig til dopamin i hjernen. Dette menes at være mekanismen, hvor Levodopa lindrer symptomerne på Parkinsons sygdom.
Carbidopa
Når levodopa administreres oralt, dekarboxyleres det hurtigt til dopamin i ekstracerebrale væv, så kun en lille del af en given dosis transporteres uændret til centralnervesystemet. Carbidopa inhiberer dekarboxyleringen af perifer levodopa, hvilket gør mere levodopa til rådighed til levering til hjernen.
Entacapone
Entacapone is a selective og reversible inhibitor of catechol-O-methyltransferase (COMT).
COMT katalyserer overførslen af methylgruppen af S-adenosyl-L-methionin til den fenoliske gruppe af substrater, der indeholder en catechol-struktur. Fysiologiske substrater af COMT inkluderer DOPA -catecholamines (dopamin noradrenalin og epinephrin) og deres hydroxylerede metabolitter. Når decarboxylering af levodopa forhindres ved at carbidopa COMT bliver det vigtigste metaboliserende enzym for levodopa katalyserer dets stofskifte til 3-methoxy-4- hydroxy-l-phenylalanin (3-AMD).
Farmakokinetik
Farmakokinetikken af Stalevo -tabletter er blevet undersøgt hos raske forsøgspersoner (alder 45 år til 75 år). Generelt efter administration af tilsvarende doser af levodopa carbidopa og entacapone som Stalevo eller som carbidopa og levodopa -produkt plus comtan (entacapone) tabletter de gennemsnitlige plasmakoncentrationer af levodopa carbidopa og entacapone er sammenlignelige.
Absorption og distribution
Både levodopa og entacapone absorberes hurtigt og elimineres, og deres distributionsvolumen er moderat lille. Carbidopa absorberes og elimineres lidt langsommere sammenlignet med levodopa og entacapone. Der er betydelige inter- og intra-individuelle variationer i absorptionen af levodopa carbidopa og entacapone især med hensyn til dens Cmax.
Fødevareeffekten på Stalevo-tabletten er ikke evalueret. Fordi Levodopa konkurrerer med visse aminosyrer til transport over tarmvæggen, kan absorptionen af levodopa være forringet hos nogle patienter efter at have spist et højt proteinmåltid. Måltider rig på store neutrale aminosyrer kan forsinke og reducere absorptionen af levodopa [se Oplysninger om patientrådgivning ].
Levodopa
De farmakokinetiske egenskaber af levodopa efter administration af enkeltdosis Stalevo (Carbidopa levodopa og entacapone) tabletter er sammenfattet i tabel 3.
Tabel 3: Farmakokinetiske egenskaber ved levodopa med forskellige tabletstyrker af Stalevo (gennemsnit ± SD)
| Tabletstyrke | AUC0 -∞ (nanogram • H via ML) | Cmax (nanogram pr. Ml) | Tmax (H) |
| 12,5 mg pr. 50 mg pr. 200 mg | 1040 ± 314 | 470 ± 154 | 1,1 ± 0,5 |
| 25 mg pr. 100 mg pr. 200 mg | 2910 ± 715 | 975 ± 247 | 1,4 ± 0,6 |
| 37,5 mg pr. 150 mg pr. 200 mg | 3770 ± 1120 | 1270 ± 329 | 1,5 ± 0,9 |
| 50 mg pr. 200 mg pr. 200 mg | 6115 ± 1536 | 1859 ± 455 | 1,76 ± 0,7 |
Levodopa is bound to plasma protein only to a minor extent (about 10% to 30%).
Carbidopa
Efter administration af Stalevo som en enkelt dosis til sunde mandlige og kvindelige forsøgspersoner blev den maksimale koncentration af carbidopa nået inden for 2,5 timer til 3,4 timer i gennemsnit. Den gennemsnitlige Cmax varierede fra ca. 40 nanogram pr. Ml til 225 nanogram pr. Ml og den gennemsnitlige AUC fra 170 nanogram • H pr. Ml til 1200 nanogram • H pr. Ml med forskellige Stalevo -styrker, der tilvejebringer 12,5 mg 25 mg 37,5 mg eller 50 mg carbidopa.
Carbidopa is approximately 36% bound to plasma protein.
Entacapone
Efter administration af Stalevo som en enkelt dosis til sunde mandlige og kvindelige forsøgspersoner blev den maksimale koncentration af entacapone i plasma nået inden for 0,8 timer til 1,2 timer i gennemsnit. Den gennemsnitlige Cmax for entacapone var ca. 1200 nanogram pr. Ml til 1500 nanogram pr. Ml og AUC 1250 nanogram • H pr. Ml til 1750 nanagram • H pr. Ml efter administration af forskellige Stalevo -styrker, der alle leverer 200 mg entacapone.
Plasmaproteinbindingen af entacapon er 98% over koncentrationsområdet på 0,4 mcg pr. Ml til 50 mcg pr. Ml. Entacapone binder hovedsageligt til serumalbumin.
Metabolisme og eliminering
Levodopa
Levodopas eliminering af levodopa den aktive del af den antiparkinson-aktivitet var 1,7 timer (område 1,1 timer til 3,2 timer).
Levodopa is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) og O-methylation by COMT.
Carbidopa
Eliminationshalveringstiden for Carbidopa var i gennemsnit 1,6 timer til 2 timer (område 0,7 timer til 4,0 timer).
Carbidopa is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid og α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapone
Eliminationshalveringstiden for Entacapone var i gennemsnit 0,8 time til 1 time (NULL,3 timer til 4,5 timer).
Entacapone is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapone og the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent og 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 C-mærket dosis af entacapone 10% af mærket forælder og metabolit udskilles i urin og 90% i fæces.
På grund af kort eliminering af halveringstider forekommer der ingen ægte ophobning af levodopa eller entacapone, når de administreres gentagne gange.
Nedskærmning af nyren
Entacapone
Farmakokinetikken af entacapon er blevet undersøgt efter en enkelt 200 mg entacapon -dosis hos personer med normal moderat og alvorligt nedsat nyrefunktioner uden levodopa og dopa decarboxylaseinhibitor coadministration. Der blev ikke fundet nogen signifikante effekter af nyrefunktion på farmakokinetikken af entacapone.
Levodopa And carbidopa
Ingen undersøgelser af farmakokinetikken af levodopa og carbidopa hos patienter med nedsat nyrefunktion.
Leverskrivning i leveren
Entacapone
Hepatisk svækkelse havde en signifikant effekt på farmakokinetikken for entacapone, da 200 mg entacapone blev administreret alene. En enkelt 200 mg dosis af entacapone uden levodopa og dopa decarboxylaseinhibitor coadministration viste ca. 2 gange højere AUC- og Cmax-værdier hos patienter med en historie med alkoholisme og leverdæmpning (n = 10) sammenlignet med normale individer (n = 10). Alle patienter havde biopsi-bevist levercirrhose forårsaget af alkohol. Ifølge børnepugh-klassificering havde 7 patienter med leversygdom mild nedsat leverfunktion, og 3 patienter havde moderat leverfunktion. Da kun ca. 10% af entacapon -dosis udskilles i urin, da overordnet forbindelse og konjugeret glucuronid galdesudskillelse ser ud til at være den vigtigste rute for udskillelse af dette lægemiddel. Stalevo bør administreres med omhu til patienter med galdeobstruktion eller lever sygdom.
Levodopa And Carbidopa
Der er ingen undersøgelser af farmakokinetikken af levodopa og carbidopa hos patienter med nedsat leverfunktion.
Geriatrisk brug
I farmakokinetiske undersøgelser udført hos raske frivillige efter en enkelt dosis carbidopa-levodopa- og entacapone (som Stalevo eller som separate carbidopa/levodopa og comtan-tabletter):
Levodopa
Levodopa AUC er signifikant (i gennemsnit 10% til 20%) højere hos ældre (60 år til 75 år) end yngre emner (45 år til 60 år). Der er ingen signifikant forskel i Cmax af levodopa mellem yngre (45 år til 60 år) og ældre emner (60 år til 75 år).
Carbidopa
Der er ingen signifikant forskel i Cmax og AUC af carbidopa mellem yngre (45 år til 60 år) og ældre emner (60 år til 75 år).
Entacapone
AUC for Entacapone er signifikant (i gennemsnit 15%) højere hos ældre (60 år til 75 år) end yngre emner (45 år til 60 år). Der er ingen signifikant forskel i cmax af entacapone mellem yngre (45 år til 60 år) og ældre emner (60 år til 75 år).
Køn
Farmakokinetik following a single dose of carbidopa levodopa og entacapone together either as Stalevo or as separate carbidopa/levodopa og Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Levodopa
Plasmaeksponeringen (AUC og Cmax) af levodopa er signifikant højere hos kvinder end mænd (i gennemsnit 40% for AUC og 30% for Cmax). Disse forskelle forklares primært ved kropsvægt. Anden offentliggjort litteratur viste signifikant kønseffekt (højere koncentrationer hos kvinder), selv efter korrektion for kropsvægt.
Carbidopa
Der er ingen kønsforskel i farmakokinetikken i Carbidopa.
Entacapone
Der er ingen kønsforskel i farmakokinetikken for enacapone.
Lægemiddelinteraktionsundersøgelser
Stofmetaboliseret af COMT
Når en enkelt 400 mg dosis entacapon blev givet sammen med intravenøs isoprenalin (isoproterenol) og epinephrin uden coadministreret levodopa og DOPA -dekarboxylaseinhibitor, var de samlede gennemsnitlige maksimale ændringer i hjerterytmen under infusion ca. 50% og 80% højere end med placebo for ISOPRENALINE og EPINEPINEPINE.
Lægemidler, der vides at være metaboliseret af COMT, skal administreres med forsigtighed hos patienter, der modtager entacapone uanset indgivelsesvejen [se Lægemiddelinteraktioner ].
Lægemidler metaboliseret via CYP2C9
På grund af dens tilknytning til CYP2C9 in vitro entacapone kan potentielt forstyrre medicinske produkter med stofskifte afhængig af dette isoenzym. I en interaktionsundersøgelse hos raske frivillige øgede Entacapone AUC for R-Warfarin i gennemsnit med 18%, og INR-værdierne steg i gennemsnit med 13% [se Lægemiddelinteraktioner ].
Hormonniveauer
Af ingredienserne i Stalevo Levodopa er kendt for at deprimere prolactinsekretion og øge væksthormon niveauer.
Kliniske studier
Effektiviteten af entacapone som et supplement til levodopa i behandlingen af Parkinsons sygdom blev etableret i tre 24-ugers multicenter randomiserede dobbeltblinde placebokontrollerede studier hos patienter med Parkinsons sygdom. I 2 af disse undersøgelser (undersøgelser 1 og 2) svingede patientens sygdom, dvs. var kendetegnet ved dokumenterede perioder med ON (perioder med relativt god funktion) og slukket (perioder med relativt dårlig funktion) på trods af optimal levodopa -terapi. Der var også en tilbagetrækningsperiode efter 6 måneders behandling. I det tredje forsøg blev patienter ikke forpligtet til at have oplevet udsving. Før den kontrollerede del af disse undersøgelser blev patienter stabiliseret på levodopa i 2 uger til 4 uger.
Der er begrænset erfaring med at bruge entacapone hos patienter, der ikke oplever udsving.
I undersøgelser blev 1 og 2 patienter randomiseret til at modtage placebo eller entacapone 200 mg indgivet samtidig med hver dosis carbidopa/levodopa (op til 10 gange dagligt, men patienter var i gennemsnit 4 doser til 6 doser pr. Doser). Den dobbeltblinde del af begge undersøgelser var 6 måneder lang. Patienter registrerede med jævne mellemrum den tid, der blev brugt i on- og off -stater i hjemmedagbøger gennem hele forsøgets varighed. I en undersøgelse udført i de nordiske lande var det primære resultatmål den samlede gennemsnitlige tid, der blev brugt i staten under en 18 timers dagbog registreret dag (kl. 18 til midnat). I den anden undersøgelse var det primære resultatmål andelen af den vågne tid, der blev brugt over 24 timer i staten.
Foruden det primære resultatmål blev målingen af den tid, der blev brugt i off-staten, evalueret, og patienter blev også evalueret ved underdel af Unified Parkinsons sygdomsvurderingsskala (UPDRS) en ofte anvendt multi-post-vurderingsskala, der var beregnet til at vurdere mentation (del I) aktiviteter i daglig levetid (del II) motorfunktion (del III) komplikationer af behandling En efterforsker og patientens globale vurdering af klinisk tilstand en 7-punkts subjektiv skala designet til at vurdere global funktion i Parkinsons sygdom; og ændringen i daglig carbidopa/levodopa dosis.
hvor længe varer metoprolol tartrat
I undersøgelse 1 171 blev patienter randomiseret i 16 centre i Finland Norge Sverige og Danmark (undersøgelse 1), som alle modtog samtidig levodopa plus dopa decarboxylaseinhibitor (enten carbidopa/levodopa eller benserazid/levodopa). I undersøgelse blev 2 205 patienter randomiseret i 17 centre i Nordamerika (USA og Canada); Alle patienter modtog samtidig carbidopa/levodopa.
Følgende tabeller (tabel 4 og tabel 5) viser resultaterne af disse to undersøgelser:
Tabel 4: Effektivitetsresultater af undersøgelse 1
| Primær foranstaltning fra hjemmedagbogen (fra en 18-timers dagbog dag) | |||
| Baseline | Skift fra baseline ved måned 6* | P-værdi vs. placebo | |
| Timer med vågen tid på | |||
| Placebo | 9.2 | 0,1 | - |
| Entacapone | 9.3 | 1.5 | mindre end 0,001 |
| Varighed på tiden efter første AM -dosis (HRS) | |||
| Placebo | 2.2 | 0.0 | - |
| Entacapone | 2.1 | 0,2 | mindre end 0,05 |
| Sekundære foranstaltninger fra hjemmedagbogen (fra en 18-timers dagbog dag) † | |||
| Timer med vågen fritid | |||
| Placebo | 5.3 | 0.0 | - |
| Entacapone | 5.5 | -1.3 | mindre end 0,001 |
| Andel af vågen tid på ‡ (%) | |||
| Placebo | 63.8 | 0,6 | - |
| Entacapone | 62.7 | 9.3 | mindre end 0,001 |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 705 | 14 | - |
| Entacapone | 701 | -87 | mindre end 0,001 |
| Frekvens af levodopa daglige indtag | |||
| Placebo | 6.1 | 0,1 | - |
| Entacapone | 6.2 | - 0,4 | mindre end 0,001 |
| Andre sekundære foranstaltninger | |||
| Baseline | Skift fra baseline i måned 6 | P-værdi vs. placebo | |
| Undersøgerens globale (samlede) % forbedrede§ | |||
| Placebo | - | 28 | - |
| Entacapone | - | 56 | mindre end 0,01 |
| Patientens globale (samlede) % forbedrede§ | |||
| Placebo | - | 22 | - |
| Entacapone | - | 39 | N.S.¶ |
| Updrs i alt | |||
| Placebo | 37.4 | -1.1 | - |
| Entacapone | 38.5 | -4.8 | mindre end 0,01 |
| UPDRS MOTOR | |||
| Placebo | 24.6 | -0.7 | - |
| Entacapone | 25.5 | -3.3 | mindre end 0,05 |
| UPDRS ADL | |||
| Placebo | 11.0 | -0.4 | - |
| Entacapone | 11.2 | -1.8 | mindre end 0,05 |
| *Betyde; Månedens 6-værdier repræsenterer gennemsnittet af uger 8 16 og 24 ved protokoldefineret resultatmål. † P -værdier for sekundære mål er nominelle P -værdier uden nogen justering for mangfoldighed. ‡ Ikke et slutpunkt for denne undersøgelse, men primært slutpunkt i den nordamerikanske undersøgelse. § I mindst en kategoriændring ved slutpunktet. ¶ Ikke væsentligt. |
Tabel 5: Effektivitetsresultater af undersøgelse 2
| Primær foranstaltning fra hjemmedagbogen (til en 24-timers dagbog dag) | |||
| Baseline | Skift fra baseline ved måned 6* | P-værdi vs. placebo | |
| Procent af vågen tid på | |||
| Placebo | 60.8 | 2.0 | - |
| Entacapone | 60.0 | 6.7 | mindre end 0,05 |
| Sekundære foranstaltninger fra hjemmedagbogen (til en døgnåbent dagbog) † | |||
| Timer med vågen fritid | |||
| Placebo | 6.6 | -0.3 | - |
| Entacapone | 6.8 | -1.2 | mindre end 0,01 |
| Timer med vågen tid på | |||
| Placebo | 10.3 | 0,4 | - |
| Entacapone | 10.2 | 1.0 | N.S. ‡ |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 758 | 19 | - |
| Entacapone | 804 | -93 | mindre end 0,001 |
| Frekvens af levodopa daglige indtag | |||
| Placebo | 6.0 | 0,2 | - |
| Entacapone | 6.2 | 0.0 | N.S. ‡ |
| Andre sekundære foranstaltninger† | |||
| Baseline | Skift fra baseline i måned 6 | P-værdi vs. placebo | |
| Undersøgerens globale (samlede) % forbedrede§ | |||
| Placebo | - | 21 | - |
| Entacapone | - | 34 | mindre end 0,05 |
| Patientens globale (samlede) % forbedrede§ | |||
| Placebo | - | 20 | - |
| Entacapone | - | 31 | mindre end 0,05 |
| Updrs i alt¶ | |||
| Placebo | 35.6 | 2.8 | - |
| Entacapone | 35.1 | -0.6 | mindre end 0,05 |
| UPDRS MOTOR ¶ | |||
| Placebo | 22.6 | 1.2 | - |
| Entacapone | 22.0 | -0.9 | mindre end 0,05 |
| UPDRS ADL¶ | |||
| Placebo | 11.7 | 1.1 | - |
| Entacapone | 11.9 | 0.0 | mindre end 0,05 |
| *Betyde; Månedens 6-værdier repræsenterer gennemsnittet af uger 8 16 og 24 ved protokoldefineret resultatmål. † P -værdier for sekundære mål er nominelle P -værdier uden nogen justering for mangfoldighed. ‡ Ikke signifikant. § I mindst en kategoriændring ved slutpunktet. ¶Score ændring ved slutpunkt på lignende måde som den nordiske undersøgelse. |
Effekter på tiden adskiller sig ikke efter alderen Kønsvægtsygdomme ved sværhedsgraden ved baseline levodopa og samtidig behandling med dopaminagonister eller selegilin.
Tilbagetrækning af entacapone
I undersøgelse 2 resulterede pludselig tilbagetrækning af entacapone uden ændring af dosis af carbidopa/levodopa i en signifikant forværring af udsving sammenlignet med placebo. I nogle tilfælde var symptomerne lidt værre end ved baseline, men vendte tilbage til ca. baseline -sværhedsgraden inden for 2 uger efter levodopa -dosisforøgelse i gennemsnit med 80 mg. I undersøgelse 1 blev der ligeledes en signifikant forværring af parkinsoniske symptomer efter entacapone -tilbagetrækning som vurderet 2 uger efter lægemiddeludtrækning. I denne fase var symptomerne omtrent ved baseline -sværhedsgraden efter levodopa -dosis stigning med ca. 50 mg.
I den tredjeplacebokontrollerede undersøgelse (undersøgelse 3) blev i alt 301 patienter randomiseret i 32 centre i Tyskland og Østrig. I dette forsøg som i de andre 2 undersøgelser blev entacapone 200 mg indgivet med hver dosis levodopa og dopa decarboxylaseinhibitor (op til 10 gange dagligt) og UPDRS -dele II og III og total dagligt til tiden var de primære mål for effektiviteten. Resultater for de primære foranstaltninger såvel som for nogle sekundære mål er vist i tabel 6.
Tabel 6: Effektivitetsresultater af undersøgelse 3
| Primære foranstaltninger | |||
| Baseline | Skift fra baseline i måned 6 | P-værdi vs. placebo (LOCF) | |
| Updrsadl* | |||
| Placebo | 12.0 | 0,5 | - |
| Entacapone | 12.4 | -0.4 | mindre end 0,05 |
| UPDRS MOTOR* | |||
| Placebo | 24.1 | 0,1 | - |
| Entacapone | 24.9 | -2.5 | mindre end 0,05 |
| Timer med vågen tid på (Home Diary)† | |||
| Placebo | 10.1 | 0,5 | - |
| Entacapone | 10.2 | 1.1 | N.S. ‡ |
| Sekundære foranstaltninger§ | |||
| Baseline | Skift fra baseline i måned 6 | P-værdi vs. placebo | |
| Updrs i alt * | |||
| Placebo | 37.7 | 0,6 | - |
| Entacapone | 39.0 | -3.4 | mindre end 0,05 |
| Procent af vågen tid på (Home Diary) ** | |||
| Placebo | 59.8 | 3.5 | - |
| Entacapone | 62.0 | 6.5 | N.S. ‡ |
| Timer med vågen fritid (Home Diary) | |||
| Placebo | 6.8 | -0.6 | - |
| Entacapone | 6.3 | -1.2 | 0.07 |
| Levodopa Total Daily Dose (mg)* | |||
| Placebo | 572 | 4 | - |
| Entacapone | 566 | -35 | N.S. |
| Frekvens af levodopa dagligt indtag* | |||
| Placebo | 5.6 | 0,2 | - |
| Entacapone | 5.4 | 0.0 | mindre end 0,01 |
| Global (samlet) % forbedret¶ | |||
| Placebo | - | 34 | - |
| Entacapone | - | 38 | N.S. ‡ |
| *Samlet befolkning; Resultatændring ved slutpunktet. † Fluktuerende population med 5 doser til 10 doser; Resultatændring ved slutpunktet. ‡ Ikke signifikant. §P -værdier for sekundære mål er nominelle P -værdier uden nogen justering for mangfoldighed. ¶Total befolkning; Mindst en kategoriændring ved slutpunktet. |
Patientinformation til Stalevo
Falder i søvn under aktiviteter i dagligdagen og somnolens
Rådgiv patienter om potentialet for beroligende effekter forbundet med Stalevo inklusive somnolens og muligheden for at falde i søvn, mens de deltager i aktiviteter i dagligdagen. Fordi somnolens kan være en hyppig bivirkning med potentielt alvorlige konsekvenser, bør patienter ikke drive et motorkøretøjs drift af tunge maskiner eller deltage i andre potentielt farlige aktiviteter, indtil de har fået tilstrækkelig erfaring med Stalevo til at afgøre, om det påvirker deres mentale og/eller motoriske præstation negativt [se Advarsler og forholdsregler ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Rådgiver patienter til at tale med deres receptpligtige sundhedsydelser, før de tager alkohol -beroligende medicin eller andre CNS -depressiva (f.eks. Benzodiazepiner antipsykotika antidepressiva osv.) På grund af de mulige additive effekter i kombination med Stalevo.
Hypotension Orthostatic Hypotension And Syncope
Rådgiv patienter om, at de kan udvikle symptomatiske (eller asymptomatiske) posturale (ortostatiske) hypotension eller ikke -ortostatisk hypotension, mens de tager Stalevo. Hypotension/ortostatisk hypotension kan forekomme hyppigere under den indledende terapi. Patienter bør ikke stige hurtigt efter at have siddet eller liggende, især hvis de har gjort det i langvarige perioder og især ved påbegyndelse af behandling med Stalevo.
Rådgiv patienter om potentialet for synkope hos patienter, der bruger dopaminagonister. Af denne grund informerer patienter om muligheden for at synkope, mens de tager Stalevo [se Advarsler og forholdsregler ].
Dyskinesis
Informer patienter om, at Stalevo kan forårsage og/eller forværre allerede eksisterende dyskinesier [se Advarsler og forholdsregler ].
Hallucinationer og/eller psykotisk lignende opførsel
Informer patienter om, at hallucinationer og anden psykotisk lignende opførsel kan forekomme, mens Stalevo [se Advarsler og forholdsregler ].
Impulskontrol og/eller tvangsmæssig adfærd
Rådgiv patienter om, at de kan opleve impulskontrol og/eller tvangsmæssig adfærd, mens de tager en eller flere af de medicin, der bruges til behandling af Parkinsons sygdom, herunder Stalevo. Spørg patienter om udviklingen af nye eller øgede spiludtrængninger opfordrer trakes seksuelle trang til opfordringer til ukontrollerede udgifter eller andre intense trang, mens de behandles med Stalevo. Rådgiv patienter om at informere deres læge eller sundhedsudbyder, hvis de oplever nye eller øgede spiludtrækninger øgede seksuelle trang eller andre intense trang, mens de tager Stalevo. Læger skal overveje dosisreduktion eller stoppe medicinen, hvis en patient udvikler sådanne trang, mens de tager Stalevo [se Advarsler og forholdsregler ].
Tilbagetrækning-fremkommende hyperpyrexi og forvirring
Rådgiv patienter om, at de kan udvikle feber og forvirring som en del af et syndrom, der ligner NMS og muligvis med andre kliniske træk (f.eks. Muskelstivhed autonom dysfunktion hyper- eller hypotension osv.). Dette feber- og forvirringssyndrom kan især forekomme med dosisreduktion eller tilbagetrækning af Stalevo, men kan også udvikle sig efter påbegyndelse af behandlingen. Rådgive patienter om at kontakte deres sundhedsudbyder, hvis de ønsker at afbryde eller mindske dosis af Stalevo og til at kontakte en sundhedsudbyder, hvis de udvikler feber og forvirring [se Advarsler og forholdsregler ].
Diarre And Colitis
Informer patienterne om, at diarré kan forekomme med Stalevo, og det kan have en forsinket begyndelse. Undertiden kan langvarig diarré være forårsaget af colitis (betændelse i tarmtarmen). Patienter med diarré skal drikke væsker for at opretholde tilstrækkelig hydrering og overvåge for vægttab. Hvis diarré forbundet med Stalevo forlænges, forventes det at afbryde lægemidlet at føre til opløsning. Hvis diarré fortsætter efter at have stoppet Stalevo, kan det være nødvendigt med yderligere diagnostiske undersøgelser. I nogle tilfælde kan diarré være forbundet med colitis [se Advarsler og forholdsregler ].
Rhabdomyolyse
Rådgiv patienter om, at de kan udvikle rhabdomyolyse og myalgi, hvis de oplever langvarig motorisk aktivitet inklusive dyskinesi. Denne begivenhed kan også være forbundet med feber og forvirring [se Advarsler og forholdsregler ].
Kvalme And Opkast
Informer patienter om, at Stalevo kan forårsage kvalme og opkast kan forekomme hyppigere under den første terapi og kan kræve dosisjustering.
Brug til brug
Instruer patienter om kun at tage Stalevo som foreskrevet. Instruer patienter om kun at tage en enkelt tablet af Stalevo i hvert doseringsinterval. Instruer patienter om ikke at tage flere tabletter eller yderligere dele af tabletter for at opnå en højere dosis levodopa. Rådgiv patienter om ikke at splitte knus eller tygge Stalevo.
Informer patienten om, at Stalevo er en formulering af carbidopa/levodopa kombineret med entacapone, der er designet til at begynde frigivelse af ingredienser inden for 30 minutter efter indtagelse. Det er vigtigt, at Stalevo tages med regelmæssige intervaller i henhold til den tidsplan, der er beskrevet af lægen. FORSIGTIG Patienten om ikke at ændre det foreskrevne doseringsregime og ikke at tilføje yderligere Antiparkinson -medicin, herunder andre Carbidopa/Levodopa -præparater uden først at konsultere lægen.
Rådgive patienter om, at episoder (iført lægemiddeleffekt) forekommer i slutningen af doseringsintervallet, men uforudsigelige episoder kan forekomme når som helst. Rådgive patienten om at underrette en sundhedsudbyder om mulige behandlingsjusteringer, hvis en sådan respons udgør et problem for patientens hverdag.
Rådgive patienter om, at mørk farve (rødbrun eller sort) kan optræde i spyt urin eller sved efter at have taget Stalevo. Selvom farven ser ud til at være klinisk ubetydelige beklædningsgenstande kan blive misfarvet.
Rådgive patienter om, at en ændring i diæt til fødevarer, der er høje i protein, kan forsinke absorptionen af levodopa. Overdreven surhed forsinker også mavetømning og dermed forsinker absorptionen af levodopa. Jernsalte (såsom i tabletter med flere vitamin) kan også reducere effektiviteten af Stalevo.
Graviditet
Instruer patienter om at underrette deres sundhedsudbyder, hvis de bliver gravide eller har til hensigt at blive gravide under terapi [se Brug i specifikke populationer ].
Amning
Instruer patienter om at underrette deres sundhedsudbyder, hvis de har til hensigt at amme eller amme et spædbarn [se Brug i specifikke populationer ].
